铜及其化合物在生产、生活中都有广泛的应用。探究一、铜的性质及其应用(1)化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,下列说法正确的是 ____ (填序号)。A.溶液甲中一定含有Al(NO3)3和Zn(NO3)2B.固体乙中一定含有Ag,可能含有Cu和ZnC.若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2D.向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2(2)碳还原氧化铜的实验装置如图甲、乙所示。C+CuO 气体-|||-澄清的-|||-图 石灰水-|||-甲-|||-K CuO+C-|||-足量-|||-澄清 硫-|||-浓-|||-石灰水 酸-|||-B c DⅠ.甲图中酒精灯上网罩的作用是 ____ 。[提出问题]碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?[作出猜想]猜想①:CO;猜想②:CO2;猜想③:CO和CO2。[设计方案]实验装置如图乙。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。方案一:从定性观察角度判断若B中无明显实验现象,D处气体能被点燃,则猜想①成立。方案二:从定量计算角度判断取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据: 反应前的质量 反应后的质量 A(玻璃管+固体) m1 m2 B+C(广口瓶+混合液) m3 m4 Ⅱ.若猜想②成立,则理论上(m4-m3) ____ (填“<”“=”或“>”)(m1-m2)。Ⅲ.若猜想③成立且CuO全部转化成Cu,则参加反应的碳的质量m的取值范围是 ____ 。(3)兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿)。青铜器属于 ____ (填序号)。铜绿Cu2(OH)2CO3分解的化学方程式为 ____ 。A.无机材料B.合成材料C.复合材料D.复合肥为了弄清铜生成铜绿的条件,某化学实验小组借鉴课本“铁钉锈蚀条件的探究”实验,设计了“铜片锈蚀条件的探究”实验,实验如图1所示(所用铜片洁净、光亮)。C+CuO 气体-|||-澄清的-|||-图 石灰水-|||-甲-|||-K CuO+C-|||-足量-|||-澄清 硫-|||-浓-|||-石灰水 酸-|||-B c D实验较长时间后,发现 ____ (填试管编号)试管中铜片最先生锈。小组讨论后发现实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是:Cu和 ____ (写出试管中需要的物质)。可以省略不做的实验是试管 ____ (填试管编号)。探究二、铜的制备研究铜可采用如下方法制备:方法一:火法炼铜:Cu2S+O2(underline(;高温;))/(;)2Cu+SO2方法二:湿法炼铜:CuSO4+Fe═FeSO4+Cu(4)上述两种方法中,你认为哪种方法更好,原因是 ____ 。辉铜矿的主要成分为Cu2S,常用于火法炼铜。若生成过程中铜元素的转化率为90%,生产64t Cu需要含Cu2S 80%的辉铜矿 ____ t。(保留一位小数)探究三、铜的化合物的制备研究碱式碳酸铜可用于生产木材防腐剂等。工业上可用微蚀刻废液(含有一定量Cu2+、H+、SO42-、H2O2和微量Fe3+)制备高纯度碱式碳酸铜,其制备过程如图2:C+CuO 气体-|||-澄清的-|||-图 石灰水-|||-甲-|||-K CuO+C-|||-足量-|||-澄清 硫-|||-浓-|||-石灰水 酸-|||-B c D(5)加入试剂1的目的是除去废液中的酸性物质,试剂1最好选用 ____ (填序号)。a.Fe2O3b.CaCO3c.CuO(6)加入Na2CO3沉淀前须除去Fe3+,否则Fe2(SO4)3会与Na2CO3反应,产生一种气体,同时生成NaFe3(OH)6(SO4)2沉淀,影响产品质量,请写出反应的化学方程式 ____ 。(7)加入Na2CO3沉淀时,反应液pH对产品中的SO42-含量以及反应液中Cu2+沉淀效率的影响如图3所示,第二次沉淀时溶液pH最好控制在 ____ 。(8)所制得的碱式碳酸铜的组成可表示为:xCuCO3•yCu(OH)2•zH2O。某研究小组设计如图4实验装置测定其中CuCO3的质量分数(不考虑植物油中溶解CO2产生的影响)。C+CuO 气体-|||-澄清的-|||-图 石灰水-|||-甲-|||-K CuO+C-|||-足量-|||-澄清 硫-|||-浓-|||-石灰水 酸-|||-B c D实验步骤如下:①连接装置并检验装置气密性;②准确称量样品的质量1.2g;③装药品,调节量气装置两边液面相平,读取量气管刻度为10mL;④向锥形瓶内加入50mL(足量)的稀硫酸,充分反应;⑤冷却到室温;⑥再次调节量气装置两边液面相平,读取量气管刻度为172mL。Ⅰ.步骤一中检验装置气密性的方法是 ____ 。Ⅱ.装置B的作用是 ____ ,C中的试剂是 ____ (填序号)。a.碱石灰b.浓硫酸c.无水硫酸铜Ⅲ.步骤⑥中调节液面相平的操作是 ____ 。Ⅳ.若标准状况下,每44g二氧化碳的体积为22.4L。根据实验数据计算产品中CuCO3的质量分数(写出计算过程,保留到0.1%)。计算过程:Ⅴ.若其他操作均正确,仅因下列因素可使测定结果偏小的是 ____ (填序号)。A.步骤③中平视刻度,步骤⑥中仰视读数B.硫酸的用量不足C.量气管中未加植物油D.步骤⑥中没有调节量气装置两边液面相平,直接读数(9)碱式碳酸铜【xCuCO3•yCu(OH)2•zH2O】的热分解研究。小组同学用热分析仪对固体进行热分解,获得相关数据,绘成的固体质量与分解温度的关系如图5。(已知Cu(OH)2的分解温度小于CuCO3的分解温度。)Ⅰ.通过计算可得x:y:z= ____ 。Ⅱ.若将16.0g剩余固体继续加热到更高的温度,发现固体质量减少了1.6g后质量不再改变,写出此过程中可能发生反应的化学方程式: ____ 。
铜及其化合物在生产、生活中都有广泛的应用。探究一、铜的性质及其应用
(1)化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,下列说法正确的是 ____ (填序号)。
A.溶液甲中一定含有Al(NO3)3和Zn(NO3)2
B.固体乙中一定含有Ag,可能含有Cu和Zn
C.若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2
D.向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2
(2)碳还原氧化铜的实验装置如图甲、乙所示。
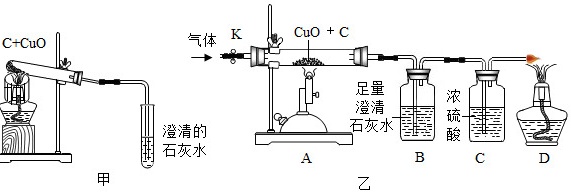
Ⅰ.甲图中酒精灯上网罩的作用是 ____ 。
[提出问题]碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
[作出猜想]猜想①:CO;猜想②:CO2;猜想③:CO和CO2。
[设计方案]实验装置如图乙。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
方案一:从定性观察角度判断
若B中无明显实验现象,D处气体能被点燃,则猜想①成立。
方案二:从定量计算角度判断
取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
| 反应前的质量 | 反应后的质量 | |
| A(玻璃管+固体) | m1 | m2 |
| B+C(广口瓶+混合液) | m3 | m4 |
Ⅲ.若猜想③成立且CuO全部转化成Cu,则参加反应的碳的质量m的取值范围是 ____ 。
(3)兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿)。青铜器属于 ____ (填序号)。铜绿Cu2(OH)2CO3分解的化学方程式为 ____ 。
A.无机材料
B.合成材料
C.复合材料
D.复合肥
为了弄清铜生成铜绿的条件,某化学实验小组借鉴课本“铁钉锈蚀条件的探究”实验,设计了“铜片锈蚀条件的探究”实验,实验如图1所示(所用铜片洁净、光亮)。
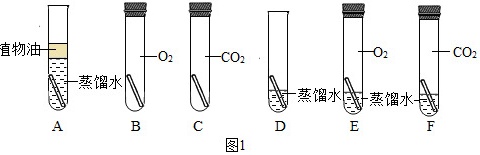
实验较长时间后,发现 ____ (填试管编号)试管中铜片最先生锈。小组讨论后发现实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是:Cu和 ____ (写出试管中需要的物质)。可以省略不做的实验是试管 ____ (填试管编号)。
探究二、铜的制备研究
铜可采用如下方法制备:
方法一:火法炼铜:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2
方法二:湿法炼铜:CuSO4+Fe═FeSO4+Cu
(4)上述两种方法中,你认为哪种方法更好,原因是 ____ 。辉铜矿的主要成分为Cu2S,常用于火法炼铜。若生成过程中铜元素的转化率为90%,生产64t Cu需要含Cu2S 80%的辉铜矿 ____ t。(保留一位小数)
探究三、铜的化合物的制备研究
碱式碳酸铜可用于生产木材防腐剂等。工业上可用微蚀刻废液(含有一定量Cu2+、H+、SO42-、H2O2和微量Fe3+)制备高纯度碱式碳酸铜,其制备过程如图2:
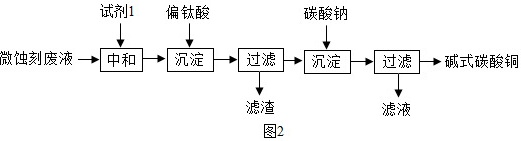
(5)加入试剂1的目的是除去废液中的酸性物质,试剂1最好选用 ____ (填序号)。
a.Fe2O3
b.CaCO3
c.CuO
(6)加入Na2CO3沉淀前须除去Fe3+,否则Fe2(SO4)3会与Na2CO3反应,产生一种气体,同时生成NaFe3(OH)6(SO4)2沉淀,影响产品质量,请写出反应的化学方程式 ____ 。
(7)加入Na2CO3沉淀时,反应液pH对产品中的SO42-含量以及反应液中Cu2+沉淀效率的影响如图3所示,第二次沉淀时溶液pH最好控制在 ____ 。
(8)所制得的碱式碳酸铜的组成可表示为:xCuCO3•yCu(OH)2•zH2O。某研究小组设计如图4实验装置测定其中CuCO3的质量分数(不考虑植物油中溶解CO2产生的影响)。
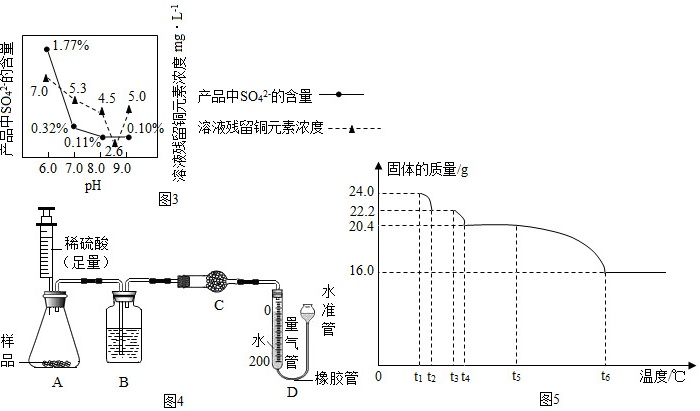
实验步骤如下:①连接装置并检验装置气密性;②准确称量样品的质量1.2g;③装药品,调节量气装置两边液面相平,读取量气管刻度为10mL;④向锥形瓶内加入50mL(足量)的稀硫酸,充分反应;⑤冷却到室温;⑥再次调节量气装置两边液面相平,读取量气管刻度为172mL。
Ⅰ.步骤一中检验装置气密性的方法是 ____ 。
Ⅱ.装置B的作用是 ____ ,C中的试剂是 ____ (填序号)。
a.碱石灰
b.浓硫酸
c.无水硫酸铜
Ⅲ.步骤⑥中调节液面相平的操作是 ____ 。
Ⅳ.若标准状况下,每44g二氧化碳的体积为22.4L。根据实验数据计算产品中CuCO3的质量分数(写出计算过程,保留到0.1%)。
计算过程:
Ⅴ.若其他操作均正确,仅因下列因素可使测定结果偏小的是 ____ (填序号)。
A.步骤③中平视刻度,步骤⑥中仰视读数
B.硫酸的用量不足
C.量气管中未加植物油D.步骤⑥中没有调节量气装置两边液面相平,直接读数
(9)碱式碳酸铜【xCuCO3•yCu(OH)2•zH2O】的热分解研究。小组同学用热分析仪对固体进行热分解,获得相关数据,绘成的固体质量与分解温度的关系如图5。(已知Cu(OH)2的分解温度小于CuCO3的分解温度。)
Ⅰ.通过计算可得x:y:z= ____ 。
Ⅱ.若将16.0g剩余固体继续加热到更高的温度,发现固体质量减少了1.6g后质量不再改变,写出此过程中可能发生反应的化学方程式: ____ 。
参考答案与解析:
-
相关试题
-
铜及其化合物在生产、生活中都有广泛的应用。探究一、铜的性质及其应用(1)化学小组用一定量AgNO_(3)和Al(NO_(3))_(3)的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,下列
-
铜及其化合物在生产、生活中都有广泛的应用。探究一、铜的性质及其应用(1)化学小组用一定量AgNO_(3)和Al(NO_(3))_(3)的混合溶液加入铜粉和锌粉,
- 查看答案
-
在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置
-
[单选题]在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是()A . MgB . CuC . AgD . H2
- 查看答案
-
将一些锌粉加入硝酸银、硝酸铜的混合溶液中,完全反应后过滤。下列说法正确的是
-
[单选题]将一些锌粉加入硝酸银、硝酸铜的混合溶液中,完全反应后过滤。下列说法正确的是A.滤液中一定不含硝酸银,滤纸上一定不含锌,一定不含铜B.滤液中一定含有硝酸锌,滤纸上一定含有银,可能含有铜C.滤液中可能含硝酸锌,滤纸上可能含有铜,也可能含有锌D.滤液中一定含有硝酸银,滤纸上一定含有铜,一定含有锌
- 查看答案
-
在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴
-
[单选题]在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是A.滤出的固体中一定含有铜,可能含有铁和镁B.滤出的固体一定含有铜,一定不含铁和镁C.滤液中一定含有氯化镁和氯化亚铁,可能含有氯化铜D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
- 查看答案
-
(5分)在CuSO4和ZnSO4的混合溶液中加入一定量的铁粉,充分反应后过滤,向
-
[试题](5分)在CuSO4和ZnSO4的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,没有气泡产生,则滤出的固体是________(填名称),滤液中一定含有的溶质为________、________ (填化学式),有关反应的化学方程式为______________________。
- 查看答案
-
同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。(1)若将所得滤渣放入稀盐酸中,有气泡产生,则①滤液里一定
-
同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。(1)若将所得滤渣
- 查看答案
-
贮放AgNO3标准溶液应用()。
-
[填空题] 贮放AgNO3标准溶液应用()。
- 查看答案
-
②将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是
-
[单选题]②将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是______。A.肯定有银B.肯定有铜C.可能有铁D.可能是铁和银
- 查看答案
-
不能鉴别AgNO3、BaCl2、KSO和Mg(NO3)2四种溶液(不考虑它们间的
-
[单选题]不能鉴别AgNO3、BaCl2、KSO和Mg(NO3)2四种溶液(不考虑它们间的相互反应)的试剂组是()。A . 盐酸、硫酸B . 盐酸、氢氧化钠溶液C . 氨水、硫酸D . 氨水、氢氧化钠溶液
- 查看答案
-
计算C(AgNO3)0.1000mol/L的AgNO3溶液对Cl-和NaCL的滴
-
[问答题] 计算C(AgNO3)0.1000mol/L的AgNO3溶液对Cl-和NaCL的滴定度?(相对原子质量:(Cl=35.5,Na=23)
- 查看答案