三草酸合铁(Ⅲ)酸钾(K3[Fe(C2O4)3]•3H2O)是一种经典的光敏剂,也是制备负载型活性铁催化剂的主要原料。用废铁铬(含少量Al2O3、Fe2O3)先制备草酸铁,然后再制备三草酸合铁(Ⅲ)酸钾。Ⅰ.制备草酸亚铁过量废铁屑 碳酸钠 K2C2O4-|||-稀硫酸 反应I 调节pH 过滤 FeSO4 反应Ⅱ → 过滤 →FeC2O4·2H2O溶液-|||-滤渣已知:部分氢氧化物沉淀时溶液的pH如下表: 沉淀物 Fe(OH)3 Fe(OH)2 Al(OH)3 开始沉淀 2.3 7.5 3.4 完全沉淀 3.2 9.7 4.4 (1)加入过量废铁屑的主要目的是 ____ (双选)。A.提高铁的利用率B.除去溶液中的Fe3+C.防止Fe2+被氧化D.抑制Fe2+的水解(2)加入少量Na2CO3后,混合溶液pH范围应调控在 ____ 。A.3.2以下B.3.2∼3.4C.4.4∼7.5D.7.5以上(3)写出反应Ⅱ的离子方程式: ____ 。(4)关于K2C2O4溶液中有关离子浓度的说法正确的是 ____ (不定项)。A.[K+]+[H+]=2[C2(O)_(4)^2-]+[HC2(O)_(4)^-]+[OH-]B.2[K+]=[C2(O)_(4)^2-]+[HC2(O)_(4)^-]+[H2C2O4]C.[HC2(O)_(4)^-]+[H2C2O4]+[H+]=[OH-]D.对溶液进行稀释,[C2(O)_(4)^2-]与[HC2(O)_(4)^-]的比值变小Ⅱ.制备三草酸合铁(Ⅲ)酸钾步骤一:在草酸亚铁固体中,加入饱和K2C2O4溶液;步骤二:保持恒温40℃,边搅拌边缓慢加入3%H2O2溶液,直至氧化完全;步骤三:将溶液加热至沸,加入饱和H2C2O4溶液,溶液转为绿色,获得三草酸合铁(Ⅲ)酸钾溶液。(5)从步骤三所得溶液获得三草酸合铁(Ⅲ)酸钾晶体的操作依次为水浴浓缩、 ____ 、 ____ ,然后用乙醇淋洗。(6)步骤二使用H2O2做氧化剂,其优点是 ____ ;滴加H2O2时需保持恒温40℃,原因是 ____ 。(7)三草酸合铁(Ⅲ)酸钾溶液中存在如下过程:[Fe(C2O4)3]3-(aq)⇌Fe3+(aq)+C2(O)_(4)^2-(aq),某同学想检验C2(O)_(4)^2-的存在,结合CaC2O4属于难溶电解质的特点,他向三草酸合铁(Ⅲ)酸钾溶液中加入CaCl2溶液,并未看到有沉淀生成。从平衡角度解释上述现象 ____ 。Ⅲ.三草酸合铁(Ⅲ)酸钾含量测定测定三草酸合铁(Ⅲ)酸钾样品纯度的方法如下:称取样品0.2415g,放入250mL锥形瓶中,加入25mL水和5mL1mol•L-1H2SO4,用0.0200mol•L-1KMnO4标准溶液滴定至终点,反应原理为:2KMnO4+5H2C2O4+3H2SO4═2MnSO4+K2SO4+10CO2↑+8H2O(8)确认滴定终点的操作是 ____ 。(9)若最终消耗KMnO4标准溶液23.19mL,则样品纯度为 ____ (精确到0.1%)。(已知K3[Fe(C2O4)3]•3H2O的摩尔质量为491g•mol-1)
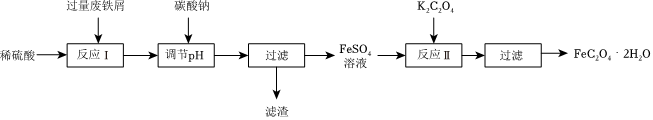
三草酸合铁(Ⅲ)酸钾(K3[Fe(C2O4)3]•3H2O)是一种经典的光敏剂,也是制备负载型活性铁催化剂的主要原料。用废铁铬(含少量Al2O3、Fe2O3)先制备草酸铁,然后再制备三草酸合铁(Ⅲ)酸钾。Ⅰ.制备草酸亚铁
已知:部分氢氧化物沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
A.提高铁的利用率
B.除去溶液中的Fe3+
C.防止Fe2+被氧化
D.抑制Fe2+的水解
(2)加入少量Na2CO3后,混合溶液pH范围应调控在 ____ 。
A.3.2以下
B.3.2∼3.4
C.4.4∼7.5
D.7.5以上
(3)写出反应Ⅱ的离子方程式: ____ 。
(4)关于K2C2O4溶液中有关离子浓度的说法正确的是 ____ (不定项)。
A.[K+]+[H+]=2[C2${O}_{4}^{2-}$]+[HC2${O}_{4}^{-}$]+[OH-]
B.2[K+]=[C2${O}_{4}^{2-}$]+[HC2${O}_{4}^{-}$]+[H2C2O4]
C.[HC2${O}_{4}^{-}$]+[H2C2O4]+[H+]=[OH-]
D.对溶液进行稀释,[C2${O}_{4}^{2-}$]与[HC2${O}_{4}^{-}$]的比值变小
Ⅱ.制备三草酸合铁(Ⅲ)酸钾
步骤一:在草酸亚铁固体中,加入饱和K2C2O4溶液;
步骤二:保持恒温40℃,边搅拌边缓慢加入3%H2O2溶液,直至氧化完全;
步骤三:将溶液加热至沸,加入饱和H2C2O4溶液,溶液转为绿色,获得三草酸合铁(Ⅲ)酸钾溶液。
(5)从步骤三所得溶液获得三草酸合铁(Ⅲ)酸钾晶体的操作依次为水浴浓缩、 ____ 、 ____ ,然后用乙醇淋洗。
(6)步骤二使用H2O2做氧化剂,其优点是 ____ ;滴加H2O2时需保持恒温40℃,原因是 ____ 。
(7)三草酸合铁(Ⅲ)酸钾溶液中存在如下过程:[Fe(C2O4)3]3-(aq)⇌Fe3+(aq)+C2${O}_{4}^{2-}$(aq),某同学想检验C2${O}_{4}^{2-}$的存在,结合CaC2O4属于难溶电解质的特点,他向三草酸合铁(Ⅲ)酸钾溶液中加入CaCl2溶液,并未看到有沉淀生成。从平衡角度解释上述现象 ____ 。
Ⅲ.三草酸合铁(Ⅲ)酸钾含量测定
测定三草酸合铁(Ⅲ)酸钾样品纯度的方法如下:
称取样品0.2415g,放入250mL锥形瓶中,加入25mL水和5mL1mol•L-1H2SO4,用0.0200mol•L-1KMnO4标准溶液滴定至终点,反应原理为:
2KMnO4+5H2C2O4+3H2SO4═2MnSO4+K2SO4+10CO2↑+8H2O
(8)确认滴定终点的操作是 ____ 。
(9)若最终消耗KMnO4标准溶液23.19mL,则样品纯度为 ____ (精确到0.1%)。
(已知K3[Fe(C2O4)3]•3H2O的摩尔质量为491g•mol-1)
参考答案与解析:
-
相关试题
-
Fe2O3理论含铁()。
-
[单选题]Fe2O3理论含铁()。A .70%B .80%C .56%D .65%
- 查看答案
-
铁催化剂在还原前的主要成份是Fe2O3和FeO。
-
[判断题] 铁催化剂在还原前的主要成份是Fe2O3和FeO。A . 正确B . 错误
- 查看答案
-
铁氧化物的还原顺序Fe3O4→Fe2O3→FeO→Fe。
-
[判断题] 铁氧化物的还原顺序Fe3O4→Fe2O3→FeO→Fe。A . 正确B . 错误
- 查看答案
-
中变铁铬系催化剂的活性组分为Fe3O4。
-
[判断题] 中变铁铬系催化剂的活性组分为Fe3O4。A . 正确B . 错误
- 查看答案
-
热轧板表面的氧化铁皮主要是:三氧化二铁(Fe2O3)、四氧化三铁(Fe3O4)和
-
[判断题] 热轧板表面的氧化铁皮主要是:三氧化二铁(Fe2O3)、四氧化三铁(Fe3O4)和氧化铁(FeO)。A . 正确B . 错误
- 查看答案
-
铁催化剂还原后的活性组分是Fe3O4。
-
[判断题] 铁催化剂还原后的活性组分是Fe3O4。A . 正确B . 错误
- 查看答案
-
16.重铬酸钠(Na2Cr3O)广泛应用于医药和印染行业,用含铬矿渣(主要成分是Cr2O3,还含有少量-|||-Fe2O3和Al2O3)制备Na2Cr2O7的流程如下:-|||-O 2 H2O H2S
-
16.重铬酸钠(Na2Cr3O)广泛应用于医药和印染行业,用含铬矿渣(主要成分是Cr2O3,还含有少量-|||-Fe2O3和Al2O3)制备Na2Cr2O7的流
- 查看答案
-
中温变换催化剂活性组分是Fe2O3。
-
[判断题] 中温变换催化剂活性组分是Fe2O3。A . 正确B . 错误
- 查看答案
-
铁系合成氨催化剂中所添加的Al2O3的作用?
-
[问答题] 铁系合成氨催化剂中所添加的Al2O3的作用?
- 查看答案
-
以Al2O3催化剂的制备为例,说明沉淀法制备催化剂的过程?
-
[问答题] 以Al2O3催化剂的制备为例,说明沉淀法制备催化剂的过程?
- 查看答案