请说明下列公式的使用条件 因为状态函数与过程无关.0 ℃; 101.3 kPa下; 1 mol冰熔化成水; 吸热 6.02 kJ;此过程 △G =0..液体水在100℃;下气化为水蒸气;此过程的ΔU > 0;ΔH > 0;ΔS= > 0;ΔG = 0101.3 kPa下; 1 mol的 100 ℃水与 100 ℃的大热源相接触; 经过两种不同的过程到达终态 100 ℃; 101.3 kPa的水蒸气: (1)保持压力不变; (2)向真空膨胀.试分别计算这两种过程的 Q; W;△U;△H;△S;△A及△G 并判断过程是否可逆.已知 100℃;101.3 kPa下水的气化热△vapH = 40.71 kJ.mol; V(l) = 18.8×10 m.mol; V(g) = 3.02×10 m.mol.
请说明下列公式的使用条件 (3分)
(1) dS = Q/dT (2)ΔH = nCp;m(T2-T1) (3)ΔG =ΔH - TΔS
答:(1)dS = Q/dT :可逆过程 (2)ΔH = nCp;m(T2-T1) :恒压且热容与温度无关
(3)ΔG =ΔH – TΔS :恒温
;是非题
.( )能发生的过程一定是自发过程。
.( )功可以全部转变成热;但热一定不能全部转化为功。
.( )从单一热源吸取热量而全部变为功是可能的。
.( )家里没有空调;可以打开冰箱门来代替空调达到降温的目的。
.( )所有绝热过程的Q为零;△S也必为零。
.( )熵值不可能为负值。
.( )某一化学反应的热效应被反应温度T除;即得此反应的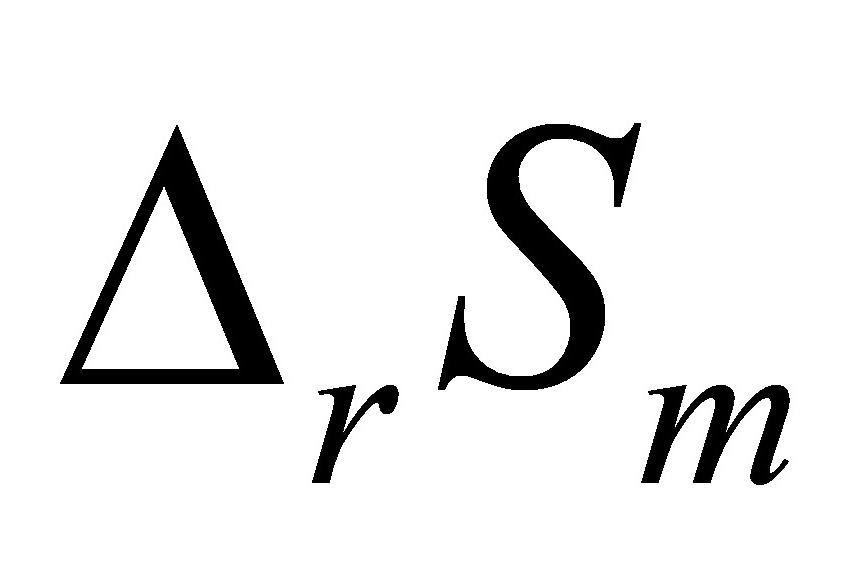
.( )因为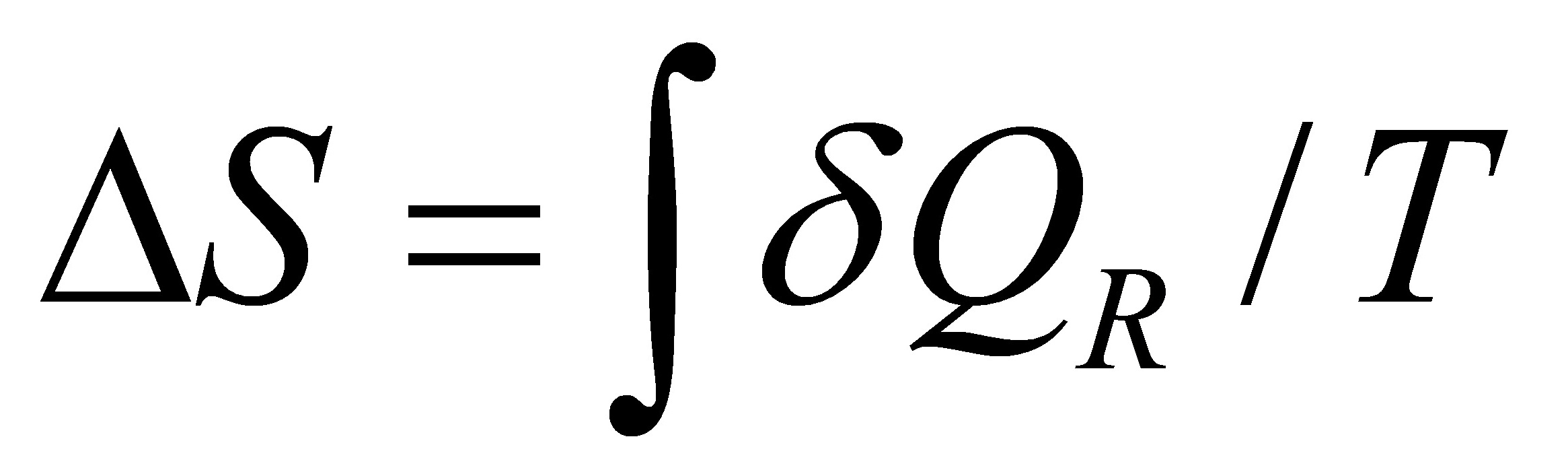 ;所以只有可逆过程才有熵变;而
;所以只有可逆过程才有熵变;而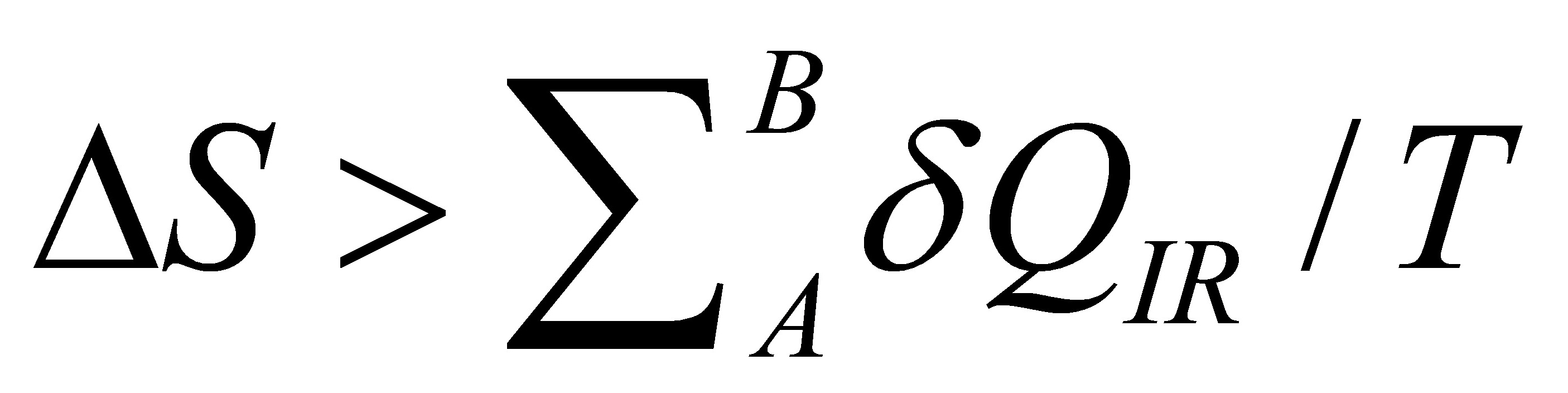 ;扬以不可逆过程只有热温商;没有熵变。
;扬以不可逆过程只有热温商;没有熵变。
.( )物质的标准熵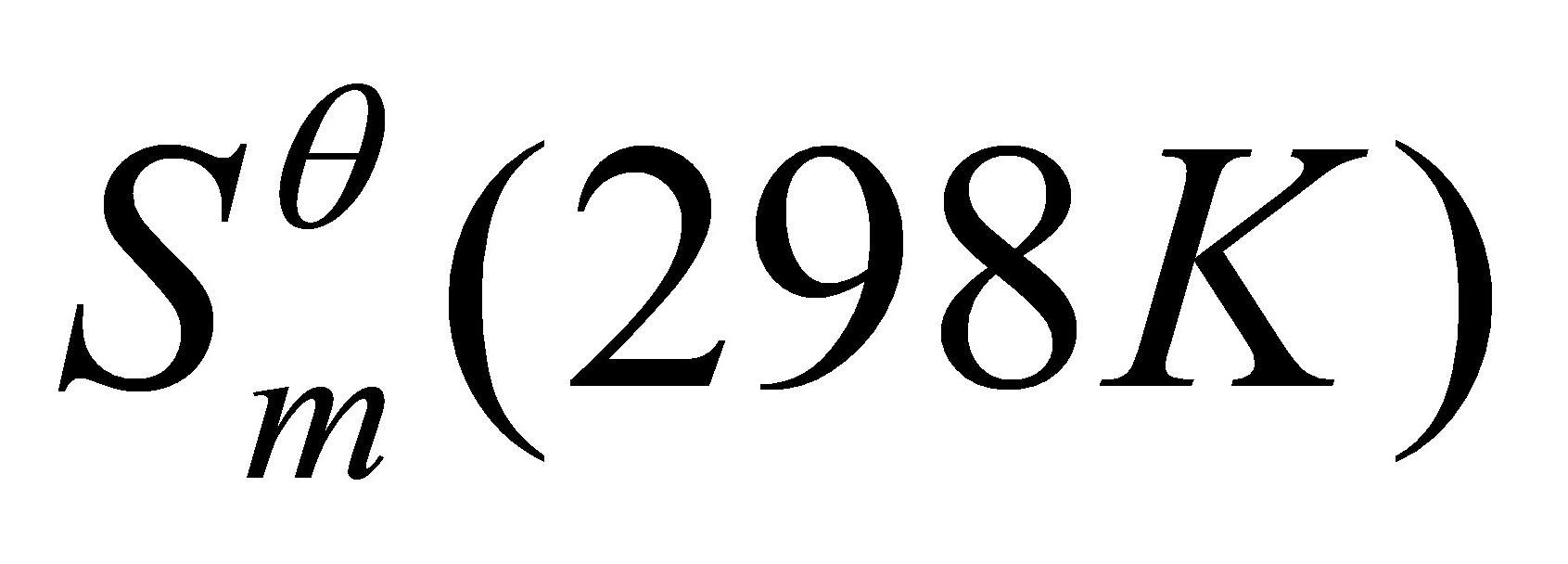 值是该状态下熵的绝对值。
值是该状态下熵的绝对值。
.( )理想气体绝热可逆过程的△S一定为零;△G不一定为零。
.( )体系达到平衡时熵值最大;吉布斯函数最小。
.( )在绝热恒容的反应器中;H2和Cl2化合成HCl;此过程的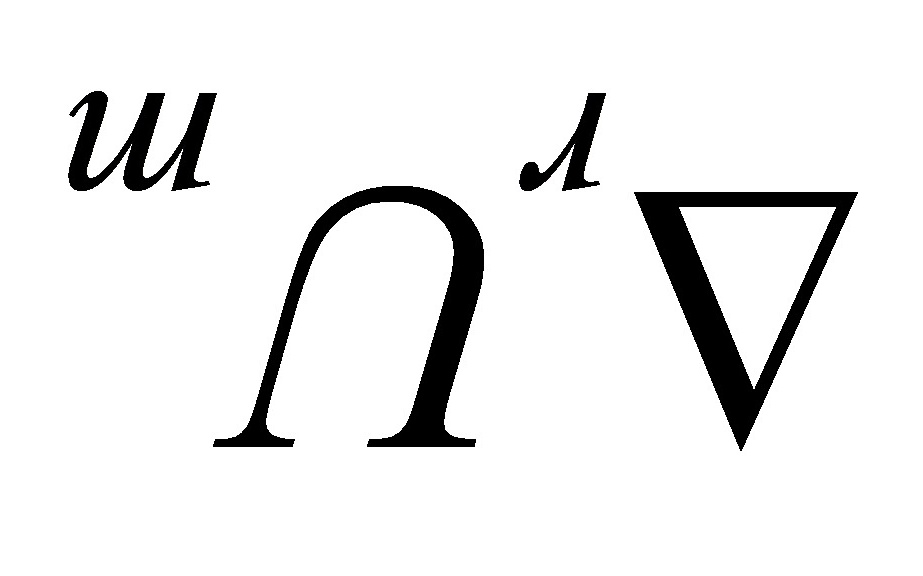 为零。
为零。
.( )水在100℃;102325Pa下沸腾;吉布斯函数会减少。
.( )△G代表在恒温恒压条件下;体系对外做功的最大能力。
.( )隔离体系的熵恒定不变。
.( )不可逆过程必为自发过程。
.( )ΔrGm>0的反应;是不可能进行的反应。
;填空题
.一个过程系统的熵变为△S; 而另一个过程的始终态与前过程相同;但路径不同;则此过程系统的熵变应为__△S___。(1分)
因为状态函数与过程无关
.0 ℃; 101.3 kPa下; 1 mol冰熔化成水; 吸热 6.02 kJ;此过程 △G =0.
.液体水在100℃;下气化为水蒸气;此过程的
ΔU > 0;ΔH > 0;ΔS= > 0;ΔG = 0
(填“>”、“<”或“=”
.101.3 kPa下; 1 kg 100 ℃的水蒸气冷凝为同温度下的水;此过程 △S(系统)
<0; △S(总) =0 ( 填 >; < 或 = ).
;计算题
.(15分)101.3 kPa下; 1 mol的 100 ℃水与 100 ℃的大热源相接触; 经过两种不同的过程到达终态 100 ℃; 101.3 kPa的水蒸气: (1)保持压力不变; (2)向真空膨胀.试分别计算这两种过程的 Q; W;△U;△H;△S;△A及△G 并判断过程是否可逆.已知 100℃;101.3 kPa下水的气化热△vapH = 40.71 kJ.mol; V(l) = 18.8×10 m.mol; V(g) = 3.02×10 m.mol.
参考答案与解析:
-
相关试题
-
在101.3kPa下,110℃的水变为110℃水蒸气,吸热Qp,在该相变过程中下
-
[单选题]在101.3kPa下,110℃的水变为110℃水蒸气,吸热Qp,在该相变过程中下列哪个关系式不成立?()A . ΔS体>0B . ΔS环不确定C . ΔS体+ΔS环>0D . ΔG体<0
- 查看答案
-
(相变熵)101.3 kPa下, 25 ℃的 1 mol水蒸发成同温度的蒸气,此过程系统的熵变△S。
-
(相变熵)101.3 kPa下, 25 ℃的 1 mol水蒸发成同温度的蒸气,此过程系统的熵变△S。(相变熵)101.3 kPa下, 25 ℃的 1 mo
- 查看答案
-
1mol水在373K和100kPa向真空蒸发,变成373K和100kPa的水蒸气,试计算此过程的△S体系、△S环境和△S总,并判断此过程是否自发。水的蒸发热为40.64kJ/mol
-
1mol水在373K和100kPa向真空蒸发,变成373K和100kPa的水蒸气,试计算此过程的△S体系、△S环境和△S总,并判断此过程是否自发。水的蒸发热为4
- 查看答案
-
试计算1mol 液态甲苯在100℃、p下气化为100℃、p下1mol 气态甲苯过程的△H、△S,并说明此变化过程的方向性。已知甲苯在其正常沸点110℃时的气化热为33.30 kJ·mol-1,C6
-
试计算1mol 液态甲苯在100℃、p下气化为100℃、p下1mol 气态甲苯过程的△H、△S,并说明此变化过程的方向性。已知甲苯在其正常沸点110℃时的气
- 查看答案
-
在298K、101.325kPa下,1mol过冷水蒸气变为298K、101.325kPa的液态水,求此过程的△S及△G。已知298K水的饱和蒸汽压为3.1674kPa,气化热为2217kJ/kg。上述
-
在298K、101.325kPa下,1mol过冷水蒸气变为298K、101.325kPa的液态水,求此过程的△S及△G。已知298K水的饱和蒸汽压为3.1674
- 查看答案
-
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
-
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝
- 查看答案
-
下列固体属于受热先熔化成液体,再由液体吸热蒸发产生可燃蒸气的是()。
-
[单选题]下列固体属于受热先熔化成液体,再由液体吸热蒸发产生可燃蒸气的是()。A .樟脑B .石蜡C .萘D .涤纶
- 查看答案
-
1mol 25°C,101.3kPa液态水向真空膨胀成25°C,101.3kPa水蒸气的△G大于零。
-
1mol 25°C,101.3kPa液态水向真空膨胀成25°C,101.3kPa水蒸气的△G大于零。A. 正确B. 错误
- 查看答案
-
在100℃,101325Pa下,1mol水全部向真空容器气化为100℃,101325Pa的蒸气,则该过程
-
在100℃,101325Pa下,1mol水全部向真空容器气化为100℃,101325Pa的蒸气,则该过程A. ΔG0,不可逆
- 查看答案
-
体积为1m3的冰块全部熔化成水后,水的质量是 kg,水的体积是 。(冰的密度为0
-
[主观题]体积为1m3的冰块全部熔化成水后,水的质量是 kg,水的体积是 。(冰的密度为0.9×103kg/m3)
- 查看答案