例 7-5 CO(CH2 COOH)2在水溶液中的分解为一级反应。在333.15K和283.15K温度下-|||-的速率常数分别为 .484times (10)^-2(s)^-1 和 https:/img.zuoyebang.cc/zyb_a4650e95e835546706ea1b75c0b8ea9a.jpg.080times (10)^-4(s)^-1, 求该反应的活化能和在303.15K下的速率常-|||-数k303.15。
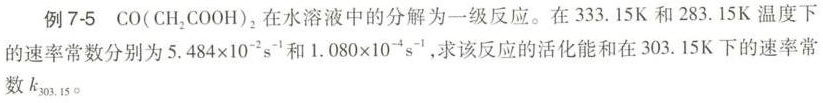
参考答案与解析:
-
相关试题
-
假设主、副反应的速度常数分别为k1和k2,则选择因子(S)为()。
-
[填空题] 假设主、副反应的速度常数分别为k1和k2,则选择因子(S)为()。
- 查看答案
-
已知反应(Ni(s) + 4CO(g) = Ni(CO)_4(g)),当温度为323K和503K时,测得其标准平衡常数分别为3.89 times 10^4和1.92 times 10^-5。(1) 计
-
已知反应(Ni(s) + 4CO(g) = Ni(CO)_4(g)),当温度为323K和503K时,测得其标准平衡常数分别为3.89 times 10^4和1.
- 查看答案
-
I.设反应①Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常数为K1。反应②Fe(s)+H2O(g) FeO(s)+H2(g)的平衡常数为K2,在不同温度下,K1、K2的值如下:T(K)K
-
I.设反应①Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常数为K1。反应②Fe(s)+H2O(g) FeO(s)+H2(g)的平衡常数为K2,在不
- 查看答案
-
1.N2O5的分解反应 _(2)(O)_(5)arrow 2N(O)_(2)+(1/2)(O)_(2) 是一级反应,已知在某温度下的速率系数为-|||-.8times (10)^-4(s)^-1-||
-
1.N2O5的分解反应 _(2)(O)_(5)arrow 2N(O)_(2)+(1/2)(O)_(2) 是一级反应,已知在某温度下的速率系数为-|||-.8ti
- 查看答案
-
1-1 级对峙反应由纯 A 开始反应,当进行到A和B浓度相等的时间为:(正、逆向反应速率常数分别为k1 ,k2) ()
-
1-1 级对峙反应由纯 A 开始反应,当进行到A和B浓度相等的时间为:(正、逆向反应速率常数分别为k1 ,k2) ()A. t=ln(k1/k2)B. t=1/
- 查看答案
-
98K时,A、B两种气体在水中的亨利常数分别为k1和k2,且k1>k2,则当P1
-
[单选题]98K时,A、B两种气体在水中的亨利常数分别为k1和k2,且k1>k2,则当P1=P2时,A、B在水中的溶解量C1和C2的关系为()A . C1>C2B . C1<C2C . C1=C2D . 不能确定
- 查看答案
-
1.4 在0℃和1 atm下,测得一铜块的体胀系数和等温压缩系数分别为 alpha =4.85times (10)^-5(k)^-1 和 _(T)=7.8times -|||-^-7a(tan )^-
-
1.4 在0℃和1 atm下,测得一铜块的体胀系数和等温压缩系数分别为 alpha =4.85times (10)^-5(k)^-1 和 _(T)=7.8tim
- 查看答案
-
乙酸酐按下式水解为乙酸:(CH3CO)2O + H2O--2CH3COOH,实验测定该反应为一级不可逆反应,在288K时,反应速率常数k为0.0806min-1。现设计以理想反应器,每天处理乙酸酐14
-
乙酸酐按下式水解为乙酸:(CH3CO)2O + H2O--2CH3COOH,实验测定该反应为一级不可逆反应,在288K时,反应速率常数k为0.0806min-1
- 查看答案
-
300K 时,一级对峙反应 A overset (K_{1)}( arrow ) B 的平衡常数 K_(ell )=2, 且 k_(1)=0.244s^-1。 在此温度下逆反应的速率系数 k_(-1
-
300K 时,一级对峙反应 A overset (K_{1)}( arrow ) B 的平衡常数 K_(ell )=2, 且 k_(1)=0.244s^-1。
- 查看答案
-
1.3在0℃和1pn下,测得一铜块的体胀系数和等温压缩系数分别为 alpha =4.85times -|||-^-5(k)^-1 和 _(r)=7.8times (10)^-7(p)_(n)-1 α和
-
1.3在0℃和1pn下,测得一铜块的体胀系数和等温压缩系数分别为 alpha =4.85times -|||-^-5(k)^-1 和 _(r)=7.8times
- 查看答案