CuSO4·H2O中,中心离子(CuSO4·H2O)的配位分子数是( )
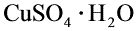 中,中心离子(
中,中心离子(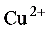 )的配位分子数是( )。
)的配位分子数是( )。
B. 2
C. 1
D. 4
参考答案与解析:
-
相关试题
-
4-1-1-2 在50℃下,CuSO4•5H2O(s)与CuSO4•3H2O(s)平衡共存时,气相中水蒸气的分压力为6.27kPa;CuSO4•3H2O(s)与CuSO4•H2O(s)平衡共存时,气相
-
4-1-1-2 在50℃下,CuSO4•5H2O(s)与CuSO4•3H2O(s)平衡共存时,气相中水蒸气的分压力为6.27kPa;CuSO4•3H2O(s)与
- 查看答案
-
CuSO4与水可生成 CuSO4H2O, CuSO4 3H2O, CuSO4 5H2O 三种水合物,则在一定温度下与水蒸气平衡的含水盐最多为:
-
CuSO4与水可生成 CuSO4H2O, CuSO4 3H2O, CuSO4 5H2O 三种水合物,则在一定温度下与水蒸气平衡的含水盐最多为:A. 3种B. 2
- 查看答案
-
准确称取CuSO4・5H2O(摩尔质量为63.546)0.3229g,溶于水中,
-
[单选题]准确称取CuSO4・5H2O(摩尔质量为63.546)0.3229g,溶于水中,加几滴H2SO4,转入100mL容量瓶中,用水稀释到刻度,摇匀。则此溶液浓度为()。A . B . C . D .
- 查看答案
-
制备CuSO4可以采取如图4所示的三种途径。下列说法正确的是( )。①稀H2SO4、稀HNO3-|||-②O2、△-|||-Cu CuSO4-|||-70%H2SO4-|||-③浓H2SO4,△-|
-
制备CuSO4可以采取如图4所示的三种途径。下列说法正确的是( )。①稀H2SO4、稀HNO3-|||-②O2、△-|||-Cu CuSO4-|||-70%H
- 查看答案
-
配制1mg/mL的Cu2+标准滴定溶液的方法如下:准确称取CuSO4・5H2O(
-
[单选题]配制1mg/mL的Cu2+标准滴定溶液的方法如下:准确称取CuSO4・5H2O(摩尔质量为63.546)(),溶于水中,加几滴H2SO4,转入100mL容量瓶中,用水稀释到刻度,摇匀。
- 查看答案
-
硫酸工业在国民经济中占有重要地位。(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO4·5H2O)取精华法”。借助现代仪器分析,该制备过程中CuSO4·5H2O分解的TG曲线(热重)及DSC曲线
-
硫酸工业在国民经济中占有重要地位。(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO4·5H2O)取精华法”。借助现代仪器分析,该制备过程中CuSO4·5
- 查看答案
-
H2O分子和HCl分子间存在:
-
H2O分子和HCl分子间存在:A. 色散力B. 化学键C. 取向力
- 查看答案
-
【题文】用胆矾(CuSO4·5H2O)配制0.1mol/L的硫酸铜溶液,下列操作中正确的是( )
-
【题文】用胆矾(CuSO4·5H2O)配制0.1mol/L的硫酸铜溶液,下列操作中正确的是( )A. 取25g胆矾溶于1L水中B. 取16g胆矾溶于水配成1L溶
- 查看答案
-
12.已知H与O可以形成H2O和H2O 2两种化合物。请完成下列空白:-|||-(1)H2O内的 -H 水分子间的范德华力和氢键,从强到弱依次为-|||-__ H^+ 可与H2O形成 _(3)(O)^
-
12.已知H与O可以形成H2O和H2O 2两种化合物。请完成下列空白:-|||-(1)H2O内的 -H 水分子间的范德华力和氢键,从强到弱依次为-|||-__
- 查看答案
-
配合物(NH4)2[FeF5(H2O)]的系统命名为(),配离子的电荷是(),配
-
[填空题] 配合物(NH4)2[FeF5(H2O)]的系统命名为(),配离子的电荷是(),配位体是(),配位原子是(),中心离子的配位数是()。根据价键理论,中心原子的杂化轨道为(),属()型配合物。
- 查看答案