4 -17 已知CaF2溶解度为 times (10)^-4molcdot (L)^-1 ,求其溶度积K
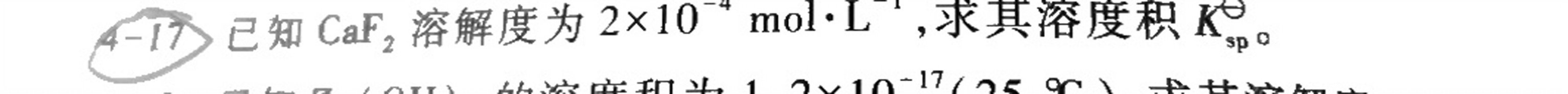
参考答案与解析:
-
相关试题
-
Mg(OH())_(2)在水中的溶解度为1.12times (10)^-4molcdot (dm)^-3。(1)试求其溶度积常数(K)_(sp)。(2)如果在0.10(dm)^3, 0.10molcd
-
Mg(OH())_(2)在水中的溶解度为1.12times (10)^-4molcdot (dm)^-3。(1)试求其溶度积常数(K)_(sp)。(2)如果在0
- 查看答案
-
已知298.15K 时,将电极 /(Cd)^2+(1.00times (10)^-4molcdot (L)^-1) 和 |(Fe)^2+(1.00molcdot (L)^-1) 组成-|||-原电池。
-
已知298.15K 时,将电极 /(Cd)^2+(1.00times (10)^-4molcdot (L)^-1) 和 |(Fe)^2+(1.00molcdot
- 查看答案
-
例:计算0.1molcdot L^-1和1.0times10^-4molcdot L^-1NH4Cl溶液的pH,已知NH3的K_(b)=1.8times10^-5。
-
例:计算0.1molcdot L^-1和1.0times10^-4molcdot L^-1NH4Cl溶液的pH,已知NH3的K_(b)=1.8times10^-
- 查看答案
-
已知298.15K时Ag2CrO4的溶解度为1.0×10-4mol/L,则该温度下Ag2CrO4的标准溶度积常数为( )
-
已知298.15K时Ag2CrO4的溶解度为1.0×10-4mol/L,则该温度下Ag2CrO4的标准溶度积常数为( )A. 1.0×10-12B. 1.0×1
- 查看答案
-
7.计算下列电极在298K时的电极电势:-|||-(1) |(H)^+(1.0times (10)^-2molcdot (L)^-1) ^2+(1.0times (10)^-4molcdot (L)^
-
7.计算下列电极在298K时的电极电势:-|||-(1) |(H)^+(1.0times (10)^-2molcdot (L)^-1) ^2+(1.0times
- 查看答案
-
Ag2CrO4在纯水中的溶解度S=5.0×10-5mol/L,则其溶度积(),K
-
[填空题] Ag2CrO4在纯水中的溶解度S=5.0×10-5mol/L,则其溶度积(),KspAg2CrO4在0.01 mol/L AgNO3溶液中的溶解度()。
- 查看答案
-
[例 -11 已知BaSO4的-|||-=1.08times 10-10, 分别计-|||-算BaSO4-|||-(1)在纯水中的溶解度;-|||-(2)在 .10molcdot L-1BaCl2 溶
-
[例 -11 已知BaSO4的-|||-=1.08times 10-10, 分别计-|||-算BaSO4-|||-(1)在纯水中的溶解度;-|||-(2)在 .
- 查看答案
-
已知C、A、F2的溶解度为2×10-4mol/L,则C、A、F2的溶度积为()
-
[单选题]已知C、A、F2的溶解度为2×10-4mol/L,则C、A、F2的溶度积为()A .3.2×10-11B .4×10-8C .3.2×10-13D .8×10-12
- 查看答案
-
8.36 在298.15K时,Ag2CrO4的溶度积Ksp为 .21times (10)^-12 ,求Ag2CrO4在以下溶液中的-|||-溶解度:-|||-(1)纯水中;-|||-(2) .002m
-
8.36 在298.15K时,Ag2CrO4的溶度积Ksp为 .21times (10)^-12 ,求Ag2CrO4在以下溶液中的-|||-溶解度:-|||-(
- 查看答案
-
CaF2的溶度积的表达式KSP()。
-
[填空题] CaF2的溶度积的表达式KSP()。
- 查看答案