本题为rm(《)化学与生活rm(()选修rm(1)》)选做题。 rm((1))保持营养平衡、合理使用药物,有利于人体健康。现有下列四种物质: A.葡萄糖 rm(B.)氨基酸 rm(C.)青霉素 rm(D.)维生素rm(C) 请根据题意,选择恰当的选项,用字母代号填空。 rm(①)蛋白质水解的最终产物是________; rm(②)人体内重要的供能物质,能发生银镜反应的是________; rm(③)能阻止多种细菌生长,使用前要进行皮肤敏感实验的是_________; rm(④)具有较强的还原性,广泛存在于新鲜水果和蔬菜中的是_________。 rm((2))化学式材料科学发展的基础,合理使用材料有利于人类的生产和生活。 请根据题意,选择恰当的选项,用字母代号填空。 rm(①)光导纤维被称为信息高速公路的骨架,其主要成分是_________: A.硅 rm(B.)二氧化硅 rm(C.)硅酸 rm(②)塑料、合成纤维和合成橡胶是人们常说的三大合成材料。我国航天服外层是用一种特殊的高强度涤纶制成的。涤纶属于_________: A.塑料 rm(B.)合成纤维 rm(C.)合成橡胶 rm(③)钢铁在潮湿的空气中容易发生电化学腐蚀,其负极反应为_________: A.rm(Fe - 2e^-= Fe^2+) rm(B.O_{2)+2H_(2)O + 4e^- = 4OH^-} rm(C.2H^++2e^- = H_{2)↑} rm((3))防治环境污染,改善生态环境,已成为全球共识。 rm(①)酸雨是指rm(pH)小于rm(5.6)的降水,下列汽油排放的是_________rm(()填字母代号rm()) A.rm(CO_{2)} rm(B.CH_{4)} rm(C.SO_{2)} rm(②)废塑料制品造成的“白色污染”已成为社会一大公害,下列治理“白色污染”的方法中,不可取的是_________rm(()填字母代号rm()) A.焚烧废塑料 rm(B.)减少使用塑料 rm(C.)回收和再利用废塑料 rm(③)使用重金属离子超标的水,会危害人体健康,利用沉淀反应可以除去水中的重金属离子。例如,向含有rm(Hg^2+)的废水中rm(Na_{2)S}含有rm(Hg^2+)沉淀而出去。请写出该反应的离子该反应的离子方程式__________。 本题为rm(《)化学反应原理rm(》()选修rm(4),每空rm(2)分,共rm(20)分rm()) rm((1))水溶液中的离子平衡是中学化学中重要知识。 rm(①)常温下,rm(0.001mol/LNaOH)溶液的rm(pH=)_____________; rm(②(NH_{4))_(2)SO_(4)}是一种重要的氮肥,长期施用会使土壤酸化,其原因是______rm(()用离子方程式表示rm()); rm(③)已知在rm(25℃):rm(AgCl(s)⇌ Ag^+(aq)+Cl^-(aq) K_{sp)=1.8×10^-10} rm(Ag_{2)S(s)⇌ 2Ag^+(aq)+S^2-(aq) K_(sp)=6.3×10^-50} 向和浓度均为rm(0.001mol/L)的混合溶液中,逐滴加入rm(AgNO_{3)}溶液,最先产生的沉淀是________rm(()填“rm(AgCl)”或“rm(Ag)rm({,!)_(2)}rm(S)”rm())。 rm((2))甲醇是可再生能源,其燃烧热为rm(726.5kJ·mol^-1)。下列能正确表示甲醇燃烧的热化学方程式的是________rm(()填字母代号rm())。 A.rm(CH_{3)OH(l)+ dfrac(3)(2)O_(2)(g)=CO_(2)(g)+2H_(2)O(l)} rm(triangle H=+726.5kJ·mol^-1) B.rm(CH_{3)OH(l)+ dfrac(3)(2)O_(2)(g)=CO_(2)(g)+2H_(2)O(l)} rm(triangle H=—726.5kJ·mol^-1) C.rm(CH_{3)OH+ dfrac(3)(2)O_(2)=CO_(2)+2H_(2)O} rm(triangle H=—726.5kJ·mol^-1) rm((3)800℃),向某恒容密闭容器中充入反应物rm(A),发生反应rm(2A(g)⇌ 2B(g)+C(g) triangle H < 0)。已知rm(A)的浓度随时间的变化如下: 反应时间rm(((min) ) rm(0) rm(10) rm(20) rm(30) rm(40) rm(50) rm(60) rm(c(A)(mol/L)) rm(1.0) rm(0.80) rm(0.67) rm(0.58) rm(0.43) rm(0.50) rm(0.50) 请回答下列问题: rm(①)在rm(10-20min)内,rm(A)的平均反应速率为_______rm(mol/(L.min)); rm(②)不能说明该反应达到化学平衡状态的是_________rm(()填字母代号rm()); A.容器内气体密度不再变化 B.容器内气体密度不再变化 C.容器内气体的压强不再变化 rm(③800℃)时,平衡常数rm(K=)________; rm(④)若温度将为rm(600℃),其平衡常数rm(K)将_______rm(()填“增大”、“减小”、或“不变”rm())。 rm((4))如图所示,闭合rm(S)后不久,可观察到滤纸rm(a)端附近呈蓝色,则: 电源 s-|||-a b--|||-滤纸条(浸有 KI说 粉溶液) rm(①)滤纸rm(b)端与电源_________rm(()填“正极”或“负 极”rm())相连; rm(②)滤纸rm(a)端发生的电极反应式为_______
本题为$\rm{《}$化学与生活$\rm{(}$选修$\rm{1)》}$选做题。
$\rm{(1)}$保持营养平衡、合理使用药物,有利于人体健康。现有下列四种物质:
A.葡萄糖 $\rm{B.}$氨基酸 $\rm{C.}$青霉素 $\rm{D.}$维生素$\rm{C}$
请根据题意,选择恰当的选项,用字母代号填空。
$\rm{①}$蛋白质水解的最终产物是________;
$\rm{②}$人体内重要的供能物质,能发生银镜反应的是________;
$\rm{③}$能阻止多种细菌生长,使用前要进行皮肤敏感实验的是_________;
$\rm{④}$具有较强的还原性,广泛存在于新鲜水果和蔬菜中的是_________。
$\rm{(2)}$化学式材料科学发展的基础,合理使用材料有利于人类的生产和生活。
请根据题意,选择恰当的选项,用字母代号填空。
$\rm{①}$光导纤维被称为信息高速公路的骨架,其主要成分是_________:
A.硅 $\rm{B.}$二氧化硅 $\rm{C.}$硅酸
$\rm{②}$塑料、合成纤维和合成橡胶是人们常说的三大合成材料。我国航天服外层是用一种特殊的高强度涤纶制成的。涤纶属于_________:
A.塑料 $\rm{B.}$合成纤维 $\rm{C.}$合成橡胶
$\rm{③}$钢铁在潮湿的空气中容易发生电化学腐蚀,其负极反应为_________:
A.$\rm{Fe - 2e^{-}= Fe^{2+}}$ $\rm{B.O_{2}+2H_{2}O + 4e^{-} = 4OH^{-}}$ $\rm{C.2H^{+}+2e^{-} = H_{2}↑}$
$\rm{(3)}$防治环境污染,改善生态环境,已成为全球共识。
$\rm{①}$酸雨是指$\rm{pH}$小于$\rm{5.6}$的降水,下列汽油排放的是_________$\rm{(}$填字母代号$\rm{)}$
A.$\rm{CO_{2}}$ $\rm{B.CH_{4}}$ $\rm{C.SO_{2}}$
$\rm{②}$废塑料制品造成的“白色污染”已成为社会一大公害,下列治理“白色污染”的方法中,不可取的是_________$\rm{(}$填字母代号$\rm{)}$
A.焚烧废塑料 $\rm{B.}$减少使用塑料 $\rm{C.}$回收和再利用废塑料
$\rm{③}$使用重金属离子超标的水,会危害人体健康,利用沉淀反应可以除去水中的重金属离子。例如,向含有$\rm{Hg^{2+}}$的废水中$\rm{Na_{2}S}$含有$\rm{Hg^{2+}}$沉淀而出去。请写出该反应的离子该反应的离子方程式__________。
本题为$\rm{《}$化学反应原理$\rm{》(}$选修$\rm{4}$,每空$\rm{2}$分,共$\rm{20}$分$\rm{)}$
$\rm{(1)}$水溶液中的离子平衡是中学化学中重要知识。
$\rm{①}$常温下,$\rm{0.001mol/LNaOH}$溶液的$\rm{pH=}$_____________;
$\rm{②(NH_{4})_{2}SO_{4}}$是一种重要的氮肥,长期施用会使土壤酸化,其原因是______$\rm{(}$用离子方程式表示$\rm{)}$;
$\rm{③}$已知在$\rm{25℃}$:$\rm{AgCl(s)⇌ Ag^{+}(aq)+Cl^{-}(aq) K_{sp}=1.8×10^{-10}}$
$\rm{Ag_{2}S(s)⇌ 2Ag^{+}(aq)+S^{2-}(aq) K_{sp}=6.3×10^{-50}}$
向和浓度均为$\rm{0.001mol/L}$的混合溶液中,逐滴加入$\rm{AgNO_{3}}$溶液,最先产生的沉淀是________$\rm{(}$填“$\rm{AgCl}$”或“$\rm{Ag}$$\rm{{\,\!}_{2}}$$\rm{S}$”$\rm{)}$。
$\rm{(2)}$甲醇是可再生能源,其燃烧热为$\rm{726.5kJ·mol^{-1}}$。下列能正确表示甲醇燃烧的热化学方程式的是________$\rm{(}$填字母代号$\rm{)}$。
A.$\rm{CH_{3}OH(l)+ \dfrac{3}{2}O_{2}(g)=CO_{2}(g)+2H_{2}O(l)}$ $\rm{\triangle H=+726.5kJ·mol^{-1}}$
B.$\rm{CH_{3}OH(l)+ \dfrac{3}{2}O_{2}(g)=CO_{2}(g)+2H_{2}O(l)}$ $\rm{\triangle H=—726.5kJ·mol^{-1}}$
C.$\rm{CH_{3}OH+ \dfrac{3}{2}O_{2}=CO_{2}+2H_{2}O}$ $\rm{\triangle H=—726.5kJ·mol^{-1}}$
$\rm{(3)800℃}$,向某恒容密闭容器中充入反应物$\rm{A}$,发生反应$\rm{2A(g)⇌ 2B(g)+C(g) \triangle H < 0}$。已知$\rm{A}$的浓度随时间的变化如下:
反应时间$\rm{((min) }$ | $\rm{0}$ | $\rm{10}$ | $\rm{20}$ | $\rm{30}$ | $\rm{40}$ | $\rm{50}$ | $\rm{60}$ |
$\rm{c(A)(mol/L)}$ | $\rm{1.0}$ | $\rm{0.80}$ | $\rm{0.67}$ | $\rm{0.58}$ | $\rm{0.43}$ | $\rm{0.50}$ | $\rm{0.50}$ |
请回答下列问题:
$\rm{①}$在$\rm{10-20min}$内,$\rm{A}$的平均反应速率为_______$\rm{mol/(L.min)}$;
$\rm{②}$不能说明该反应达到化学平衡状态的是_________$\rm{(}$填字母代号$\rm{)}$;
A.容器内气体密度不再变化
B.容器内气体密度不再变化
C.容器内气体的压强不再变化
$\rm{③800℃}$时,平衡常数$\rm{K=}$________;
$\rm{④}$若温度将为$\rm{600℃}$,其平衡常数$\rm{K}$将_______$\rm{(}$填“增大”、“减小”、或“不变”$\rm{)}$。
$\rm{(4)}$如图所示,闭合$\rm{S}$后不久,可观察到滤纸$\rm{a}$端附近呈蓝色,则:
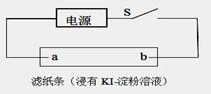
$\rm{①}$滤纸$\rm{b}$端与电源_________$\rm{(}$填“正极”或“负 极”$\rm{)}$相连;
$\rm{②}$滤纸$\rm{a}$端发生的电极反应式为_______
参考答案与解析:
-
相关试题
-
CH_{4)}rm(b. CH≡CH)rm(c. CH_{3)CH_(2)OH} rm(②)下列化合物中,能发生水解反应的是 rm(()填字母rm())。 rm(a.)葡萄糖rm(b.)乙酸rm(c
-
CH_{4)}rm(b. CH≡CH)rm(c. CH_{3)CH_(2)OH} rm(②)下列化合物中,能发生水解反应的是 rm(()填字母rm())。 r
- 查看答案
-
核外电子层结构相同的一组粒子是 ______ A.rm(Mg^2+)、rm(Al^3+)、rm(Cl^-)、rm(Ne) rm(B.Na^+)、rm(F^-)、rm(S^2-)、rm(Ar)
-
核外电子层结构相同的一组粒子是 ______ A.rm(Mg^2+)、rm(Al^3+)、rm(Cl^-)、rm(Ne) rm(B.Na^+)、rm(F
- 查看答案
-
精氨酸的rm pK1=2.17、rm pK2=9.04(rm a-NH3)、rm pK3=12.48(胍基),rm pI=( )
-
精氨酸的rm pK1=2.17、rm pK2=9.04(rm a-NH3)、rm pK3=12.48(胍基),rm pI=( )A. $\rm\frac1
- 查看答案
-
已知rm varphi ^circleddash (rm Sn^2 /Sn)=-0.138rm V,rm varphi ^circleddash (rm Sn^4 /Sn^2 )=0.154
-
已知rm varphi ^circleddash (rm Sn^2 /Sn)=-0.138rm V,rm varphi ^circleddash (rm
- 查看答案
-
某温度下,在rm(2L)的密闭容器中,加入rm(1molX(g))和rm(2molY(g))发生反应:rm(X(g)+mY(g)⇌3Z(g)),平衡时,rm(X)、rm(Y)、rm(Z)的体积分数分别
-
某温度下,在rm(2L)的密闭容器中,加入rm(1molX(g))和rm(2molY(g))发生反应:rm(X(g)+mY(g)⇌3Z(g)),平衡时,rm(X
- 查看答案
-
在rm(100 mL 0.10 mol·L^-1)的rm(AgNO_{3)}溶液中加入rm(100 mL) 溶有rm(2.08 g BaCl_{2)}的溶液,再加入rm(100 mL)溶有rm(0.0
-
在rm(100 mL 0.10 mol·L^-1)的rm(AgNO_{3)}溶液中加入rm(100 mL) 溶有rm(2.08 g BaCl_{2)}的溶液,再
- 查看答案
-
下列说法错误的是rm(() rm())
-
下列说法错误的是rm(() rm())A. 胶体粒子能透过滤纸,但不能透过半透膜B. 胶体和溶液的本质区别在于分散质粒子大小C. 蛋清、豆浆、墨水都是胶体D.
- 查看答案
-
某多孔储氢材料前驱体结构如图。已知(rm M)、(rm W)、(rm X)、(rm Y)、(rm Z)五种元素原子序数依次增大,基态(rm Z)原子的电子填充了(rm 3)个能级,其中有(rm 2)个
-
某多孔储氢材料前驱体结构如图。已知(rm M)、(rm W)、(rm X)、(rm Y)、(rm Z)五种元素原子序数依次增大,基态(rm Z)原子的电子填充了
- 查看答案
-
rm(()一rm()) rm(()Ⅰrm()50mL0.5mol·L^-1)的盐酸与rm(50mL0.55mol·L^-1)的rm(NaOH)溶液在下图所示的位置中进行中和反应。通过测定反应过程中放出
-
rm(()一rm()) rm(()Ⅰrm()50mL0.5mol·L^-1)的盐酸与rm(50mL0.55mol·L^-1)的rm(NaOH)溶液在下图所示的位
- 查看答案
-
已知用rm 0.1000 mathrm(molcdot L^-1) NaOH 滴定rm 20.00 ml同浓度的rm HCl 溶液,突跃范围为4.30~9.70。如果rm NaOH 和rm H
-
已知用rm 0.1000 mathrm(molcdot L^-1) NaOH 滴定rm 20.00 ml同浓度的rm HCl 溶液,突跃范围为4.30~9.
- 查看答案