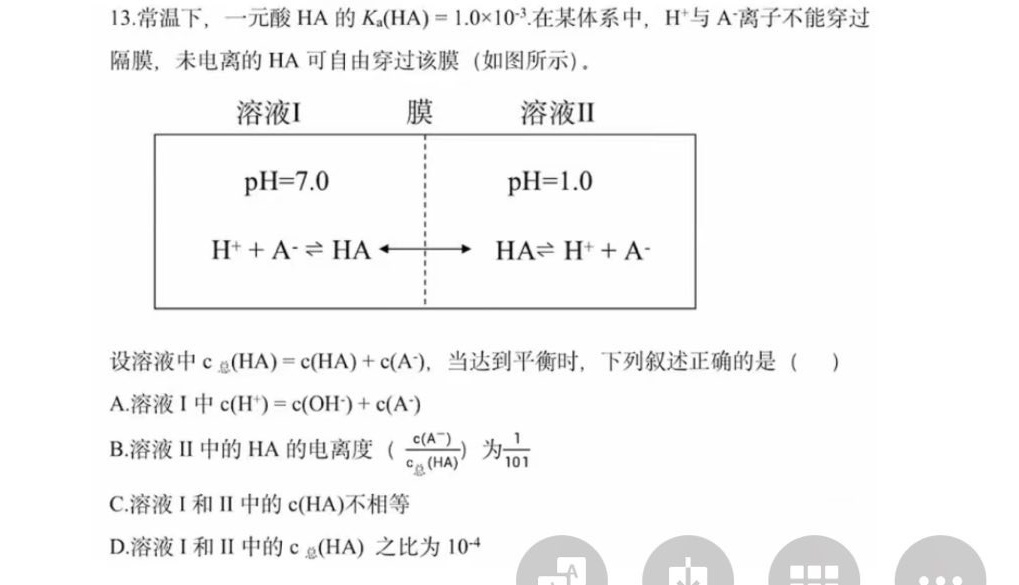
13.常温下,一元酸HA的 _(a)(HA)=1.0times (10)^-3 在某体系中, ^+ 与 ^- 离子不能穿过-|||-隔膜,未电离的HA可自由穿过该膜(如图所示),-|||-溶液I 膜 溶液II-|||-=7.0 =1.0-|||-H^++A^-=HA HA=H^++A^--|||-设溶液中 _(a)(HA)=c(HA)+c((A)^-), 当达到平衡时,下列叙述正确的是 ()-|||-A.溶液I中 ((H)^+)=c((OH)^-)+c((A)^-)-|||-B.溶液Ⅱ中的HA的电离度 (dfrac (c({A)^-)}({c)_(A)(HA)}) 为dfrac (1)(101)-|||-C.溶液I和Ⅱ中的c(H A)不相等-|||-D.溶液I和Ⅱ中的c.(HA)之比为 -4
参考答案与解析:
-
相关试题
-
溶液I 膜 溶液Ⅱ-|||-=7.0 =1.0-|||-H^++A^- =HA^+ +=(H)^++(A)^-常温下,一元酸HA的Ka(HA)=1.0×10-3。在某体系中,H+与A-离子不能穿过隔膜
-
溶液I 膜 溶液Ⅱ-|||-=7.0 =1.0-|||-H^++A^- =HA^+ +=(H)^++(A)^-常温下,一元酸HA的Ka(HA)=1.0×10-3
- 查看答案
-
0.10 mol⋅L−1 HA 溶液中有 1% 的 HA 电离,则 HA 的电离平衡常数 Ka,为( )A.1.0×10−5B.1.0×10−7C.1.0×10−8D.1.0×10−9
-
0.10 mol⋅L−1 HA 溶液中有 1% 的 HA 电离,则 HA 的电离平衡常数 Ka,为( )A.1.0×10−5B.1.0×10−7C.1.0
- 查看答案
-
已知室温时,0.1mo1£¯L某一元酸HA在水中有0.1%发生电离,下列叙述错误
-
[单选题]已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:A.该溶液的pH=4B.升高温度,溶液的pH增大C.此酸的电离平衡常数约为1×10-7D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
- 查看答案
-
某弱酸 HA 的 K a =1.0 × 10 -3 , 1.0mol/L 的该酸水溶液的 pH 为()。
-
某弱酸 HA 的 K a =1.0 × 10 -3 , 1.0mol/L 的该酸水溶液的 pH 为()。A. 3.0B. 2.0C. 1.5D. 6.0
- 查看答案
-
一元弱酸HA在溶液中以HA和A-两种型体存在,若一元弱酸的解离常数为Ka,两种型体的分布分数分别为δHA和δA-,当pH=pKa时,δHA()δA-;当pHpKa时,δHA()δA-,溶液中以()为主
-
一元弱酸HA在溶液中以HA和A-两种型体存在,若一元弱酸的解离常数为Ka,两种型体的分布分数分别为δHA和δA-,当pH=pKa时,δHA()δA-;当pHpK
- 查看答案
-
对于一元弱酸HA,当溶液中HA型体占优势时,此时pH_pKa
-
对于一元弱酸HA,当溶液中HA型体占优势时,此时pH_pKa对于一元弱酸HA,当溶液中HA型体占优势时,此时pH_pKa
- 查看答案
-
称取不纯一元酸HA试样1.600g,溶解后稀释至60.00mL,以0.2500molcdot L^-1NaOH溶液滴定。已知当HA被中和中一半时,溶液pH=5.00,,而中和到终点时,溶液pH=9.0
-
称取不纯一元酸HA试样1.600g,溶解后稀释至60.00mL,以0.2500molcdot L^-1NaOH溶液滴定。已知当HA被中和中一半时,溶液pH=5.
- 查看答案
-
已知KA(HA)=1.0×10-7,在0.1mol/LHA溶液中,pH值为()
-
[单选题]已知KA(HA)=1.0×10-7,在0.1mol/LHA溶液中,pH值为()A .7.0B .6.0C .8.0D . D.4.0
- 查看答案
-
某弱酸HA的Ka=1.0×10-4,则1.0mol·L-1的溶液的pH为()。
-
[单选题]某弱酸HA的Ka=1.0×10-4,则1.0mol·L-1的溶液的pH为()。A . 4.00B . 3.00C . 2.00D . 6.00
- 查看答案
-
若 cHA·Ka≥10−8,该一元弱酸 HA 可用强碱准确滴定;对应一元 共轭碱也可用强酸准确滴定。
-
若 cHA·Ka≥10−8,该一元弱酸 HA 可用强碱准确滴定;对应一元 共轭碱也可用强酸准确滴定。A. 正确B. 错误
- 查看答案