氯化亚铜(CuCl)是一种重要的化工产品。它不溶于H2SO4、HNO3 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],n随着环境酸度的改变而改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图:硝酸铵、水、硫酸 (NH4)2SO3、NH4Cl-|||-海绵铜→ 溶解 → 过滤 滤液 还原 过滤 滤渣 水洗 → 操作1 → 烘干-|||-T-|||-滤渣 滤液 CuCl固体(1)还原过程中主要反应的离子方程式为_______。(2)实验室为了加快过滤速度,往往采用抽滤的操作(如图)。仪器A的名称__________,有关抽滤,下列说法正确的是__________D.原子半径:r(W)>r(Z)>r(Y)6.下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是选项实验器材相应实验A天平(带砝码)、100mL容量瓶、烧杯、胶头滴管用NaCl固体配制100mL 1.00 mol/LNaCI 溶液B烧杯、环形玻璃搅拌棒、碎泡沫塑料、硬纸板中和反应反应热的测定C酸/碱式滴定管、滴定管夹、烧杯、锥形瓶、铁架台实验测定酸碱滴定曲线D三脚架、酒精灯、坩埚、坩埚钳、镊子、泥三角、滤纸、小刀、玻璃片钠在空气中燃烧
氯化亚铜(CuCl)是一种重要的化工产品。它不溶于H2SO4、HNO3 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],n随着环境酸度的改变而改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图: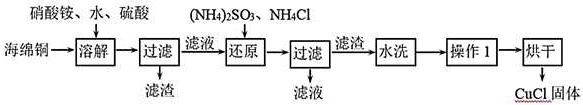 (1)还原过程中主要反应的离子方程式为_______。(2)实验室为了加快过滤速度,往往采用抽滤的操作(如图)。仪器A的名称__________,有关抽滤,下列说法正确的是__________D.原子半径:r(W)>r(Z)>r(Y)6.下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是
(1)还原过程中主要反应的离子方程式为_______。(2)实验室为了加快过滤速度,往往采用抽滤的操作(如图)。仪器A的名称__________,有关抽滤,下列说法正确的是__________D.原子半径:r(W)>r(Z)>r(Y)6.下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是| 选项 | 实验器材 | 相应实验 |
| A | 天平(带砝码)、100mL容量瓶、烧杯、胶头滴管 | 用NaCl固体配制100mL 1.00 mol/LNaCI 溶液 |
| B | 烧杯、环形玻璃搅拌棒、碎泡沫塑料、硬纸板 | 中和反应反应热的测定 |
| C | 酸/碱式滴定管、滴定管夹、烧杯、锥形瓶、铁架台 | 实验测定酸碱滴定曲线 |
| D | 三脚架、酒精灯、坩埚、坩埚钳、镊子、泥三角、滤纸、小刀、玻璃片 | 钠在空气中燃烧 |
| 元素 | X | Y | Z |
| 单质与H2反应条件 | 暗处爆炸 | 光照 | 高温、高压、催化剂 |
| 常温下氢化物水溶液的pH | 小于7 | 小于7 | 大于7 |
 B.
B. C.
C. D.
D. 10.下列关于有机化合物的说法正确的是A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别B.异丁烷的一氯代物有3种C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯11.NA为阿伏加德罗常数的值,下列说法正确的是( )A.标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NAB.标准状况下,22.4L氖气含有的电子数为10NAC.常温下,
10.下列关于有机化合物的说法正确的是A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别B.异丁烷的一氯代物有3种C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯11.NA为阿伏加德罗常数的值,下列说法正确的是( )A.标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NAB.标准状况下,22.4L氖气含有的电子数为10NAC.常温下,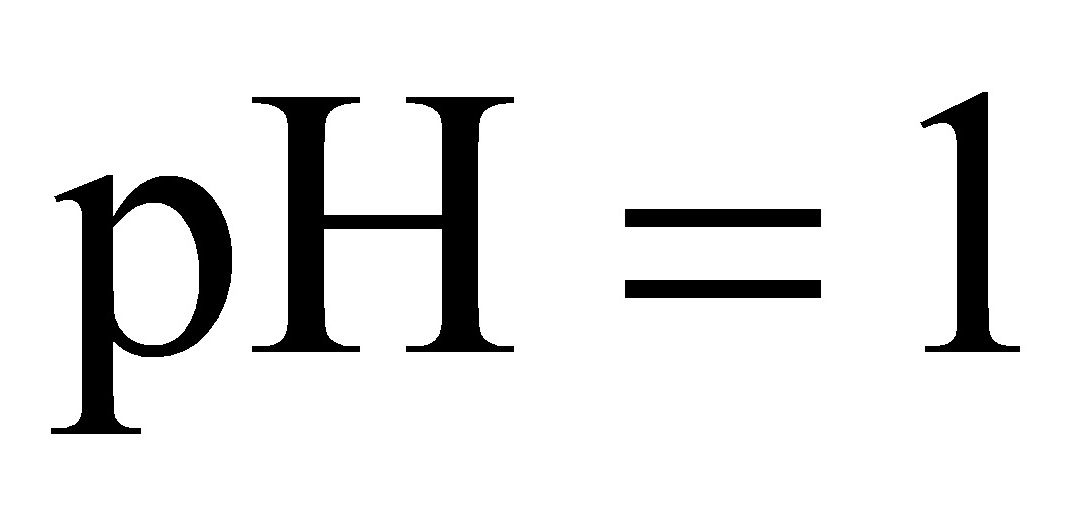 的醋酸溶液中含有的
的醋酸溶液中含有的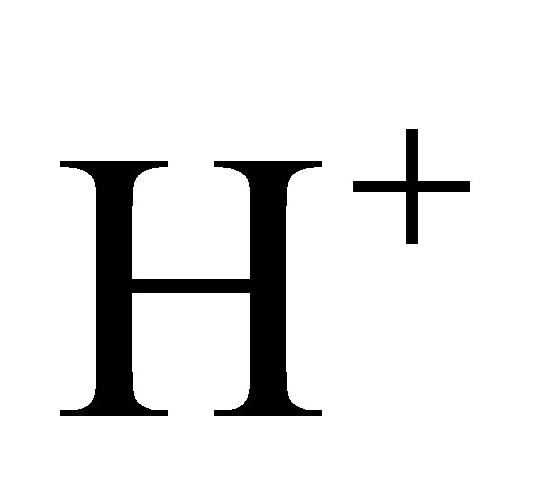 数为
数为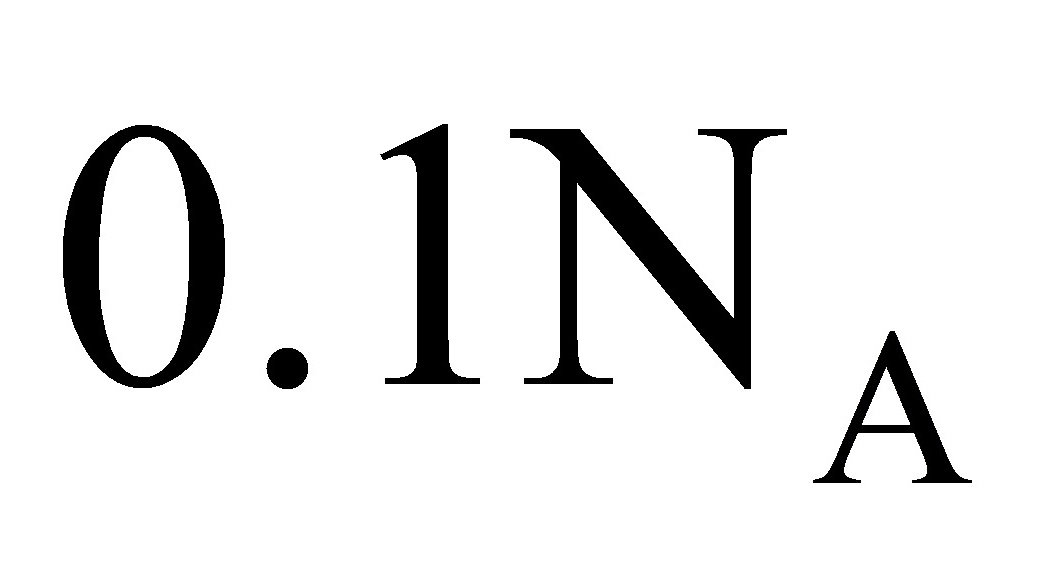 D.120g NaHSO4分子中阳离子和阴离子的总数为3NA12.由下列实验及现象推出的相应结论正确的是( )
D.120g NaHSO4分子中阳离子和阴离子的总数为3NA12.由下列实验及现象推出的相应结论正确的是( )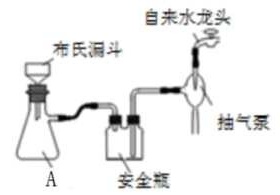 A.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶上口倒出B.在布氏漏斗中放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤C.在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸D.减压过滤不宜用于过滤胶状或颗粒太小的沉淀(3)操作1为马上再洗涤,然后在真空干燥机内于70℃干燥2h,冷却、密封包装。其中最合理的洗涤试剂__________A.浓盐酸 B.浓氨水 C.无水乙醇 D.水+乙醇真空干燥的原因是___________。(4)随着pH减小,Cu2(OH)4-nCln中铜的质量分数__________A.增大 B.不变 C.减小 D.不能确定
A.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶上口倒出B.在布氏漏斗中放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤C.在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸D.减压过滤不宜用于过滤胶状或颗粒太小的沉淀(3)操作1为马上再洗涤,然后在真空干燥机内于70℃干燥2h,冷却、密封包装。其中最合理的洗涤试剂__________A.浓盐酸 B.浓氨水 C.无水乙醇 D.水+乙醇真空干燥的原因是___________。(4)随着pH减小,Cu2(OH)4-nCln中铜的质量分数__________A.增大 B.不变 C.减小 D.不能确定
参考答案与解析:
-
相关试题
-
H2SO4溶于水时()。
-
[单选题]H2SO4溶于水时()。A .吸热B .放热C .无变化D .都不对
- 查看答案
-
化工设计概论中有关物料衡算 的题一种废酸,组成为22%HNO3,57%H2SO4和21%H2O,拟加入93%的浓H2SO4和90%的浓HNO3两种浓酸,要求混合成27%HNO3及60%H2SO4的混合
-
化工设计概论中有关物料衡算 的题一种废酸,组成为22%HNO3,57%H2SO4和21%H2O,拟加入93%的浓H2SO4和90%的浓HNO3两种浓酸,要求混合
- 查看答案
-
下列关于浓HNO3和浓H2SO4的叙述中不正确的是()。
-
[单选题]下列关于浓HNO3和浓H2SO4的叙述中不正确的是()。A . 常温下二者都可用铁制容器贮存B . 常温下二者都能与铜较快反应C . 露置于空气中,溶液浓度均降低D . 浓HNO3与浓H2SO4都具有强氧化性
- 查看答案
-
下列关于浓HNO3与浓H2SO4的叙述正确的是()。
-
[单选题]下列关于浓HNO3与浓H2SO4的叙述正确的是()。A .常温下都可用铁制容器贮存B .常温下都能与铜较快反应C .露置于空气中,溶液质量均减轻D .露置于空气中,溶液浓度均降低
- 查看答案
-
常用的酸有:盐酸(HCI)、硫酸(H2SO4)和硝酸(HNO3)等。()
-
[判断题] 常用的酸有:盐酸(HCI)、硫酸(H2SO4)和硝酸(HNO3)等。()A . 正确B . 错误
- 查看答案
-
Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,3Cu+8HNO3(稀
-
[单选题]Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,根据以上两个反应,说明硫酸和硝酸具有()。A .和金属起置换反应的性质;B .还原性;C .强烈的氧化性;D .剧烈的腐蚀性。
- 查看答案
-
在水中不同酸强度顺序为HClO4=H2SO4=HCI=HNO3。
-
[单选题]在水中不同酸强度顺序为HClO4=H2SO4=HCI=HNO3。
- 查看答案
-
制备CuSO4可以采取如图4所示的三种途径。下列说法正确的是( )。①稀H2SO4、稀HNO3-|||-②O2、△-|||-Cu CuSO4-|||-70%H2SO4-|||-③浓H2SO4,△-|
-
制备CuSO4可以采取如图4所示的三种途径。下列说法正确的是( )。①稀H2SO4、稀HNO3-|||-②O2、△-|||-Cu CuSO4-|||-70%H
- 查看答案
-
3.下列说法中正确的有几个 ()-|||-①Cu导电,所以Cu是电解质-|||-②BaSO4难溶于水,所以BaSO4不是电解质-|||-③氨溶于水得到的氨水能导电,所以氨水是电解质-|||-④液态氯化
-
3.下列说法中正确的有几个 ()-|||-①Cu导电,所以Cu是电解质-|||-②BaSO4难溶于水,所以BaSO4不是电解质-|||-③氨溶于水得到的氨水能导
- 查看答案