将298K,p下的1dm3的O2(理想气体)绝热不可逆压缩到5p,消耗功502J,求终态的T2、S2及△H、△G。已知:Sm(O2,298K)= 205.14 J·K-1·mol-1。氧气的物质的量为n=pp/Mn=18q(n(x+1n(x+0)/(由热力学第一定律,△U = Q + W;系统绝热,Q = 0 ,△U = W△U = nCV,m(T2-T1)= 0.4mol ×2.5R×(T2-298K)=502J解得T2 = 896.4Kn=pp/Mn=18q(n(x+1n(x+0)/(n=pp/Mn=18q(n(x+1n(x+0)/(△S2 = △S + S1= 7.4 J×K-1+205.14J×K-1×mol-1×0.40mol = 89.46 J×K-1△H = nCp,m(T2-T1)= 0.4mol×3.5R×(698.4-298)K = 6965.1J△G =△H -△(TS)= △H -(T2S2-T1S1)=6965.1J-(896.4K·89.46 J·K-1-298K×0.4mol·05.14J·K-1·mol-1)=-48.77kJ2.1 mol单原子理想气体温度为273 K,压强为,试计算经下列变化后的。设在此条件下气体的摩尔熵为100 J·mol·K。(1)在恒压下体积增加1倍;(2)在恒容下压强增加1倍;(3)在恒温下压强增加1倍。(答案:① -29.49 kJ·mol-1,② -26.34 kJ·mol-1,③ 1.573 kJ·mol)
将298K,p下的1dm3的O2(理想气体)绝热不可逆压缩到5p,消耗功502J,求终态的T2、S2及△H、△G。已知:Sm(O2,298K)= 205.14 J·K-1·mol-1。
氧气的物质的量为
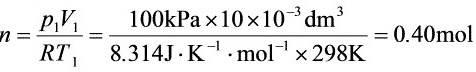
由热力学第一定律,△U = Q + W;系统绝热,Q = 0 ,△U = W
△U = nCV,m(T2-T1)= 0.4mol ×2.5R×(T2-298K)=502J
解得T2 = 896.4K
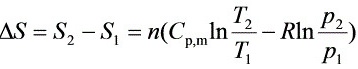
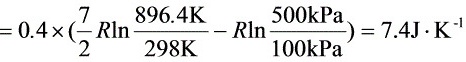
△S2 = △S + S1
= 7.4 J×K-1+205.14J×K-1×mol-1×0.40mol = 89.46 J×K-1
△H = nCp,m(T2-T1)= 0.4mol×3.5R×(698.4-298)K = 6965.1J
△G =△H -△(TS)= △H -(T2S2-T1S1)
=6965.1J-(896.4K·89.46 J·K-1-298K×0.4mol·05.14J·K-1·mol-1)
=-48.77kJ
2.1 mol单原子理想气体温度为273 K,压强为,试计算经下列变化后的。设在此条件下气体的摩尔熵为100 J·mol·K。(1)在恒压下体积增加1倍;(2)在恒容下压强增加1倍;(3)在恒温下压强增加1倍。
(答案:① -29.49 kJ·mol-1,② -26.34 kJ·mol-1,③ 1.573 kJ·mol)
参考答案与解析:
-
相关试题
-
计算下列过程的ΔH、ΔS、ΔG。298K,101。325kPa H2O(l)→473K,405.3kPa H2O(g)已知:Smø(298K,H2O,l)=188.7 J·K-1,水的比热为4.18
-
计算下列过程的ΔH、ΔS、ΔG。298K,101。325kPa H2O(l)→473K,405.3kPa H2O(g)已知:Smø(298K,H2O,l)=18
- 查看答案
-
下列电池:Pt,H2(p?)|H2SO4(aq)|O2(p?),Pt298K时E=1.228V,已知液体水的生成热ΔfHm? (298K,H2O,l) = -2.851×105J·mol-1。(1)
-
下列电池:Pt,H2(p?)|H2SO4(aq)|O2(p?),Pt298K时E=1.228V,已知液体水的生成热ΔfHm? (298K,H2O,l) = -2
- 查看答案
-
已知298K时,有Zn(s)+O2(g)=ZnO(s),ΔrHmθ═-351.5
-
[单选题]已知298K时,有Zn(s)+O2(g)=ZnO(s),ΔrHmθ═-351.5kJ•mol-1,Hg(l)+O2(g)=HgO(s),ΔrHmθ═-90.8kJ•mol-1,则反应Zn(s)+HgO(s)=Hg(l)+ZnO(s)的ΔrHmθ为()。A . 442.3kJ•mol-1B . 260.7kJ•mol-1C . –442.3kJ•mol-1D . -260.7kJ•mol-1
- 查看答案
-
将 1 mol 双原子理想气体从始态 298 K、100 kPa,绝热可逆压缩到体积为 5 dm3,试求终态的温度、压力和过程的 Q、W、ΔU、ΔH 和 ΔS。
-
将 1 mol 双原子理想气体从始态 298 K、100 kPa,绝热可逆压缩到体积为 5 dm3,试求终态的温度、压力和过程的 Q、W、ΔU、ΔH 和 ΔS。
- 查看答案
-
在298K,100kPa下,反应2H2(g)+O2(g)→2H2O(l)的ΔrHmΘ=-572kJ·mol-1,则H2O(l)的ΔfHmΘ是( )。
-
[单选题]在298K,100kPa下,反应2H2(g)+O2(g)→2H2O(l)的ΔrHmΘ=-572kJ·mol-1,则H2O(l)的ΔfHmΘ是( )。
- 查看答案
-
3-13 将1mol,298K的O2 (g)放在一敞口容器中,由容器外13.96 K的液态H2作冷却剂,使体系冷-|||-却为90.19K的O2(1)。已知O2在90.19K时的摩尔汽化热为 .820
-
3-13 将1mol,298K的O2 (g)放在一敞口容器中,由容器外13.96 K的液态H2作冷却剂,使体系冷-|||-却为90.19K的O2(1)。已知O2
- 查看答案
-
[例6.6]已知N2(g)+3H2(g )=2NH3(g) △H^θ=-91.8kJ·mol^(-1),298K时-|||-_({P)_(1)}(298K)=5.8times (10)^5 。求合成氨
-
[例6.6]已知N2(g)+3H2(g )=2NH3(g) △H^θ=-91.8kJ·mol^(-1),298K时-|||-_({P)_(1)}(298K)=5
- 查看答案
-
双原子理想气体在298 K 100 kPa始态时的_(m)=125Jcdot (K)^-1cdot (mol)^-1,现有1 mol该理想气体由始态绝热可逆压缩到压力为150 kPa的终态。试求过程的
-
双原子理想气体在298 K 100 kPa始态时的_(m)=125Jcdot (K)^-1cdot (mol)^-1,现有1 mol该理想气体由始态绝热可逆压缩
- 查看答案
-
在298K时,H2(g)+O2(g)=H2O(L),△H=-285.8kJ/mo
-
[单选题]在298K时,H2(g)+O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()A . 正反应速率增大,逆反应速率减小B . 正反应速率增大,逆反应速率增大C . 正反应速率减小,逆反应速率增大D . 正反应速率减小,逆反应速率减小
- 查看答案
-
若298K时,反应N₂O₄(g)= 2 NO₂(g)的△_x G_m^ theta = 5398 J cdot mol^-1,则当p(N₂O₄)= p(NO₂)= 1 kPa时,反应将()。
-
若298K时,反应N₂O₄(g)= 2 NO₂(g)的△_x G_m^ theta = 5398 J cdot mol^-1,则当p(N₂O₄)= p(NO
- 查看答案