氟及其化合物用途非常广泛,自然界中氟多以化合态形式存在,主要有萤石(CaF2)、冰晶石(Na3AlF6)等。回答下列问题:(1)基态氟原子中有 ____ 种能量不同的电子。(2)NF3是微电子工业中优良的等离子刻蚀气体。NF3与NH3的空间构型相同,但是NH3(-33℃)的沸点比NF3(-129℃)的高,原因为 ____ 。(3)氟硼酸(HBF4属于强酸)常用于替代浓硫酸作铅蓄电池的电解质溶液,可由HF和BF3合成,从化学键形成角度分析HF与BF3能化合的原因: ____ 。(4)液态[H2F]+中存在[H2F]+和[HF2)]-,[HF2]-的结构可表示为[P-H…F]-,[H2F]+的VSEPR模型名称为 ____ 形。NaHF2可用于制无水氟化氢和供雕刻玻璃、木材防腐等。常温常压下为白色固体,易溶于水,160℃分解。NaHF2中所含作用力的类型有 ____ (填字母)。a.离子键 b.共价键 c.配位键 d.氢键(5)CaF2是难溶化合物,其晶胞结构如图所示:C-|||-点 D-|||-C 。-|||-a f-|||-ò。 Ca^2-|||-A-|||-B-|||--|||--|||-0 x①若原子坐标参数A处为(0,0,0),B处为((1)/(2),(1)/(2),0),C处为(1.1,1),则D处为 ____ 。②每个Ca2+周围距离最近的Ca2+共有 ____ 个。③已知:CaF2晶体密度为c g•cm3则晶胞中Ca2+与最近的F之间的距离为 ____ nm (设NA表示阿伏加德罗常数的值,用含c、NA的式子表示)。
氟及其化合物用途非常广泛,自然界中氟多以化合态形式存在,主要有萤石(CaF2)、冰晶石(Na3AlF6)等。回答下列问题:(1)基态氟原子中有 ____ 种能量不同的电子。
(2)NF3是微电子工业中优良的等离子刻蚀气体。NF3与NH3的空间构型相同,但是NH3(-33℃)的沸点比NF3(-129℃)的高,原因为 ____ 。
(3)氟硼酸(HBF4属于强酸)常用于替代浓硫酸作铅蓄电池的电解质溶液,可由HF和BF3合成,从化学键形成角度分析HF与BF3能化合的原因: ____ 。
(4)液态[H2F]+中存在[H2F]+和[HF2)]-,[HF2]-的结构可表示为[P-H…F]-,[H2F]+的VSEPR模型名称为 ____ 形。NaHF2可用于制无水氟化氢和供雕刻玻璃、木材防腐等。常温常压下为白色固体,易溶于水,160℃分解。NaHF2中所含作用力的类型有 ____ (填字母)。
a.离子键 b.共价键 c.配位键 d.氢键
(5)CaF2是难溶化合物,其晶胞结构如图所示:
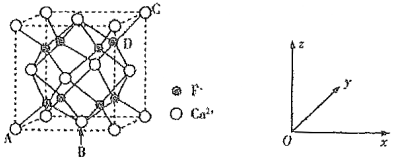
①若原子坐标参数A处为(0,0,0),B处为($\frac{1}{2}$,$\frac{1}{2}$,0),C处为(1.1,1),则D处为 ____ 。
②每个Ca2+周围距离最近的Ca2+共有 ____ 个。
③已知:CaF2晶体密度为c g•cm3则晶胞中Ca2+与最近的F之间的距离为 ____ nm (设NA表示阿伏加德罗常数的值,用含c、NA的式子表示)。
参考答案与解析:
-
相关试题
-
氟在自然界中最重要的化合物为萤石或氟石,其主要成分是()。
-
氟在自然界中最重要的化合物为萤石或氟石,其主要成分是()。A. Ca₅[PO₄]₂FB. CaF₂C. NaF·AlF₃D. Ca₅[PO₄]₃F
- 查看答案
-
自然界中化合态氮的主要来源有()
-
[单选题]自然界中化合态氮的主要来源有()A .大气及岩浆固氮B .工业固氮C .生物固氮D .以上三种说法都对
- 查看答案
-
氟以化合物或络合物的形式广泛存在于各种食物中氟中毒的临床表现为().
-
[单选题]氟以化合物或络合物的形式广泛存在于各种食物中氟中毒的临床表现为().A .消化不良B .皮疹C .头痛D .斑牙
- 查看答案
-
铝电解厂烟气净化的一种简单流程如图:过量Na2 CO3 NaAlO2-|||-烟气 __ 吸收塔 合成槽-|||-冰晶石-|||-含HF) 过滤 (Na3AlF6)-|||-滤液下列说法错误的是(
-
铝电解厂烟气净化的一种简单流程如图:过量Na2 CO3 NaAlO2-|||-烟气 __ 吸收塔 合成槽-|||-冰晶石-|||-含HF) 过滤 (Na3AlF
- 查看答案
-
黄酮类化合物在自然界多以游离形式存在,少数以苷的形式存在。
-
[判断题] 黄酮类化合物在自然界多以游离形式存在,少数以苷的形式存在。A . 正确B . 错误
- 查看答案
-
自然界中的铜主要有3种存在形式,其中最多的是()
-
自然界中的铜主要有3种存在形式,其中最多的是()A. 氧化矿B. 硫化矿C. 胆矾D. 自然铜
- 查看答案
-
冰晶石的摩尔比是冰晶石中AIF3的摩尔数与冰晶石中NaF的摩尔数之比。
-
[判断题] 冰晶石的摩尔比是冰晶石中AIF3的摩尔数与冰晶石中NaF的摩尔数之比。A . 正确B . 错误
- 查看答案
-
判断下列叙述是否正确,并说明理由。(1)自然界的物质都是以化合物形式存在的。(2
-
[主观题]判断下列叙述是否正确,并说明理由。(1)自然界的物质都是以化合物形式存在的。(2)水是有氢元素和氧元素组成的化合物。(3)冰块与水混合得到混合物。(4)电解水的反应属于分解反应。(5)凡是含氧元素的物质都是氧化物。
- 查看答案
-
温室气体主要有二氧化碳、甲烷、氮氧化合物、氟氯烃、臭氧等。
-
[判断题] 温室气体主要有二氧化碳、甲烷、氮氧化合物、氟氯烃、臭氧等。A . 正确B . 错误
- 查看答案