合成气(CO和H2)是重要的工业原料气。(1)合成气制备甲醇:CO(g)+2H2(g)=CH3OH(g)。CO的结构式为C≡O,估算该反应的ΔH需要 ____ (填数字)种化学键的键能数据。(2)合成气经“变换”“脱碳”获得纯H2。①合成气变换。向绝热反应器中通入CO、H2和过量的H2O(g):CO(g)+(H)_(2)O(g)underline(underline{低温型催化剂)} 约23(0)°C、3MPa H2 50 4-|||-个 个 40 a o {2-|||-三1三-|||-30-|||-20 l-|||-载氧体 载氧体 50 0-|||-一40 B-|||-反应器 z-|||-个 载氧体循环 20-|||-CH4 H2O 0 0.3 0.4 0.5 1.0-|||-步骤I 步骤Ⅱ x-|||-甲 乙③结合图示综合分析,步骤Ⅰ中Fe2O3的作用、气体分步制备的价值: ____ 。
合成气(CO和H2)是重要的工业原料气。(1)合成气制备甲醇:CO(g)+2H2(g)=CH3OH(g)。CO的结构式为C≡O,估算该反应的ΔH需要 ____ (填数字)种化学键的键能数据。
(2)合成气经“变换”“脱碳”获得纯H2。
①合成气变换。向绝热反应器中通入CO、H2和过量的H2O(g):$CO(g)+{H}_{2}O(g)\begin{array}{c}\underline{\underline{低温型催化剂}}\\ 约23{0}°C、3MPa\end{array}C{O}_{2}(g)+{H}_{2}(g)\;\;ΔH<0$。催化作用受接触面积和温度等因素影响,H2O(g)的比热容较大。H2O(g)过量能有效防止催化剂活性下降,其原因有 ____ 。
②脱碳在钢制吸收塔中进行,吸收液成分:质量分数30%的K2CO3吸收剂、K2CrO4(Cr正价有+3、+6)缓蚀剂等。K2CO3溶液浓度偏高会堵塞设备,导致堵塞的物质是 ____ (填化学式)。K2CrO4减缓设备腐蚀的原理是 ____ 。
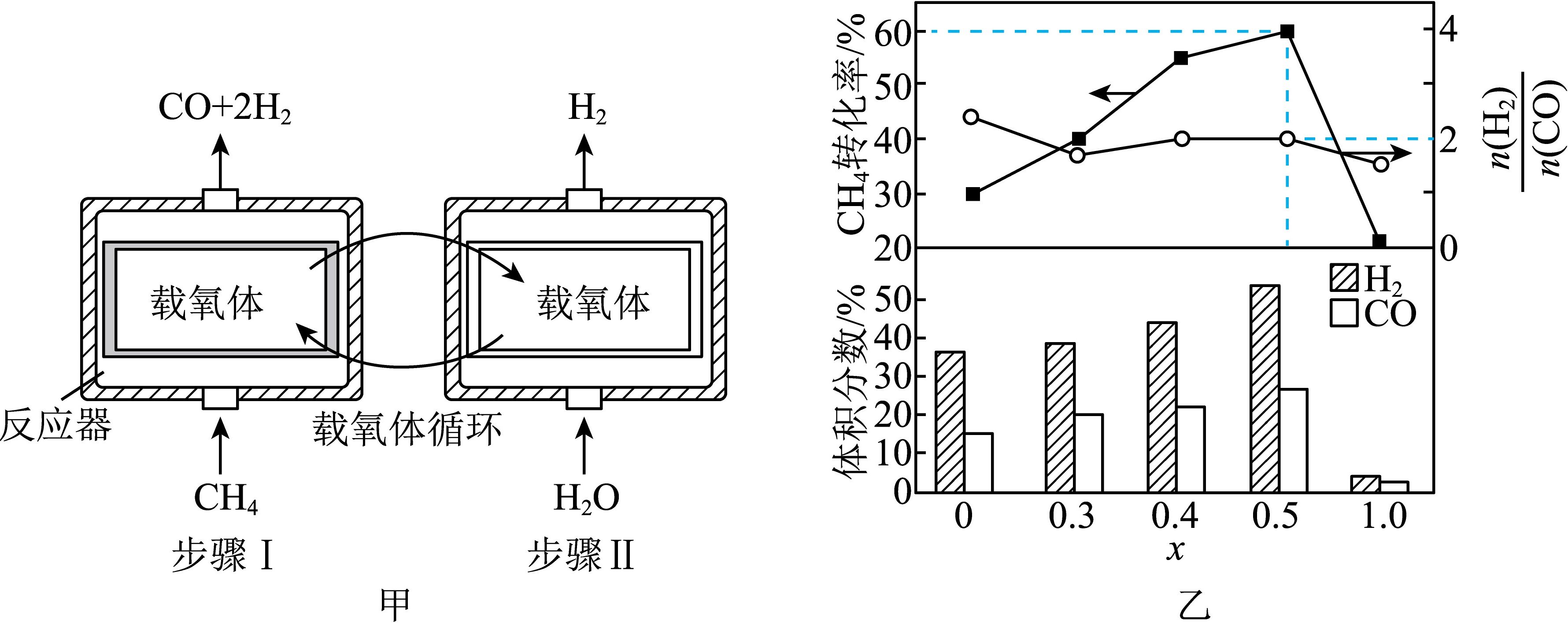
(3)研究CH4、H2O(g)与不同配比的铁铈载氧体[$\frac{x}{2}F{e}_{2}{O}_{3}•(1-x)Ce{O}_{2},0≤x≤1,Ce$是活泼金属,正价有+3、+4]反应,气体分步制备原理示意如图甲所示。相同条件下,先后以一定流速通入固定体积的CH4、H2O(g),依次发生的主要反应:
步骤Ⅰ$C{H}_{4}→_{850℃}^{载氧体供氧}CO+2{H}_{2}$
步骤Ⅱ${H}_{2}O→_{400℃}^{载氧体夺氧}{H}_{2}$
①步骤Ⅰ中,产物气体积分数、CH4转化率、$\frac{n({H}_{2})}{n(CO)}$与x的关系如图乙所示。x=0时,$\frac{n({H}_{2})}{n(CO)}$大于理论值2的可能原因有 ____ ;x=0.5时,通入标准状况下300mL的CH4至反应结束,CO的选择性=$\frac{{n}_{生成}(CO)}{{n}_{转化}(C{H}_{4})}×100%=80%$,则生成标准状况下CO和H2的总体积为 ____ mL。
②x=0.5时,新制载氧体、与CH4反应后的载氧体的X射线衍射谱图如图丙所示(X射线衍射用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。步骤Ⅱ中,能与H2O(g)反应的物质有 ____ (填化学式)。
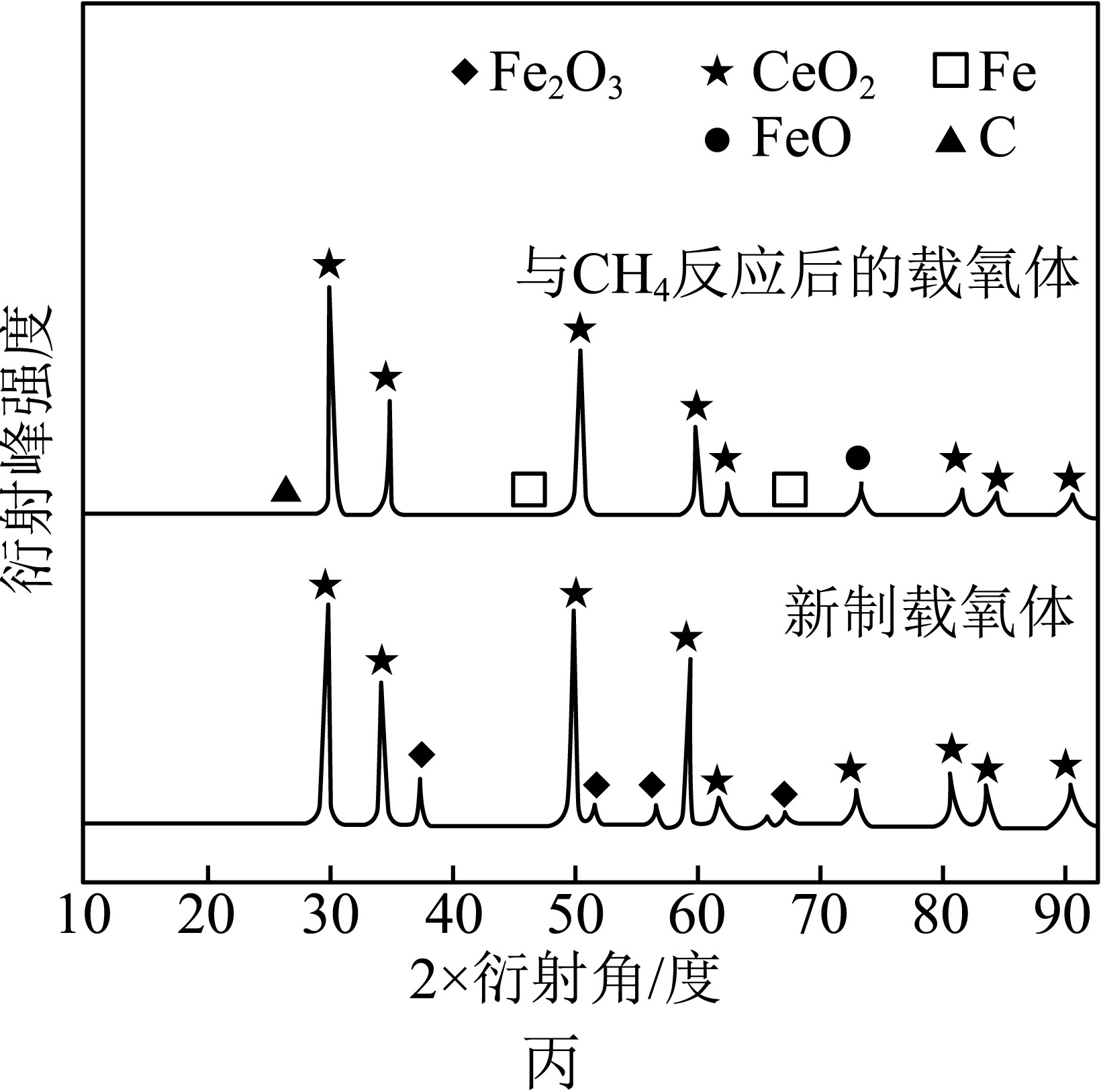
③结合图示综合分析,步骤Ⅰ中Fe2O3的作用、气体分步制备的价值: ____ 。
参考答案与解析:
-
相关试题
-
甲醇合成气中,CO:22.24%、CO2:5.86%、H264.87%,合成气的
-
[填空题] 甲醇合成气中,CO:22.24%、CO2:5.86%、H264.87%,合成气的氢碳比是()。
- 查看答案
-
计算题:设合成气组成中H2为68%;CO为27%;CO2为3%;则合成气的氢碳比
-
[问答题] 计算题:设合成气组成中H2为68%;CO为27%;CO2为3%;则合成气的氢碳比是多少?
- 查看答案
-
计算298 K下,CO(g)和CH3OH(g)的标准生成焓,并计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变。已知如下燃烧焓数据:ΔcH(298 K)(CH3OH(g))=-763.9
-
计算298 K下,CO(g)和CH3OH(g)的标准生成焓,并计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变。已知如下燃烧焓数据:ΔcH(298
- 查看答案
-
在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)△H已知:①CO(g)+2H2(g)⇌CH3OH(g)△H1=-90.7kJ•
-
在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)△H已知:①CO(g)+2H2(g)⇌
- 查看答案
-
原料气H2/CO对费托合成反应有何影响?
-
[问答题] 原料气H2/CO对费托合成反应有何影响?
- 查看答案
-
水煤气发生炉中共有C(s),H2O(g),CO(g), CO2(g)及H2(g)五种物质,它们之能发生下述反应:CO2(g)+ C(s) = 2CO(g) CO2(g) + H2(g) = CO(
-
水煤气发生炉中共有C(s),H2O(g),CO(g), CO2(g)及H2(g)五种物质,它们之能发生下述反应:CO2(g)+ C(s) = 2CO(g)
- 查看答案
-
甲醇合成反应原料气中的理论化学计量比为ν(H2):ν(CO)=2:1,实际生产中氢气的用量为( )
-
甲醇合成反应原料气中的理论化学计量比为ν(H2):ν(CO)=2:1,实际生产中氢气的用量为( )A. 小于化学计量比B. 大于化学计量比C. 等于化学计量比D
- 查看答案
-
为了提高CO在CO(g)+H2O(g) CO2(g)+H2(g)反应中的平衡转化率,可以…………………( )
-
为了提高CO在CO(g)+H2O(g) CO2(g)+H2(g)反应中的平衡转化率,可以…………………( )A. 增加CO的浓度(或分压)B. 增
- 查看答案
-
在823K,标准态下下列反应的θY:(1)CO2(g)+H2(g)=CO(g)+H2O(g) θY(2)CoO(s)+H2(g)=Co(s)+H2O(g) θY试求823K,标准态下反应(3)
-
在823K,标准态下下列反应的θY:(1)CO2(g)+H2(g)=CO(g)+H2O(g) θY(2)CoO(s)+H2(g)=Co(s)+H2O(g)
- 查看答案
-
在CO(气)+H2O(气)CO2(气)+H2(气)-Q的平衡中,能同等程度的增加
-
[单选题]在CO(气)+H2O(气)CO2(气)+H2(气)-Q的平衡中,能同等程度的增加正、逆反应速度的是()。A .加催化剂;B .增加CO2的浓度;C .减少CO的浓度;D .升高温度。
- 查看答案