总压为101.325kPa、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH的平衡分压为2.266kPa。试求此时之溶解度系数H、亨利系数E、相平衡常数m。解:首先将此气液相组成换算为y与x。NH的摩尔质量为17kg/kmol,溶液的量为15kg NH与1000kg水之和。故=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156E=P·m=101.325×1.436=145.5kPa或 kPa溶剂水的密度ρ=1000kg/m,摩尔质量M=18kg/kmolkmol/(ms·kPa)或:kmol/m所以 =dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156kmol/(m3·kPa)本题要求掌握亨利定律及亨利系数(E、H、m)之间的互相关系。6-2.已知常压、25℃下某体系的平衡关系符合亨利定律,亨利系数E为 大气压,溶质A的分压为0.54大气压的混合气体分别与三种溶液接触:①溶质A浓度为 的水溶液;②溶质A浓度为 的水溶液;③溶质A浓度为 的水溶液。试求1)上述三种情况下溶质A在二相间的转移方向。2)若吸收压力提高至3atm,再计算③的传质方向。解: 1) E=0.15×104atm,p=0.054atm,P=1atm,y=p/P=0.054① =dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156∴=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156 ∴ ∴平衡② =dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156∴=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156 ∴ ∴气相转移至液相③ =dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156∴=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156 ∴ ∴液相转移至气相2) P=3atm y=0.054 E=0.15×10atm∴m=E/P=0.05×104x4=x=5.4×10∴ ∴ ∴气相转移至液相说明:利用吸收相平衡关系可判断传质过程进行的方向;计算传质过程的推动力和吸收过程可达到的极限。低温高压有利于吸收。6-3. 在常压逆流吸收塔中,用纯吸收剂吸收混合气中的溶质组分.进塔气体中溶质组分为4.5%(体积),吸收率为90%;出塔液相组成为0.02(摩尔分数),操作条件下平衡关系为Y*=1.5X。求:1)塔顶气相传质推动力;2) 塔底气传质推动力;3) 全塔平均推动力。解:1)y=0.045=4.5%出塔气相组成Y=Y(1-φ)=0.047×(1-0.90)=0.0047进塔液相组成x2=0. m=1.5塔顶气相推动力:ΔY2=Y-Y*=Y-mX=0.047-0=0.00472)出塔液相组成: 塔底气相推动力:ΔY=Y-Y*=Y-mX=0.047-1.5×0.0204=0.01643)全塔气相平均推动力ΔY11本题要求掌握吸收过程传质推动力的计算。6-4.某传质过程的总压为300 ,吸收过程传质系数分别为 、 ,气液相平衡关系符合亨利定律,亨利系数E为 ,试求:1)吸收过程传质总系数 和 ;2)液相中的传质阻力为气相的多少倍。解:1)E = 10.67×103kPa,P = 300kPa,=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156 ∴Ky = 0.3919=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156 ∴K= 13.942) =dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156本题目要求掌握吸收传质系数的计算及相互关系。6-5.在常压逆流操作的填料吸收,用清水吸收空气-氨混合气体中的氨.混合气的质量流速为580Kg/(m·h).溶质组成为6%(体积),吸收率为99%,水的质量流速为770Kg/(m2·h).操作条件下平衡关系为Y*=0.9X.若填料层高度为4m。求:1)气相总传质单元数N2;2)气相总传质单元高度HOG解:1)清水吸收x=0Y=Y(1-φ)=0.0638×(1-0.99)=0.000638混合气的平均摩尔质量:Mm=My+My=29×(1-0.06)+17×0.06=28.28Kg/Kmol惰气的摩尔流速清水的摩尔流速为:=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156m本题是吸收过程的基本计算,要求能熟练掌握传质单元数和传质单元高度的计算。6-6.在一逆流操作的填料塔中,用循环溶剂吸收气体混合物中溶质。气体入塔组成为0.025(摩尔比,下同),液气比为1.6,操作条件下气液平衡关系为Y=1.2X。若循环溶剂组成为0.001,则出塔气体组成为0.0025,现因脱吸不良,循环溶剂组成变为0.01,试求此时出塔气体组成。解:两种工况下,仅吸收剂初始组成不同,但因填料层高度一定,H不变,故N也相同。由原工况下求得N后,即可求算出新工况下出塔气体组成。原工况(即脱吸塔正常操作)下:吸收液出口组成由物料衡算求得:吸收过程平均推动力和N为:ΔYOG=Y-mX=0.025-1.2×0.0151=0.00688ΔY1=Y1-mX1=0.0025-1.2×0.001=0.0013=dfrac ({n)_(A)}(n)=dfrac ({n)_(A)}({n)_(A)+(n)_(n)}=dfrac (15/17)(15/17+1000/18)=0.0156新工况(即脱吸塔不正常)下;设此时出塔气相组成为Y′,出塔液相组成为X′,入塔液相组成为X′,则吸收塔物料衡算可得:
第六单元 吸 收
6-1. 总压为101.325kPa、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH的平衡分压为2.266kPa。试求此时之溶解度系数H、亨利系数E、相平衡常数m。
解:首先将此气液相组成换算为y与x。
NH的摩尔质量为17kg/kmol,溶液的量为15kg NH与1000kg水之和。故
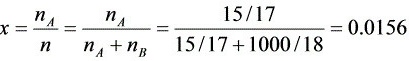
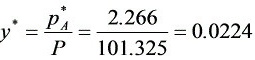
E=P·m=101.325×1.436=145.5kPa
或 kPa
溶剂水的密度ρ=1000kg/m,摩尔质量M=18kg/kmol
kmol/(ms·kPa)
或:
kmol/m
所以 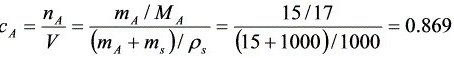 kmol/(m3·kPa)
kmol/(m3·kPa)
本题要求掌握亨利定律及亨利系数(E、H、m)之间的互相关系。
6-2.已知常压、25℃下某体系的平衡关系符合亨利定律,亨利系数E为 大气压,溶质A的分压为0.54大气压的混合气体分别与三种溶液接触:①溶质A浓度为 的水溶液;②溶质A浓度为 的水溶液;③溶质A浓度为 的水溶液。试求1)上述三种情况下溶质A在二相间的转移方向。2)若吸收压力提高至3atm,再计算③的传质方向。
解: 1) E=0.15×104atm,p=0.054atm,P=1atm,y=p/P=0.054
①
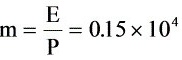
∴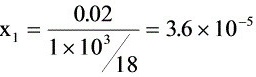 ∴ ∴平衡
∴ ∴平衡
② 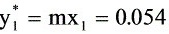
∴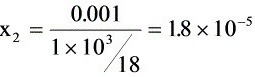 ∴ ∴气相转移至液相
∴ ∴气相转移至液相
③ 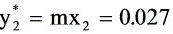
∴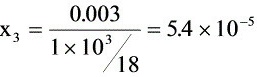 ∴ ∴液相转移至气相
∴ ∴液相转移至气相
2) P=3atm y=0.054 E=0.15×10atm
∴m=E/P=0.05×104
x4=x=5.4×10
∴ ∴ ∴气相转移至液相
说明:利用吸收相平衡关系可判断传质过程进行的方向;计算传质过程的推动力和吸收过程可达到的极限。低温高压有利于吸收。
6-3. 在常压逆流吸收塔中,用纯吸收剂吸收混合气中的溶质组分.进塔气体中溶质组分为4.5%(体积),吸收率为90%;出塔液相组成为0.02(摩尔分数),操作条件下平衡关系为Y*=1.5X。求:
1)塔顶气相传质推动力;
2) 塔底气传质推动力;
3) 全塔平均推动力。
解:
1)y=0.045=4.5%
出塔气相组成Y=Y(1-φ)=0.047×(1-0.90)=0.0047
进塔液相组成x2=0. m=1.5
塔顶气相推动力:ΔY2=Y-Y*=Y-mX=0.047-0=0.0047
2)出塔液相组成:
塔底气相推动力:ΔY=Y-Y*=Y-mX=0.047-1.5×0.0204=0.0164
3)全塔气相平均推动力ΔY11
本题要求掌握吸收过程传质推动力的计算。
6-4.某传质过程的总压为300 ,吸收过程传质系数分别为 、 ,气液相平衡关系符合亨利定律,亨利系数E为 ,试求:1)吸收过程传质总系数 和 ;2)液相中的传质阻力为气相的多少倍。
解:1)E = 10.67×103kPa,P = 300kPa,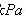
 ∴Ky = 0.3919
∴Ky = 0.3919
 ∴K= 13.94
∴K= 13.94
2) 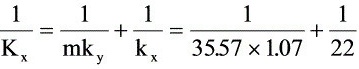
本题目要求掌握吸收传质系数的计算及相互关系。
6-5.在常压逆流操作的填料吸收,用清水吸收空气-氨混合气体中的氨.混合气的质量流速为580Kg/(m·h).溶质组成为6%(体积),吸收率为99%,水的质量流速为770Kg/(m2·h).操作条件下平衡关系为Y*=0.9X.若填料层高度为4m。求:
1)气相总传质单元数N2;
2)气相总传质单元高度HOG
解:
1)清水吸收x=0
Y=Y(1-φ)=0.0638×(1-0.99)=0.000638
混合气的平均摩尔质量:
Mm=My+My=29×(1-0.06)+17×0.06=28.28Kg/Kmol
惰气的摩尔流速
清水的摩尔流速为: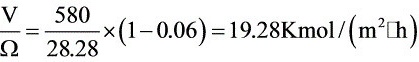

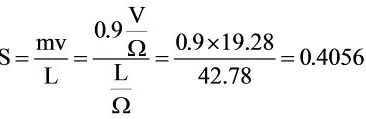 m
m
本题是吸收过程的基本计算,要求能熟练掌握传质单元数和传质单元高度的计算。
6-6.在一逆流操作的填料塔中,用循环溶剂吸收气体混合物中溶质。气体入塔组成为0.025(摩尔比,下同),液气比为1.6,操作条件下气液平衡关系为Y=1.2X。若循环溶剂组成为0.001,则出塔气体组成为0.0025,现因脱吸不良,循环溶剂组成变为0.01,试求此时出塔气体组成。
解:两种工况下,仅吸收剂初始组成不同,但因填料层高度一定,H不变,故N也相同。由原工况下求得N后,即可求算出新工况下出塔气体组成。
原工况(即脱吸塔正常操作)下:
吸收液出口组成由物料衡算求得:
吸收过程平均推动力和N为:
ΔYOG=Y-mX=0.025-1.2×0.0151=0.00688
ΔY1=Y1-mX1=0.0025-1.2×0.001=0.0013
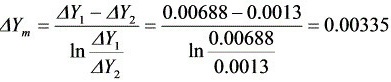
新工况(即脱吸塔不正常)下;
设此时出塔气相组成为Y′,出塔液相组成为X′,入塔液相组成为X′,则吸收塔物料衡算可得:
参考答案与解析:
-
相关试题
-
总压为101.32.kPa、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH的平衡分压为2.266kPa。试求此时之溶解度系数H、亨利系数E、相平衡常数m。解:首先将此气液相
-
总压为101.32.kPa、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH的平衡分压为2.266kPa。试求此时之溶解度系数H、亨利
- 查看答案
-
总压为101.32.kPa、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH平衡分压为2.266kPa。试求此时之溶解度系数H、亨利系数E、相平衡常数m。解:一方面将此气液相
-
总压为101.32.kPa、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH平衡分压为2.266kPa。试求此时之溶解度系数H、亨利系
- 查看答案
-
总压为、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH的平衡分压为。试求此时之溶解度系数H、亨利系数E、相平衡常数m。解:首先将此气液相组成换算为y与x。NH的摩尔质量为1
-
总压为、温度为20℃时,1000kg水中溶解15kg NH,此时溶液上方气相中NH的平衡分压为。试求此时之溶解度系数H、亨利系数E、相平衡常数m。解:首先将此气
- 查看答案
-
1.在总压为101.3kPa、温度为30℃的条件下,已知1000kg水中溶解有200kg氨气。-|||-若溶液上方气相中氨气的平衡分压为35kPa,试计算此时的相平衡常数m、亨利系数E和溶-|||-解
-
1.在总压为101.3kPa、温度为30℃的条件下,已知1000kg水中溶解有200kg氨气。-|||-若溶液上方气相中氨气的平衡分压为35kPa,试计算此时的
- 查看答案
-
4.100g水中溶解1 gNH3,查得20℃时溶液上方NH3的平衡分压为798Pa。此稀溶液的气液相平衡-|||-关系服从亨利定律,试求亨利系数E(单位为kPa)、溶解度系数H[单位为 ((m)^3c
-
4.100g水中溶解1 gNH3,查得20℃时溶液上方NH3的平衡分压为798Pa。此稀溶液的气液相平衡-|||-关系服从亨利定律,试求亨利系数E(单位为kPa
- 查看答案
-
对于气膜控制,气体的溶解度系数H( ),相平衡常数m( ),亨利系数E()
-
对于气膜控制,气体的溶解度系数H( ),相平衡常数m( ),亨利系数E()A. 很大,很大,很大B. 很大,很小,很小C. 很小,很小,很小D. 很小,很大,很
- 查看答案
-
对接近常压的低溶质浓度的气液平衡系统,当总压增大时,亨利系数E(),相平衡常数m
-
[填空题] 对接近常压的低溶质浓度的气液平衡系统,当总压增大时,亨利系数E(),相平衡常数m(),溶解度系数H()。
- 查看答案
-
对常压操作的低浓度吸收系统,当系统温度升高时,亨利系数 E 将( A ), 平衡常数 m 将( A ),溶解度系数 H 将( )
-
对常压操作的低浓度吸收系统,当系统温度升高时,亨利系数 E 将( A ), 平衡常数 m 将( A ),溶解度系数 H 将( )A. 增加B. 降低C. 不变D
- 查看答案
-
(4)在25℃及总压为101.33kPa的条件下,氨水溶液的相平衡关系为 _(c)=93.90xkPa 试求:(1)100g-|||-水中溶解1g的氨时溶液上方氨气的平衡分压和溶解度系数H;(2)相平
-
(4)在25℃及总压为101.33kPa的条件下,氨水溶液的相平衡关系为 _(c)=93.90xkPa 试求:(1)100g-|||-水中溶解1g的氨时溶液上方
- 查看答案
-
-1已知在101.3 kPa(绝对压力下),100 g水中含氨1 g的溶液上方的平衡氨气分压为987 Pa。试求:(1) 溶解度系数H (kmol·m-3·Pa-1);(2) 亨利系数E(Pa);(3
-
-1已知在101.3 kPa(绝对压力下),100 g水中含氨1 g的溶液上方的平衡氨气分压为987 Pa。试求:(1) 溶解度系数H (kmol·m-3·Pa
- 查看答案