- 充电时作阳极,放电时作正极
- 充电时作阳极,放电时作负极
- 充电时作阴极,放电时作负极
- 充电时作阴极,放电时作正极
回答下列问题:(1)利用(Fe)、(Cu)作电极设计成原电池,可以确定它们活动性的相对强弱.试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出正极反应式.正极反应式:___.(2)为处理银器表面的黑斑((Ag_{2)S)},将银器浸于铝质容器里的食盐水中并与铝接触,(Ag_{2)S}转化为(Ag),食盐水的作用是___.(3)锂电池具有比能量大、电压高、工作温度宽、可储存时间长等优点.锂电池的比能量大的原因是___.(4)有(a)、(b)、(c)、(d)四个金属电极,有关的实验装置及部分实验现象如下:由此判断这四种金属的活动性由强到弱的顺序是___.(5)铅蓄电池是典型的可充电型电池,电池总反应式为:(Pb +PbO_{2) +4H^+ +2SO^2-_(4) }xtofrom[充电](放电)(2PbSO_{4) +2H_(2)O}.①放电时,正极反应式是___;电解液中(H_{2)SO_(4)}的密度将变___;当外电路通过(1)(mol)电子时,理论上负极板的质量增加___(g).②铅蓄电池上有两个接线柱,一个接线柱旁标有"+",另一个接线柱旁标有"-".关于标有"+"的接线柱,下列说法中正确的是( ).A:充电时作阳极,放电时作正极B:充电时作阳极,放电时作负极C:充电时作阴极,放电时作负极D:充电时作阴极,放电时作正极
回答下列问题:
(1)利用${Fe}$、${Cu}$作电极设计成原电池,可以确定它们活动性的相对强弱.试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出正极反应式.
正极反应式:___.
(2)为处理银器表面的黑斑${(Ag_{2}S)}$,将银器浸于铝质容器里的食盐水中并与铝接触,${Ag_{2}S}$转化为${Ag}$,食盐水的作用是___.
(3)锂电池具有比能量大、电压高、工作温度宽、可储存时间长等优点.锂电池的比能量大的原因是___.
(4)有${a}$、${b}$、${c}$、${d}$四个金属电极,有关的实验装置及部分实验现象如下: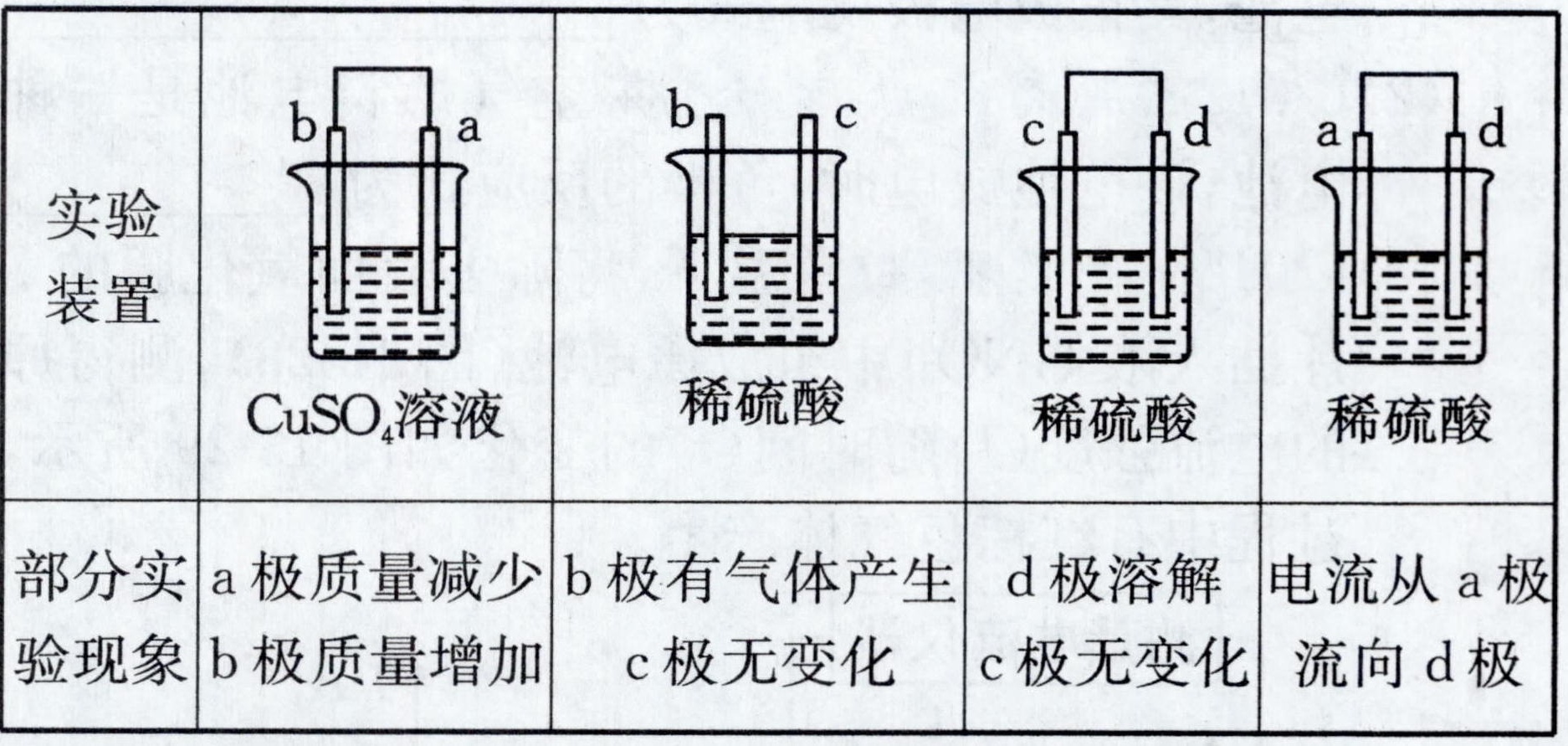
由此判断这四种金属的活动性由强到弱的顺序是___.
(5)铅蓄电池是典型的可充电型电池,电池总反应式为:
${Pb +PbO_{2} +4H^{+} +2SO^{2-}_{4} }\xtofrom[充电]{放电}{2PbSO_{4} +2H_{2}O}$.
①放电时,正极反应式是___;电解液中${H_{2}SO_{4}}$的密度将变___;当外电路通过${1}{mol}$电子时,理论上负极板的质量增加___${g}$.
②铅蓄电池上有两个接线柱,一个接线柱旁标有"$+$",另一个接线柱旁标有"$-$".关于标有"$+$"的接线柱,下列说法中正确的是( ).
参考答案与解析:
-
相关试题
-
8.写出下列原电池的电极反应式和电池反应式,并计算原电池的电动势(298K):-|||-|(Fe)^2+(1.0molcdot (L)^-1) jí ^-(1.0molcdot (L)^-1)/(Cl
-
8.写出下列原电池的电极反应式和电池反应式,并计算原电池的电动势(298K):-|||-|(Fe)^2+(1.0molcdot (L)^-1) jí ^-(1.
- 查看答案
-
有一原电池Ag | AgCl(s) | Cl-(a=1)||Cu2+(a=0、01)| Cu。(1)写出上述原电池的反应式;(2)计算该原电池在25℃时的电动势E;(3)25℃时,原电池反应的 吉布斯
-
有一原电池Ag | AgCl(s) | Cl-(a=1)||Cu2+(a=0、01)| Cu。(1)写出上述原电池的反应式;(2)计算该原电池在25℃时的电动势
- 查看答案
-
在原电池实验中,Cu-Zn原电池的正极是:()
-
在原电池实验中,Cu-Zn原电池的正极是:()A. 无法确定B. ZnC. Cu
- 查看答案
-
原电池的负极发生还原反应,正极发生氧化反应。
-
原电池的负极发生还原反应,正极发生氧化反应。A. 对B. 错
- 查看答案
-
原电池正极的电极电势为正值,负极的电极电势为负值。()
-
原电池正极的电极电势为正值,负极的电极电势为负值。()A. 对B. 错
- 查看答案
-
将下列氧化还原反应设计成原电池,并分别写出电极反应和电池符号。 (1) Sn2++ 2Fe3+= Sn4++ 2Fe2+ (2) Cu2++ H2= Cu+ 2H+
-
将下列氧化还原反应设计成原电池,并分别写出电极反应和电池符号。 (1) Sn2++ 2Fe3+= Sn4++ 2Fe2+ (2) Cu2++ H2= Cu+ 2
- 查看答案
-
在原电池中,正极发生的反应(),负极发生的反应是()。
-
在原电池中,正极发生的反应(),负极发生的反应是()。A. 氧化还原B. 还原氧化C. 还原分解D. 氧化分解E. 分解化合
- 查看答案
-
在原电池中,正极发生的反应(),负极发生的反应是()。
-
在原电池中,正极发生的反应(),负极发生的反应是()。A. 氧化还原B. 还原氧化C. 还原分解D. 氧化分解
- 查看答案
-
在原电池中,正极发生的反应(),负极发生的反应是()。
-
在原电池中,正极发生的反应(),负极发生的反应是()。A. 氧化分解B. 还原氧化C. 还原分解D. 分解合成E. 氧化原还
- 查看答案
-
原电池的碳电极作用().
-
[单选题]原电池的碳电极作用().A . 参与化学反应,并为返回电子提供通路B . 参与化学反应,但不为返回电子提供通路C . 不参与化学反应,并为返回电子提供通路D . 不参与化学反应,不为返回电子提供通路
- 查看答案