FeCl3是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。(1)将标准状况下的aL氯化氢气体溶于100g水中,得到盐酸的密度为bg·mL-1,则该盐酸的物质的量浓度是______________________。(2)向100mL的FeBr2溶液中通入标准状况下Cl23.36L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为__________________。(3)FeCl3溶液可以用来净水,其净水的原理为___________________________(用离子方程式表示)。用100mL2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________(填“大于”“等于”或“小于”)0.2NA。6.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解得到1mol羧酸和2mol乙醇,该羧酸的分子式为A.C16H22O5 B.C14H16O4 C.16H20O4 D.C14H18O57.根据下列性质判断所描述的物质可能属于分子晶体的是( )A.熔点1070℃,易溶于水,水溶液能导电B.熔点1128℃,沸点4446℃,硬度很大C.熔点10.31℃,液态不导电,水溶液能导电D.熔点97.81℃,质软,导电,密度0.97g/cm38.下列说法中不正确的是A.高吸水性树脂属于功能高分子材料B.SiC、Al2O3的熔点很高,可用作高温结构陶瓷C.光导纤维、合成纤维和人造纤维都是有机高分子化合物D.合金拓展了金属材料的使用范围,合金中也可能含有非金属元素9.下列物质中,水解前后均可发生银镜反应的是A.蔗糖 B.麦芽糖 C.淀粉 D.乙酸甲酯10.共价键、离子键和范德华力都是微粒间的作用力,下列物质:①Na2O2;②SiO2;③石墨;④金刚石;⑤CaH2;⑥白磷,其中含有两种结合力的组合是A.①③⑤⑥B.①③⑥C.②④⑥D.①②③⑥11.向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:↑n(CO2) ↑n(CO2) ↑m( ) ↑m (CO2)-|||-n (HCl) n (HCl) n (HCl) n (HCl)-|||-0 → OL → 0 IV-|||-I II III则下列分析都正确的组合是 ( )溶质的成分对应图象溶液中离子浓度关系ANaHCO3、Na2CO3Ⅱc(CO32-)c(CO32-)CNa2CO3Ⅳc(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)DNaHCO3Ic(Na+)=c(HCO3-)
(8分)FeCl3是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的aL氯化氢气体溶于100g水中,得到盐酸的密度为bg·mL-1,则该盐酸的物质的量浓度是______________________。
(2)向100mL的FeBr2溶液中通入标准状况下Cl23.36L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为__________________。
(3)FeCl3溶液可以用来净水,其净水的原理为___________________________(用离子方程式表示)。用100mL2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________(填“大于”“等于”或“小于”)0.2NA。
6.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解得到1mol羧酸和2mol乙醇,该羧酸的分子式为
A.C16H22O5 B.C14H16O4 C.16H20O4 D.C14H18O5
7.根据下列性质判断所描述的物质可能属于分子晶体的是( )
A.熔点1070℃,易溶于水,水溶液能导电
B.熔点1128℃,沸点4446℃,硬度很大
C.熔点10.31℃,液态不导电,水溶液能导电
D.熔点97.81℃,质软,导电,密度0.97g/cm3
8.下列说法中不正确的是
A.高吸水性树脂属于功能高分子材料
B.SiC、Al2O3的熔点很高,可用作高温结构陶瓷
C.光导纤维、合成纤维和人造纤维都是有机高分子化合物
D.合金拓展了金属材料的使用范围,合金中也可能含有非金属元素
9.下列物质中,水解前后均可发生银镜反应的是
A.蔗糖 B.麦芽糖 C.淀粉 D.乙酸甲酯
10.共价键、离子键和范德华力都是微粒间的作用力,下列物质:①Na2O2;②SiO2;③石墨;④金刚石;⑤CaH2;⑥白磷,其中含有两种结合力的组合是
A.①③⑤⑥B.①③⑥C.②④⑥D.①②③⑥
11.向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:
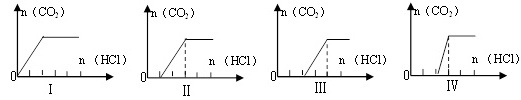
则下列分析都正确的组合是 ( )
溶质的成分
对应图象
溶液中离子浓度关系
A
NaHCO3、Na2CO3
Ⅱ
c(CO32-)c(CO32-)
C
Na2CO3
Ⅳ
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D
NaHCO3
I
c(Na+)=c(HCO3-)
A. B. C. D.
12.萤石(CaF2)晶体属于立方晶系,萤石中每个Ca2+被8个F-所包围,则每个F-周围最近距离的Ca2+数目为( )
A.2 B.4 C.6 D.8
13.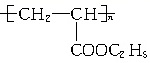 对此聚合物分析正确的是( )
对此聚合物分析正确的是( )
(4)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-bmg/L,现用ClO2将CN-氧化,只生成两种无毒气体,其离子反应方程式为________________,处理100m3这种污水,至少需要ClO2____mol。
.
参考答案与解析:
-
相关试题
-
FeCl3反应的条件是()
-
[单选题]FeCl3反应的条件是()A .芳环B .内酯环C .蒽环D .酚羟基E .活泼氢
- 查看答案
-
FeCl3反应的条件是( )。
-
FeCl3反应的条件是( )。A. 芳环B. 内酯环C. 蒽环D. 酚羟基E. 活泼氢
- 查看答案
-
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物.(1)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3
-
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物.(1)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(
- 查看答案
-
番泻甙A与FeCl3/HCl反应生成()
-
[单选题]番泻甙A与FeCl3/HCl反应生成()A . 2分子大黄酸B . 1分子大黄酸及1分子芦荟大黄素C . 2分子大黄酸葡萄糖甙D . 1分子大黄酸葡萄糖甙及1分子芦荟大黄素葡萄糖甙E . 2分子芦荟大黄素
- 查看答案
-
制备乙酰水杨酸时,常用FeCl3溶液来检查产品的纯度。
-
制备乙酰水杨酸时,常用FeCl3溶液来检查产品的纯度。制备乙酰水杨酸时,常用FeCl3溶液来检查产品的纯度。
- 查看答案
-
遇FeCl3显紫色的是( )。
-
遇FeCl3显紫色的是( )。A. 乙酰水杨酸B. 甲醛C. 苯甲酸D. 水杨酸
- 查看答案
-
取FeCl3的盐酸溶液20.0mL,加入10.0mL含HCl的乙醚溶液一起振荡,已知分配比为48,则FeCl3的萃取率为
-
取FeCl3的盐酸溶液20.0mL,加入10.0mL含HCl的乙醚溶液一起振荡,已知分配比为48,则FeCl3的萃取率为A. 9.6%B. 9.9%C. 50%
- 查看答案
-
测定FeCl3中Cl含量时,选用()指示剂指示终点。
-
[单选题]测定FeCl3中Cl含量时,选用()指示剂指示终点。A .K2Cr2O7B .K2 CrO 5C .NH 4 Fe(SO 4)2?12H 2OD .NH 4 SCN
- 查看答案
-
FeCl3与苯酚生成化合物的颜色是()
-
[单选题]FeCl3与苯酚生成化合物的颜色是()A . 白色B . 蓝紫色C . 黄色D . 黑色
- 查看答案
-
将AgNO3、CuCl2、FeCl3三种溶液用适当装置串联,通一定电量后,各阴极上析出金属的________。
-
将AgNO3、CuCl2、FeCl3三种溶液用适当装置串联,通一定电量后,各阴极上析出金属的________。A. 质量相同B. 物质的量相同D. 都不相同
- 查看答案