复分解反应存在这样一个规律:较强酸可制取较弱酸。中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应。盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解。 已知在常温下测得浓度均为0.lmol/L的下列6种溶液的pH: 溶质 CH3COONa NaHCO3 Na2CO3 NaClO NaCN C6H5ONa pH 8.8 8.1 11.6 10.3 11.1 11.3 (1)请根据上述信息判断下列反应不能发生的是_____(填编号)。 A (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO B (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO C (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO D (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO E (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO F (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO (2)一些复分解反应的发生还遵循其他的规律、下列变化都属于复分解反应: ①将石灰乳与纯碱溶液混合可制得苛性钠溶液 ②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体 ③蒸发KC1和NaNO 3的混合溶液,首先析出NaCl晶体。 根据上述反应,总结出复分解反应发生的另一规律为_____。 (3)已知溶液的pH与氢离子浓度有直接关系。物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是_____(填编号)。 ①C 6H 5OH(苯酚) ②CH 3COOH ③HClO 4 ④HC1O ⑤H 2SO 4 (4)25℃时,M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且 (O)_(2)+(H)_(2)O+2NaClO=(Na)_(2)C(O)_(3)+2HClO,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
复分解反应存在这样一个规律:较强酸可制取较弱酸。中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应。盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解。已知在常温下测得浓度均为0.lmol/L的下列6种溶液的pH:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
| pH |
8.8 |
8.1 |
11.6 |
10.3 |
11.1 |
11.3 |
(1)请根据上述信息判断下列反应不能发生的是_____(填编号)。
A
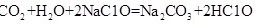
B
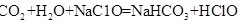
C
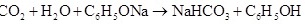
D
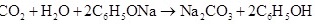
E
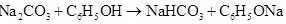
F
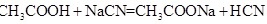
(2)一些复分解反应的发生还遵循其他的规律、下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KC1和NaNO 3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为_____。
(3)已知溶液的pH与氢离子浓度有直接关系。物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是_____(填编号)。
①C 6H 5OH(苯酚) ②CH 3COOH ③HClO 4 ④HC1O ⑤H 2SO 4
(4)25℃时,M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且
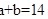 ,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
参考答案与解析:
-
相关试题
-
盐类的水解反应是一个不可逆反应。
-
[判断题] 盐类的水解反应是一个不可逆反应。A . 正确B . 错误
- 查看答案
-
能发生水解反应的盐类,其溶液越稀越有利于盐类的()。
-
[单选题]能发生水解反应的盐类,其溶液越稀越有利于盐类的()。A .溶解B .裂解C .降解D .水解
- 查看答案
-
最易发生水解反应的是强酸强碱盐。()
-
[判断题] 最易发生水解反应的是强酸强碱盐。()A . 正确B . 错误
- 查看答案
-
最易发生水解反应的是强酸强碱盐。( )
-
[主观题]最易发生水解反应的是强酸强碱盐。( )此题为判断题(对,错)。
- 查看答案
-
酯的水解反应是()的逆反应。
-
[单选题]酯的水解反应是()的逆反应。A .酯化反应B .氰解反应C .醇解反应D .氨解反应
- 查看答案
-
水解反应是中和反应的逆过程,故()。
-
[单选题]水解反应是中和反应的逆过程,故()。A .吸热B .放热C .不变D .都不是
- 查看答案
-
水解反应器尿素水解反应是()。
-
[单选题]水解反应器尿素水解反应是()。A . 吸热反应B . 放热反应C . 氧化反应D . 合成反应
- 查看答案
-
电石水解反应是()反应。
-
[填空题] 电石水解反应是()反应。
- 查看答案
-
水解反应是()。
-
[单选题]水解反应是()。A . 将聚合物降解为单体,水被消耗B . 将聚合物降解为单体,并有水的形成C . 由单体形成聚合物,水被消耗D . 由单体形成聚合物,并有水的形成
- 查看答案
-
下列哪类药物容易发生水解反应()
-
[单选题]下列哪类药物容易发生水解反应()A . 酰胺类药物B . 酚类药物C . 烯醇类药物D . 芳胺类药物E . 吡唑酮类药物
- 查看答案