第三章 热力学第二定律[复习题][1]指出下列公式的适用围。封闭体系,非体积功为0的任何过程;或组成可变的多相多组分封闭体系,非体积功为0的可逆过程。(4)非体积功为0,组成不变的均相封闭体系的等温过程。(5)△...S=-R ∑n8 lnxR-|||-B:封闭体系的绝热过程,可判定过程的可逆与否;隔离体系,可判定过程的自发与平衡。△...S=-R ∑n8 lnxR-|||-B:封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否;△...S=-R ∑n8 lnxR-|||-B:封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;[2]判断下列说法是否正确,并说明原因。(1)不可逆过程一定是自发的,而自发过程一定是不可逆的;(2)凡熵增加过程都是自发过程;(3)不可逆过程的熵永不减少;(4)系统达平衡时,熵值最大,Gibbs自由能最小;(5)当某系统的热力学能和体积恒定时,△...S=-R ∑n8 lnxR-|||-B<0的过程不可能发生;(6)某系统从始态经过一个绝热不可逆过程到达终态,先在要在相同的始、终态之间设计一个绝热可逆过程;(7)在一个绝热系统中,发生了一个不可逆过程,系统从状态1变到了状态2,不论用什么方法,系统再也回不到原来状态了;(8)理想气体的等温膨胀过程,△...S=-R ∑n8 lnxR-|||-B,系统所吸的热全部变成了功,这与Kelvin的说法不符;(9)冷冻机可以从低温热源吸热放给高温热源,这与Clausius的说法不符;(10)△...S=-R ∑n8 lnxR-|||-B恒大于△...S=-R ∑n8 lnxR-|||-B。[答](1)不正确,因为不可逆过程不一定是自发的例如 可逆压缩就不是自发过程,但自发过程一定是不可逆的;(2)不正确,因为熵增加过程不一定是自发过程,但自发过程都是熵增加的过程;所以必须在隔离体系中凡熵增加过程都是自发过程。=-26.36kJ(4)绝热可逆膨胀至压力减少一半;Q=0 △S=0△...S=-R ∑n8 lnxR-|||-B根据绝热过程方程△...S=-R ∑n8 lnxR-|||-B得△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B △...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B△A=△U-S△T=-824.58J-100J•K-1•mol-1×1mol×(206.9K-273K)=-5.787kJ△G=△H-S△T=-1374.3J-100J•K-1•mol-1×1mol×(206.9K-273K)=-5.33kJ(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。Q=0△...S=-R ∑n8 lnxR-|||-B即: △...S=-R ∑n8 lnxR-|||-B代入数据得:T2=218.4K所以 △...S=-R ∑n8 lnxR-|||-B=-680.92J△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B=-1.135kJ△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B=1.125J•K-1S2=△S+S1=1.125J•K-1+100J•K-1=101.125J•K-1△A=△U-△TS=△U-(T2S2-T1S1)=-680.92J-(218.4K×101.125J•K-1-273K×100J•K-1)=4.533kJ△G=△H-△TS=△H-(T2S2-T1S1)=-1135J-(218.4K×101.125J•K-1-273K×100J•K-1)=-26.36kJ=4.08kJ[17]将1molH2O(g)从373K,100kPa下,小心等温压缩,在没有灰尘等凝聚中心存在时,得到了373K,200kPa的介稳水蒸气,但不久介稳水蒸气全变成了液态水,即H2O(g,373K,200kPa)→H2O(l,373K,200kPa)求该过程的△H,△G和△S。已知在该条件下水的摩尔汽化焓为△...S=-R ∑n8 lnxR-|||-B,水的密度为1000kg•m-3.设气体为理想气体,液体体积受压力的影响可忽略不计。[解]设计可逆过程如下:=1mol×8.314J•K•mol×373Kln0.5=-2.15kJ△...S=-R ∑n8 lnxR-|||-B=(1mol×0.018kg•mol/1000kg•m)(200kPa-100kPa)=1.8J△G=△G+△G+△G=-2148.2J△...S=-R ∑n8 lnxR-|||-B[18]用合适的判据证明:(1)在373K和200kPa压力下,HO(l)比HO(g)更稳定;(2)在263K和100kPa压力下,H2O(s)比H2O(l)更稳定;[解](1)设计等温可逆过程如下△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B(等温等压无非体积功的可逆相变过程)△...S=-R ∑n8 lnxR-|||-B所以 △...S=-R ∑n8 lnxR-|||-B若水蒸气可看作理想气体,则所以,在373K和200kPa压力下,HO(l)比HO(g)更稳定。(2)设100kPa压力下设计如下可逆过程如下△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B>0所以自发变化总是朝熵增加的方向进行,HO(s)比HO(l)更稳定。[19]在298K和100kPa压力下,已知C(金刚石)和C(石墨)的摩尔熵、摩尔燃烧焓和密度分别为:试求:(1)在298K及100kPa下,C(石墨)→C(金刚石)的;(2)在298K及100kPa时,哪个晶体更为稳定?(3)增加压力能否使不稳定晶体向稳定晶体转化?如有可能,至少要加多大压力,才能实现这种转化?[解] (1)根据△G=△H-T△S=-393.51kJ•mol-(-395.40kJ•mol)=1.89kJ•mol-1=2.45J•K•mol-5.71J•K•mol=-3.26J•K-1•mol-1=2.862kJ•mol(2)因为298K,100kPa下,>0,说明此反应在该条件下不能自发向右进行,亦即石墨比较稳定.(3)设298K下压力为p时石墨恰能变成金刚石△...S=-R ∑n8 lnxR-|||-B>0,解上式得:p>1.52×10Pa即需要加压至1.52×102Pa时,才能在298K时,使石墨转化为金刚石.[20]某实际气体的状态方程为,式中α为常数。设有1mol该气体,在温度为T的等温条件下,由p9可逆地变到p。试写出:Q,W,△U,△H,△S,△A及△G的计算表达式。
第三章 热力学第二定律
[复习题]
[1]指出下列公式的适用围。
(1)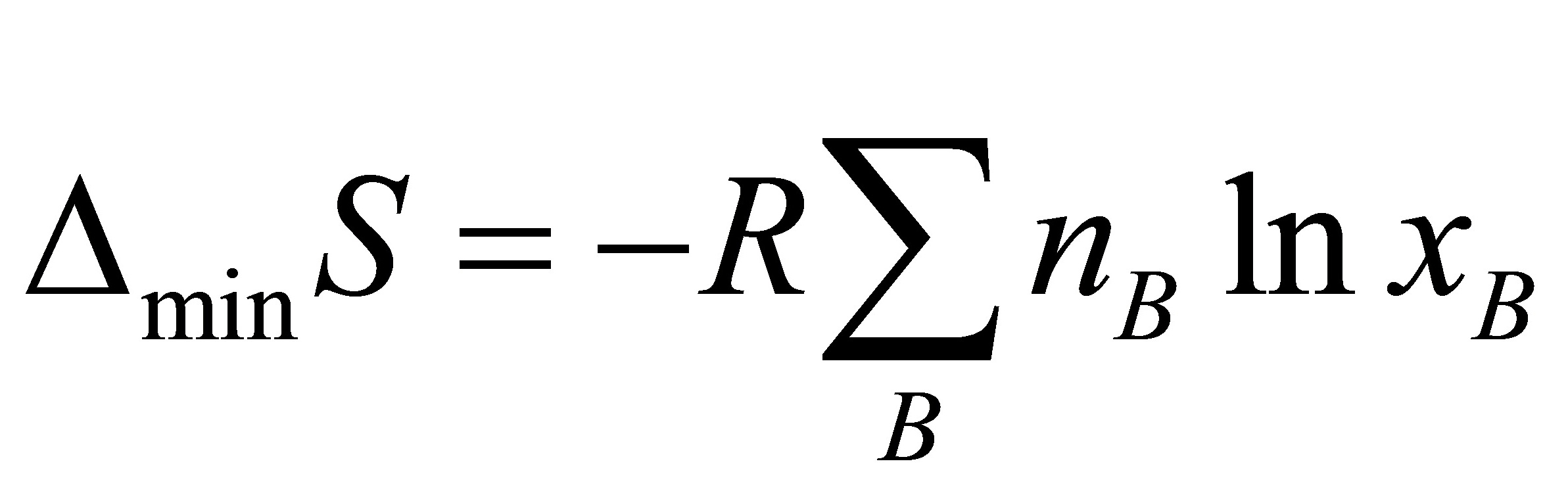 ;
;
(2)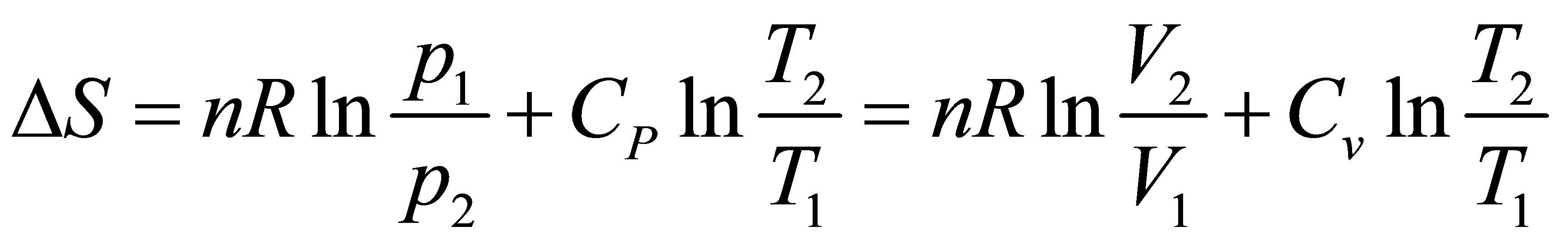 ;
;
(3)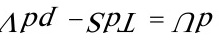 ;
;
(4)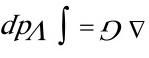
(5)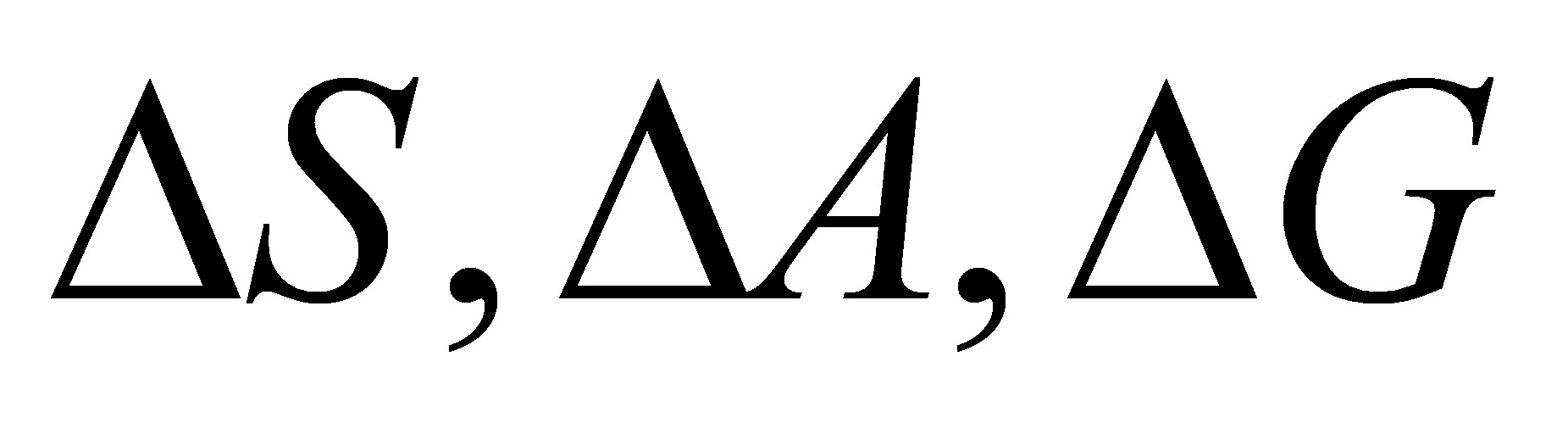 作为判据时必须满足的条件。
作为判据时必须满足的条件。
[解] (1)封闭体系平衡态,理想气体的等温混合,混合前后每种气体单独存在时的压力都相等,且等于混合后气体的总压力。
(2)非等温过程中熵的变化过程,对一定量的理想气体由状态A(P1、V1、T1)改变到状态A(P2、V2、T2)时,可由两种可逆过程的加和而求得。
(3)均相单组分(或组成一定的多组分)封闭体系,非体积功为0的任何过程;或组成可变的多相多组分封闭体系,非体积功为0的可逆过程。
(4)非体积功为0,组成不变的均相封闭体系的等温过程。
(5)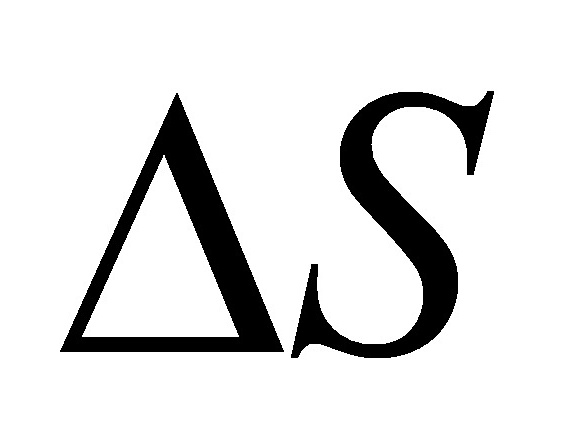 :封闭体系的绝热过程,可判定过程的可逆与否;
:封闭体系的绝热过程,可判定过程的可逆与否;
隔离体系,可判定过程的自发与平衡。
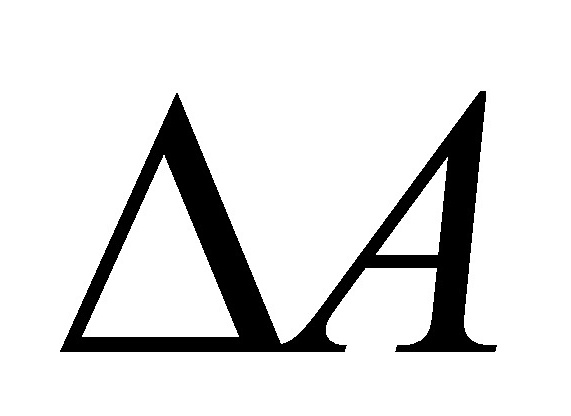 :封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否;
:封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否;
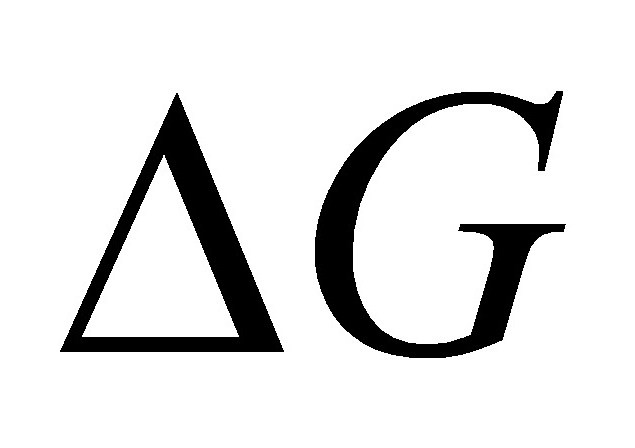 :封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;
:封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;
[2]判断下列说法是否正确,并说明原因。
(1)不可逆过程一定是自发的,而自发过程一定是不可逆的;
(2)凡熵增加过程都是自发过程;
(3)不可逆过程的熵永不减少;
(4)系统达平衡时,熵值最大,Gibbs自由能最小;
(5)当某系统的热力学能和体积恒定时,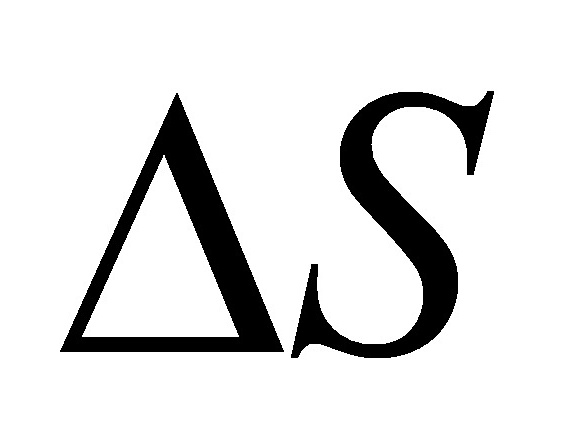 <0的过程不可能发生;
<0的过程不可能发生;
(6)某系统从始态经过一个绝热不可逆过程到达终态,先在要在相同的始、终态之间设计一个绝热可逆过程;
(7)在一个绝热系统中,发生了一个不可逆过程,系统从状态1变到了状态2,不论用什么方法,系统再也回不到原来状态了;
(8)理想气体的等温膨胀过程,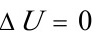 ,系统所吸的热全部变成了功,这与Kelvin的说法不符;
,系统所吸的热全部变成了功,这与Kelvin的说法不符;
(9)冷冻机可以从低温热源吸热放给高温热源,这与Clausius的说法不符;
(10)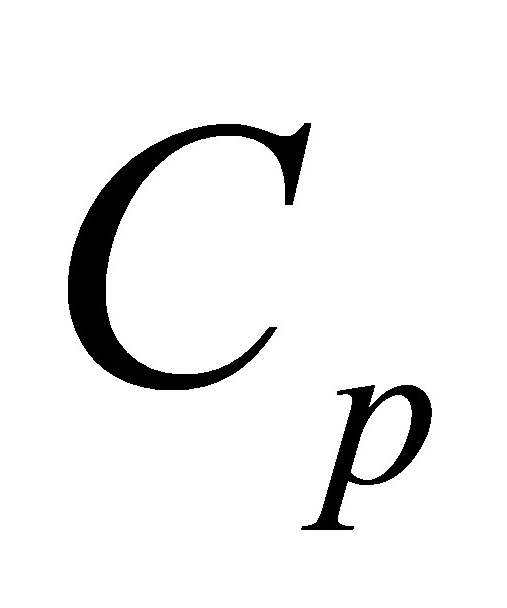 恒大于
恒大于 。
。
[答](1)不正确,因为不可逆过程不一定是自发的例如 可逆压缩就不是自发过程,但自发过程一定是不可逆的;
(2)不正确,因为熵增加过程不一定是自发过程,但自发过程都是熵增加的过程;所以必须在隔离体系中凡熵增加过程都是自发过程。
=-26.36kJ
(4)绝热可逆膨胀至压力减少一半;
Q=0 △S=0
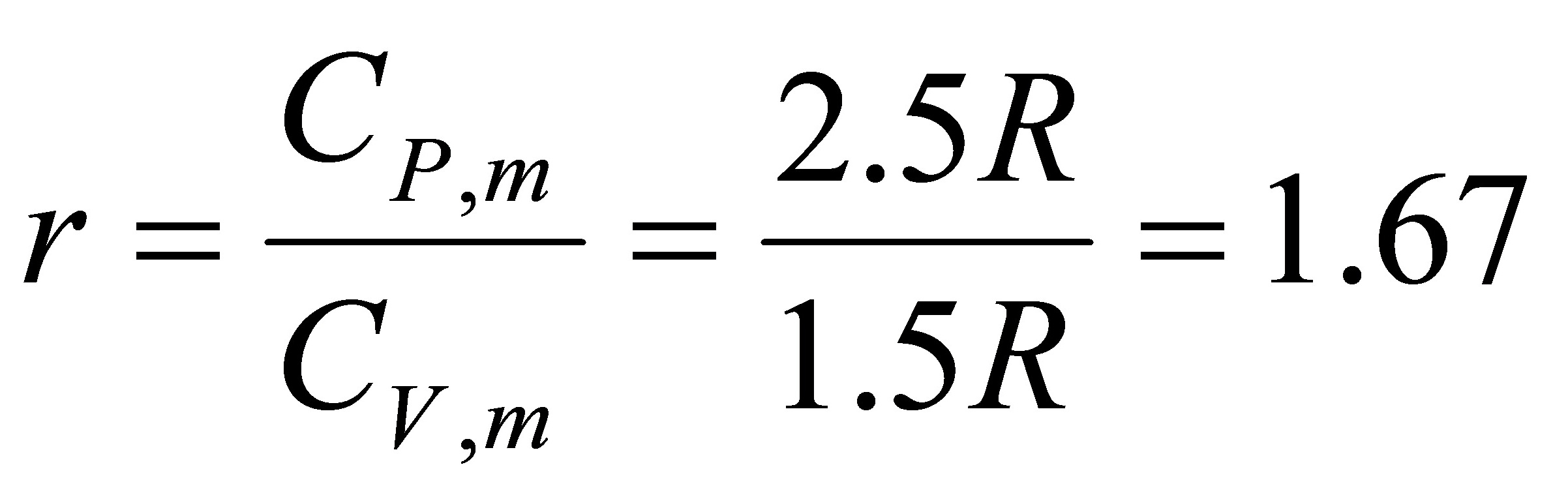
根据绝热过程方程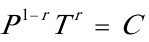 得
得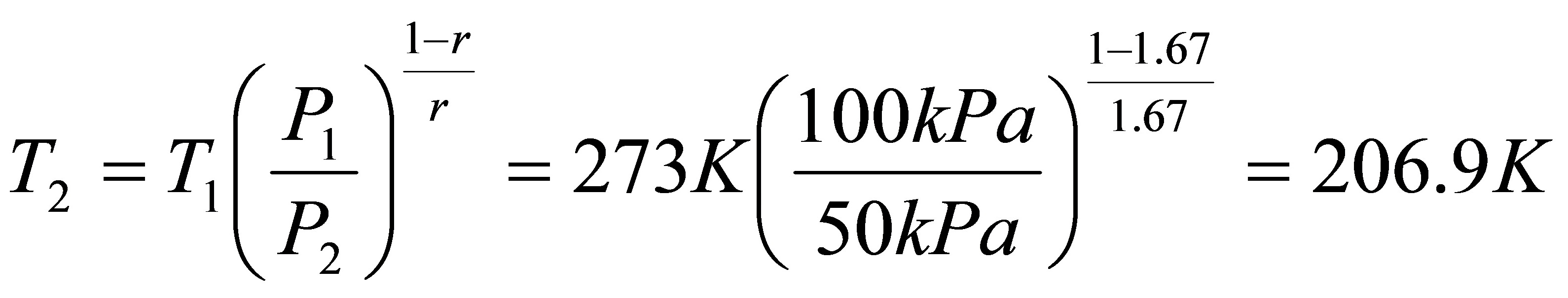
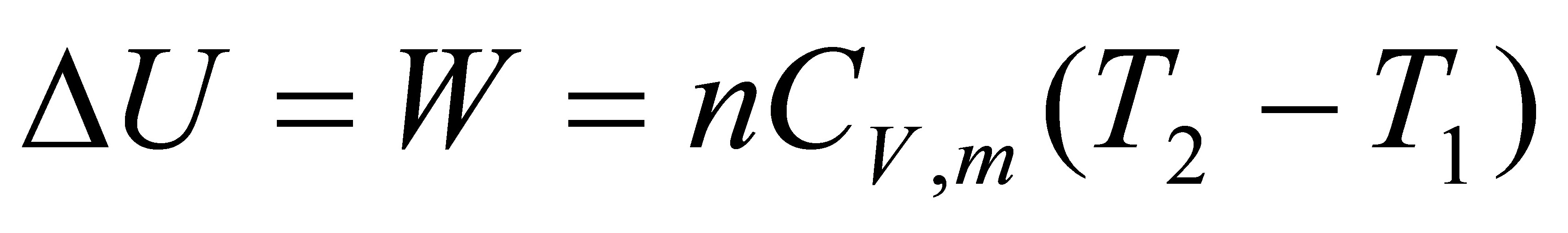
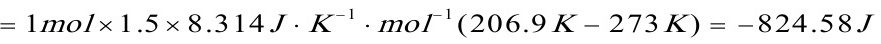
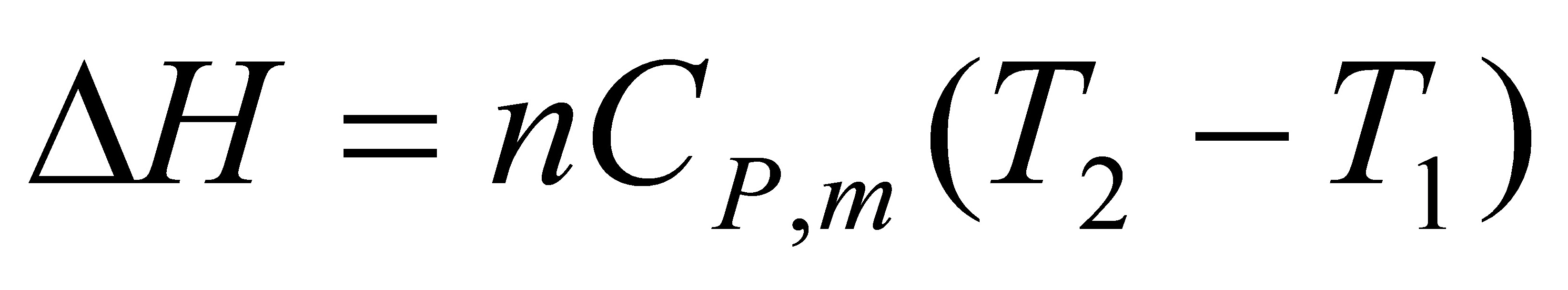
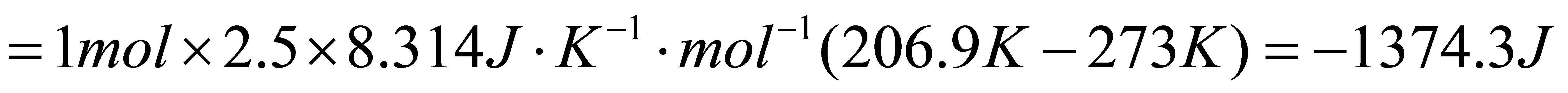
△A=△U-S△T
=-824.58J-100J•K-1•mol-1×1mol×(206.9K-273K)
=-5.787kJ
△G=△H-S△T
=-1374.3J-100J•K-1•mol-1×1mol×(206.9K-273K)
=-5.33kJ
(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。
Q=0
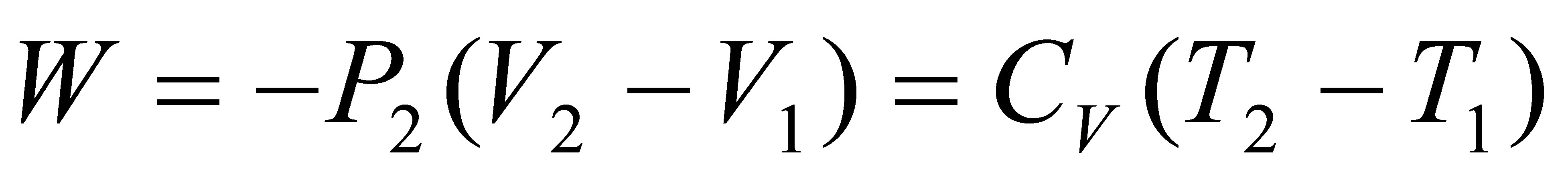
即: 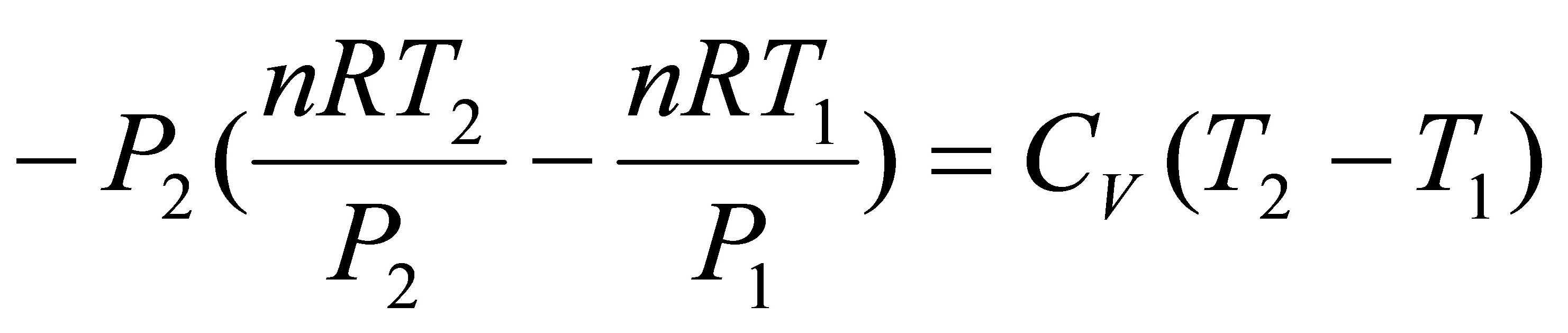
代入数据得:T2=218.4K
所以 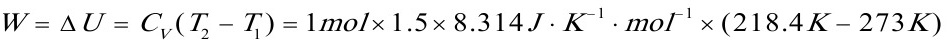
=-680.92J
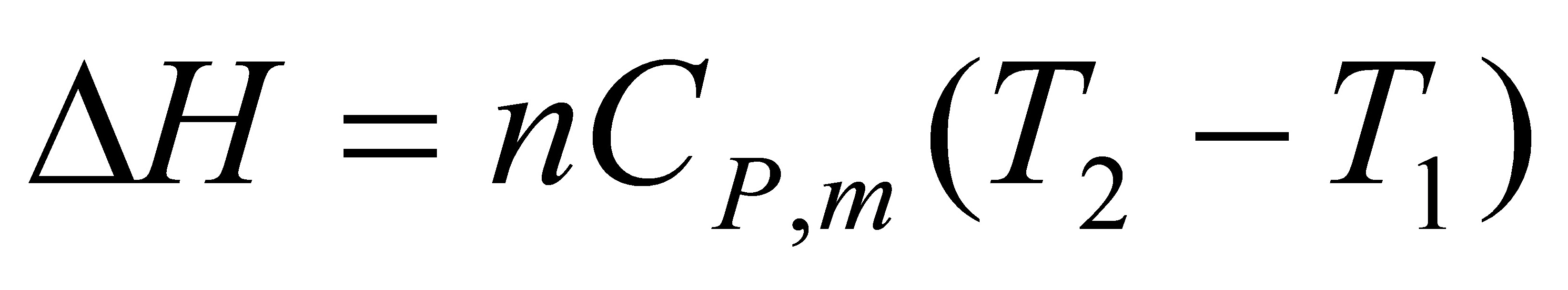
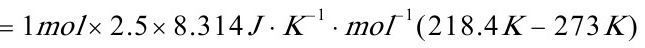
=-1.135kJ
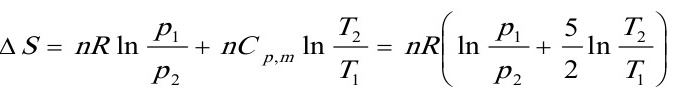
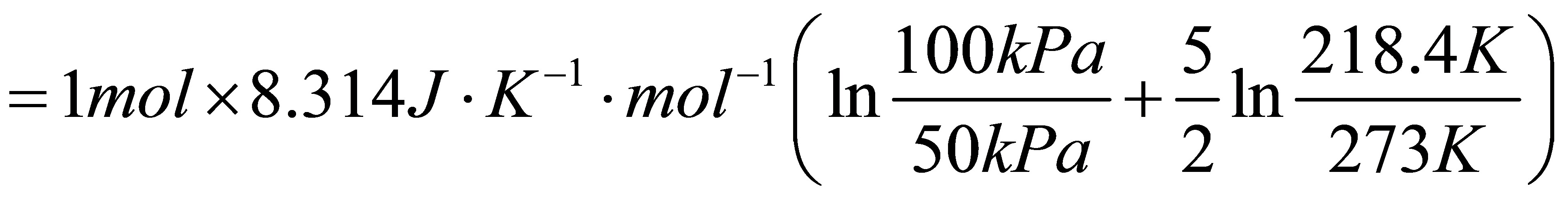
=1.125J•K-1
S2=△S+S1=1.125J•K-1+100J•K-1=101.125J•K-1
△A=△U-△TS=△U-(T2S2-T1S1)
=-680.92J-(218.4K×101.125J•K-1-273K×100J•K-1)
=4.533kJ
△G=△H-△TS=△H-(T2S2-T1S1)
=-1135J-(218.4K×101.125J•K-1-273K×100J•K-1)
=-26.36kJ
=4.08kJ
[17]将1molH2O(g)从373K,100kPa下,小心等温压缩,在没有灰尘等凝聚中心存在时,得到了373K,200kPa的介稳水蒸气,但不久介稳水蒸气全变成了液态水,即
H2O(g,373K,200kPa)→H2O(l,373K,200kPa)
求该过程的△H,△G和△S。已知在该条件下水的摩尔汽化焓为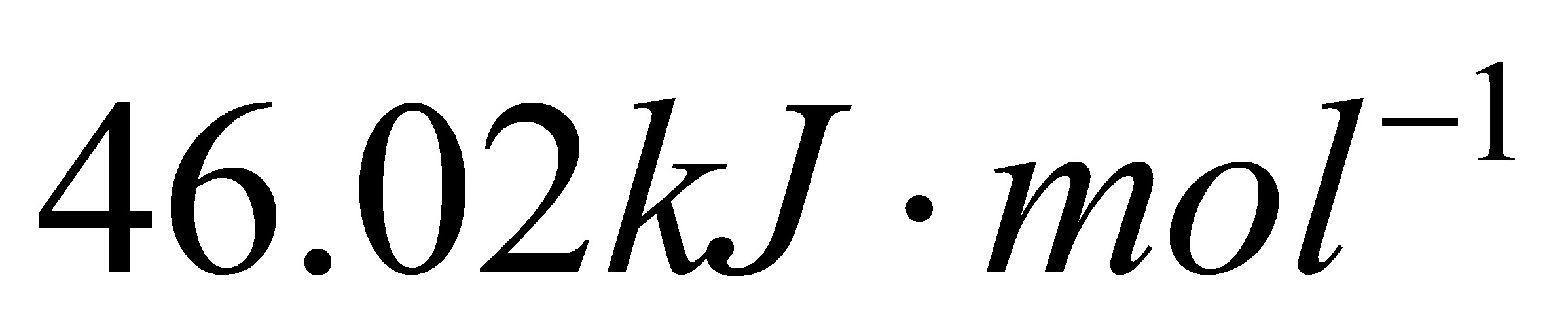 ,水的密度为1000kg•m-3.设气体为理想气体,液体体积受压力的影响可忽略不计。
,水的密度为1000kg•m-3.设气体为理想气体,液体体积受压力的影响可忽略不计。
[解]设计可逆过程如下:
=1mol×8.314J•K•mol×373Kln0.5
=-2.15kJ
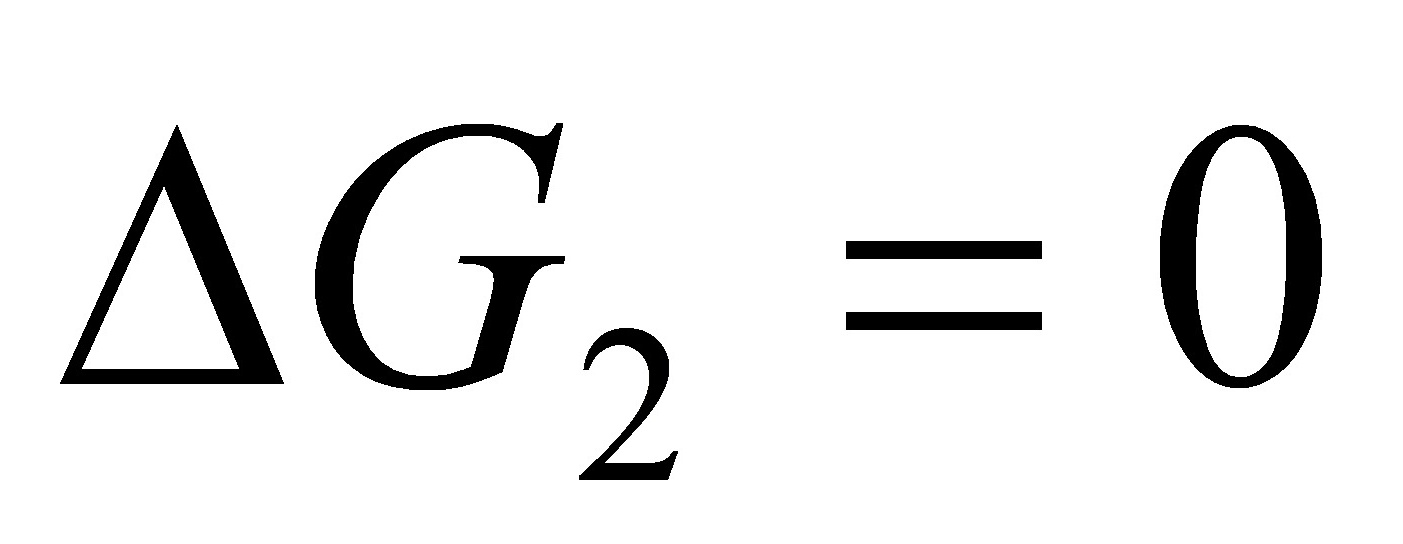
=(1mol×0.018kg•mol/1000kg•m)(200kPa-100kPa)
=1.8J
△G=△G+△G+△G=-2148.2J
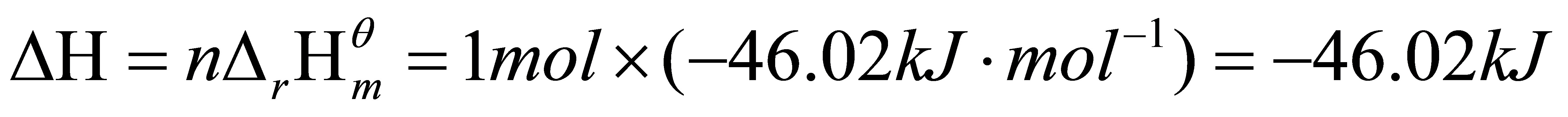
[18]用合适的判据证明:
(1)在373K和200kPa压力下,HO(l)比HO(g)更稳定;
(2)在263K和100kPa压力下,H2O(s)比H2O(l)更稳定;
[解](1)设计等温可逆过程如下
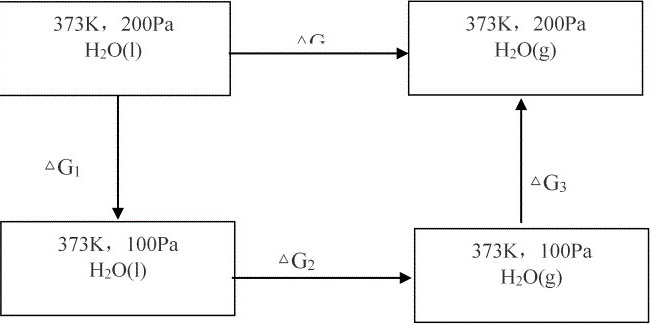
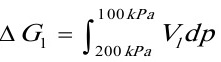 (等温等压无非体积功的可逆相变过程)
(等温等压无非体积功的可逆相变过程)
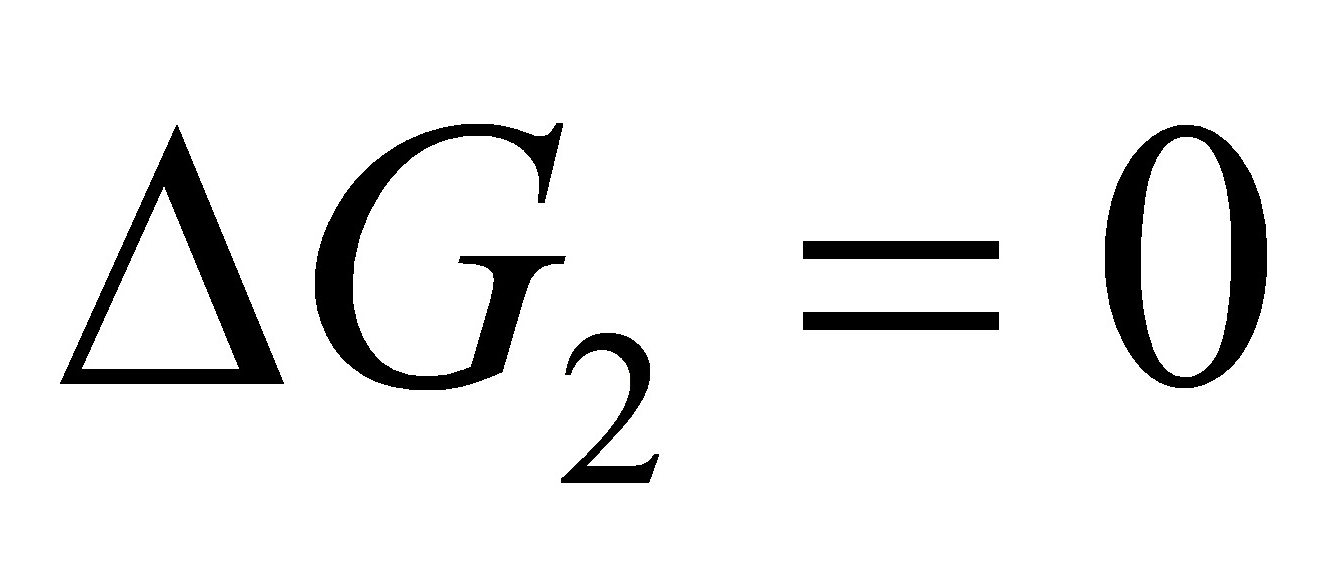
所以 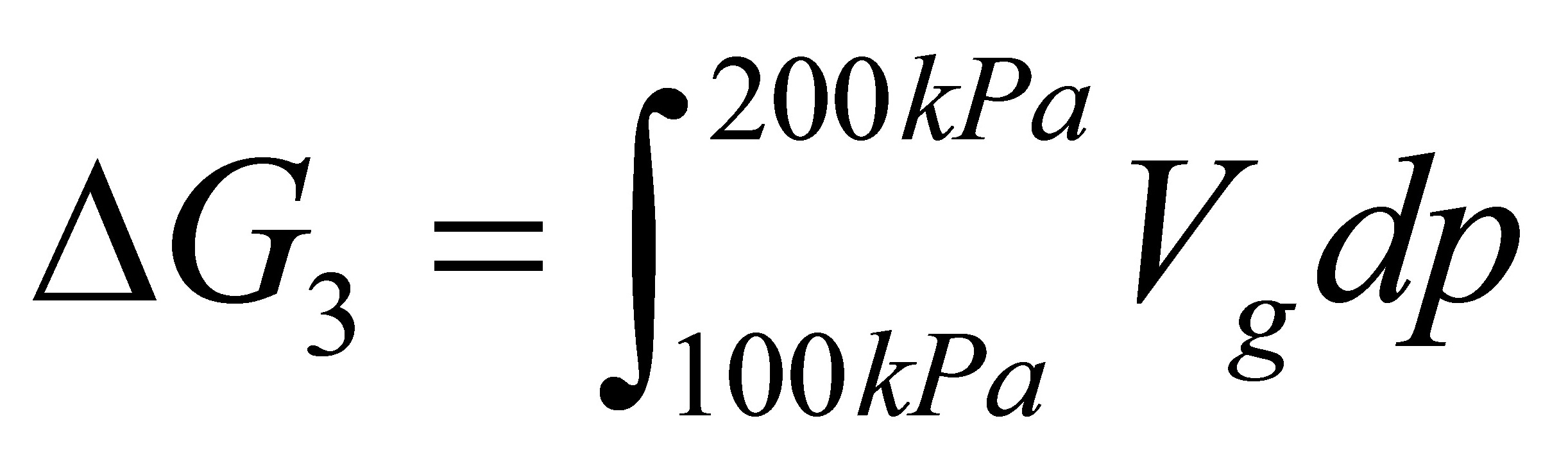
若水蒸气可看作理想气体,则
所以,在373K和200kPa压力下,HO(l)比HO(g)更稳定。
(2)设100kPa压力下设计如下可逆过程如下
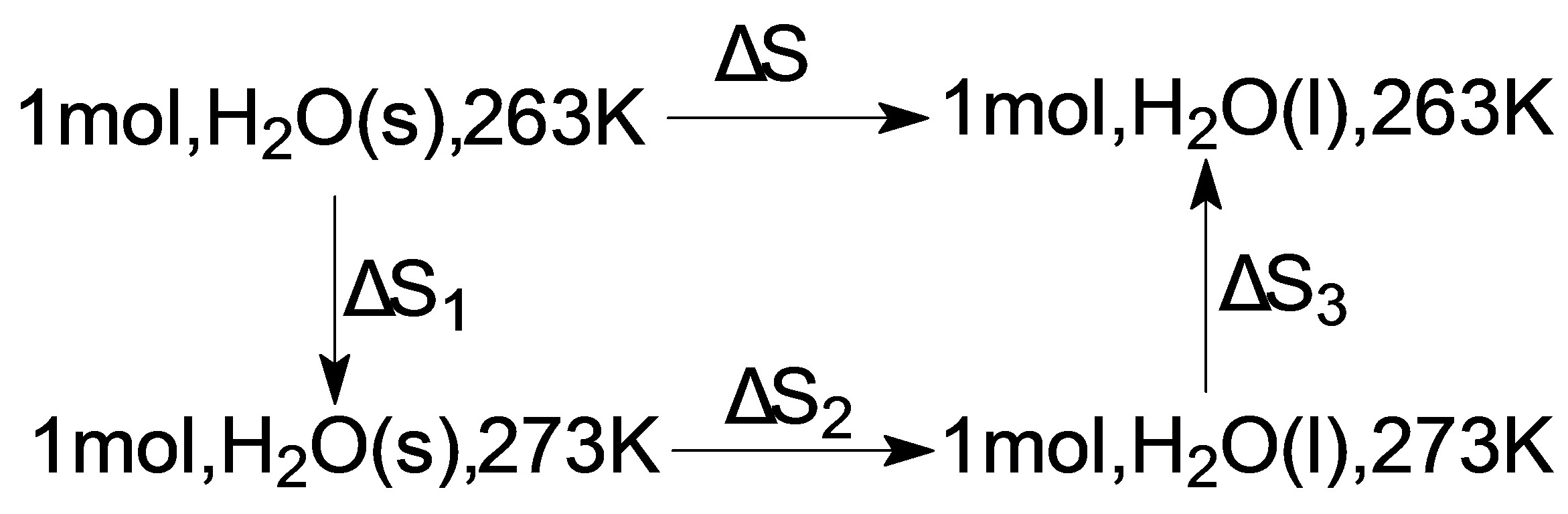
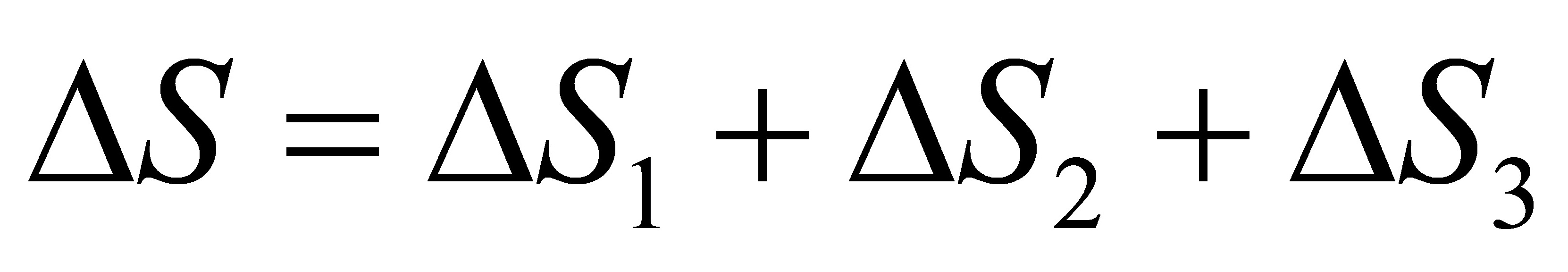 >0所以自发变化总是朝熵增加的方向进行,HO(s)比HO(l)更稳定。
>0所以自发变化总是朝熵增加的方向进行,HO(s)比HO(l)更稳定。
[19]在298K和100kPa压力下,已知C(金刚石)和C(石墨)的摩尔熵、摩尔燃烧焓和密度分别为:
试求:
(1)在298K及100kPa下,C(石墨)→C(金刚石)的;
(2)在298K及100kPa时,哪个晶体更为稳定?
(3)增加压力能否使不稳定晶体向稳定晶体转化?如有可能,至少要加多大压力,才能实现这种转化?
[解] (1)根据△G=△H-T△S
=-393.51kJ•mol-(-395.40kJ•mol)
=1.89kJ•mol-1
=2.45J•K•mol-5.71J•K•mol
=-3.26J•K-1•mol-1
=2.862kJ•mol
(2)因为298K,100kPa下,>0,说明此反应在该条件下不能自发向右进行,亦即石墨比较稳定.
(3)设298K下压力为p时石墨恰能变成金刚石
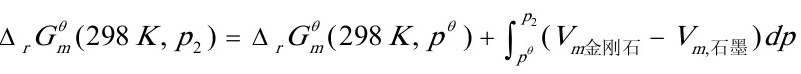 >0,解上式得:
>0,解上式得:
p>1.52×10Pa
即需要加压至1.52×102Pa时,才能在298K时,使石墨转化为金刚石.
[20]某实际气体的状态方程为,式中α为常数。设有1mol该气体,在温度为T的等温条件下,由p9可逆地变到p。试写出:Q,W,△U,△H,△S,△A及△G的计算表达式。
参考答案与解析:
-
相关试题
-
Delta (U)_(T)=0的应用条件为的应用条件为( )A理想气体的恒温过程B孤立体系C恒温恒压,非体积功为零的封闭体系D不作非体积功,无化学反应,均相,封闭体系中的可逆过程E可逆过程
-
Delta (U)_(T)=0的应用条件为的应用条件为( )A理想气体的恒温过程B孤立体系C恒温恒压,非体积功为零的封闭体系D不作非体积功,无化学反应,均
- 查看答案
-
π,x μ(a)dn(a)≤0作为可逆性判据, () 。-|||-A:仅适用于封闭系统不做非体积功时的相变化过程;-|||-B:仅适用于封闭系统不做非体积功时的化学变化过程;-|||-C:适用于封闭系
-
π,x μ(a)dn(a)≤0作为可逆性判据, () 。-|||-A:仅适用于封闭系统不做非体积功时的相变化过程;-|||-B:仅适用于封闭系统不做非体积功时的
- 查看答案
-
封闭体系,不做非体积功的条件下,以下关系错误的是( )
-
封闭体系,不做非体积功的条件下,以下关系错误的是( )A. ΔU=QvB. ΔH=QpC. ΔU=Q-WD. W(体)= -ΔnRT
- 查看答案
-
对于非体积功为0的定容过程,封闭系统从环境吸收的热量,全部用于系统热力学能的增加, 即QV =△U(定容,W'=0)
-
对于非体积功为0的定容过程,封闭系统从环境吸收的热量,全部用于系统热力学能的增加, 即QV =△U(定容,W=0)对于非体积功为0的定容过程,封闭系统从环境吸收
- 查看答案
-
在非体积功为零的条件下, 封闭系统经一等压过程, 所吸收的热全部用于增加系统的热力学能。“A( )
-
在非体积功为零的条件下, 封闭系统经一等压过程, 所吸收的热全部用于增加系统的热力学能。“A( )在非体积功为零的条件下, 封闭系统经一等压过程, 所吸收
- 查看答案
-
1.在恒压且不做非体积功的条件下,热力学第一定律可表述为 () 。-|||-
-
1.在恒压且不做非体积功的条件下,热力学第一定律可表述为 () 。-|||-
- 查看答案
-
封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。
-
[单选题]封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。A.应等于此过程的△UB.应等于该系统的△HC.应等于此过程的△HD.应等于此过程
- 查看答案
-
封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。
-
[单选题]封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。A.应等于此过程的△UB.应等于该系统的△HC.应等于此过程的△HD.应等于此过程
- 查看答案
-
封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。
-
[单选题]封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。A.应等于此过程的△UB.应等于该系统的△HC.应等于此过程的△HD.应等于此过程
- 查看答案
-
封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。
-
[单选题]封闭系统在不做非体积功、恒压下经历某过程后,其与环境所交换的热()。A.应等于此过程的△UB.应等于该系统的△HC.应等于此过程的△HD.应等于此过程
- 查看答案