中南大学郑雅杰等3位老师提出“以含砷废水沉淀还原法制备As2O3”,有较高的实际应用价值。某工厂含砷废水含有H3AsO3、H2SO4、Fe2(SO4)3、Bi2(SO4)3等,利用该废水提取As2O3的流程如图1所示。NaOH,调节pH为6 ①过量CuSO4 水-|||-含砷废水 中和 滤液1 过滤 Cu,(AsO4)2沉淀 -S(O)_(2)-|||-沉淀1 ②NaOH,调节pH为8 过滤-|||-As2O, 干燥 蒸发浓缩、冷却结晶 H,AsO,溶液 Cu1(SO,)2·2H2O 氧化 A-|||-图1 离子浓度(mol/L)开始沉淀pH离子 10-1 10-2 10-3 10-4 10-5 Fe3+ 1.9 2.2 2.5 2.9 3.2 Cu2+ 4.7 5.2 5.7 6.2 6.7 (1)为了加快中和过程的速率,可以采取的措施有 ____ (写出一条合理的措施即可)。(2)沉淀Ⅰ中的成分,除了Bi(OH)3沉淀外,还有 ____ 。(3)A可以循环利用,A的化学式为 ____ 。在滤液1中,加入NaOH调节pH为8的目的是 ____ 。(4)Cu3(AsO3)2沉淀加入一定量的水调成浆料,通入SO2,该过程的化学反应方程式是 ____ 。(5)按照一定的液固比,将水加入Cu3(AsO3)2沉淀中,调成浆料。当反应温度为25℃,SO2流量为16L/h,液固比、时间对砷、铜浸出率的影响如图2甲、乙所示。请选择最适宜的液固比、反应时间: ____ 、 ____ 。NaOH,调节pH为6 ①过量CuSO4 水-|||-含砷废水 中和 滤液1 过滤 Cu,(AsO4)2沉淀 -S(O)_(2)-|||-沉淀1 ②NaOH,调节pH为8 过滤-|||-As2O, 干燥 蒸发浓缩、冷却结晶 H,AsO,溶液 Cu1(SO,)2·2H2O 氧化 A-|||-图1(6)一定条件下,用雄黄(As4S4)制备As2O3的转化关系如图3所示。若反应中,1mol As4S4(其中As元素的化合价为+2价)参加反应时,转移28mol e-,则物质a为 ____ (填化学式)。
中南大学郑雅杰等3位老师提出“以含砷废水沉淀还原法制备As2O3”,有较高的实际应用价值。某工厂含砷废水含有H3AsO3、H2SO4、Fe2(SO4)3、Bi2(SO4)3等,利用该废水提取As2O3的流程如图1所示。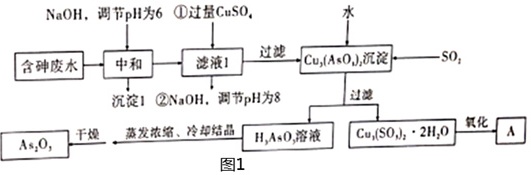
| 离子浓度(mol/L) 开始沉淀pH 离子 |
10-1 | 10-2 | 10-3 | 10-4 | 10-5 |
| Fe3+ | 1.9 | 2.2 | 2.5 | 2.9 | 3.2 |
| Cu2+ | 4.7 | 5.2 | 5.7 | 6.2 | 6.7 |
(2)沉淀Ⅰ中的成分,除了Bi(OH)3沉淀外,还有 ____ 。
(3)A可以循环利用,A的化学式为 ____ 。在滤液1中,加入NaOH调节pH为8的目的是 ____ 。
(4)Cu3(AsO3)2沉淀加入一定量的水调成浆料,通入SO2,该过程的化学反应方程式是 ____ 。
(5)按照一定的液固比,将水加入Cu3(AsO3)2沉淀中,调成浆料。当反应温度为25℃,SO2流量为16L/h,液固比、时间对砷、铜浸出率的影响如图2甲、乙所示。请选择最适宜的液固比、反应时间: ____ 、 ____ 。
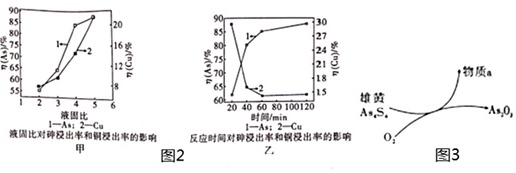
(6)一定条件下,用雄黄(As4S4)制备As2O3的转化关系如图3所示。若反应中,1mol As4S4(其中As元素的化合价为+2价)参加反应时,转移28mol e-,则物质a为 ____ (填化学式)。
参考答案与解析:
-
相关试题
-
配平方程式FeSO4+HNO3+H2SO4→Fe2(SO4)3+NO+H2O时,
-
[单选题]配平方程式FeSO4+HNO3+H2SO4→Fe2(SO4)3+NO+H2O时,H2O前面的化学计量数是()。A . 2B . 3C . 4D . 6
- 查看答案
-
配平下列反应式:FeSO4+HNO3+H2SO4=Fe2(SO4)3+NO↑+H
-
[单选题]配平下列反应式:FeSO4+HNO3+H2SO4=Fe2(SO4)3+NO↑+H2O,下列答案中系数自左到右正确的是()。A .6,2,2,3,2,4;B .6,2,3,3,2,4;C .6,2,1,3,2,1;D .6,2,3,3,2,9。
- 查看答案
-
用WPS打印出电离方程式:Fe2(SO4)3=2Fe3++3SO2-4。
-
[问答题] 用WPS打印出电离方程式:Fe2(SO4)3=2Fe3++3SO2-4。
- 查看答案
-
电极a 电源 电极b-|||-Ce(SO4)2溶液-|||->-|||-Ce2O3 石墨-|||-←x-|||-Ce(SO4)2与H 2SO4溶液 离子交换膜利用废料Ce_(2)O_(3)制备C
-
电极a 电源 电极b-|||-Ce(SO4)2溶液-|||->-|||-Ce2O3 石墨-|||-←x-|||-Ce(SO4)2与H 2SO4溶液 离子交换膜利
- 查看答案
-
17.| -S(O)_(3)H 浓 (O)_(3)+ 浓H2SO4 /、-|||-NO2
-
17.| -S(O)_(3)H 浓 (O)_(3)+ 浓H2SO4 /、-|||-NO2
- 查看答案
-
用离子-电子法配平下列反应式 (1)H2O2+Cr2(SO4)3+KOHrarr;K2CrO4+K2SO4+H2O (2)KMnO4+KNO2+KOHrarr;K2MnO4+KNO3+H2O (3)P
-
用离子-电子法配平下列反应式(1)H2O2+Cr2(SO4)3+KOHrarr;K2CrO4+K2SO4+H2O(2)KMnO4+KNO2+KOHrarr;K2
- 查看答案
-
H2SO4:H2O=(1:3)也可表示成( )。
-
[单选题]H2SO4:H2O=(1:3)也可表示成( )。A.20%H2SO4B.25%H2SO4C.30%H2SO4D.35%H2SO4E.40%H2SO4
- 查看答案
-
在H2、H2O、H2SO4、Fe、Fe3O4五种物质中,属于单质的是()。
-
[填空题] 在H2、H2O、H2SO4、Fe、Fe3O4五种物质中,属于单质的是()。
- 查看答案
-
Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,3Cu+8HNO3(稀
-
[单选题]Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,根据以上两个反应,说明硫酸和硝酸具有()。A .和金属起置换反应的性质;B .还原性;C .强烈的氧化性;D .剧烈的腐蚀性。
- 查看答案
-
三.根据化学式写出相应名称-|||-Na2O CaCl2 NaOH KCl-|||-KNO3 NaCl K2CO3 CaSO4-|||-Na2CO3 CaO SO2-|||-Fe2(SO4)-|||-
-
三.根据化学式写出相应名称-|||-Na2O CaCl2 NaOH KCl-|||-KNO3 NaCl K2CO3 CaSO4-|||-Na2CO3 CaO S
- 查看答案