已知氯气与强碱溶液反应时,生成的产物受温度的影响。实验室中利用如图1装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。-a-|||-MnO2 KOH-|||-水-|||-粉末 溶液-|||-下 NaOH-|||-冰水- 溶液-|||-A B C D E-|||-图1回答下列问题:(1)仪器a的名称是_______。(2)装置A产生氯气的化学方程式为_______。(3)装置B中的试剂为_______,该装置作用为_______。(4)装置C采用的加热方式是_______,装置D中发生反应的离子方程式为_______。(5)装置E的作用是_______,可选用试剂_______。(填标号)a.NaCl溶液b.NaOH溶液c.稀硫酸(6)探究KClO3和NaClO的氧化能力(图2)-a-|||-MnO2 KOH-|||-水-|||-粉末 溶液-|||-下 NaOH-|||-冰水- 溶液-|||-A B C D E-|||-图1操作:向1号(KClO3)和2号(NaClO)试管中,滴加中性KI溶液。现象:1号试管溶液颜色不变,2号试管溶液变为棕色。结论:该条件下氧化能力KClO3_______NaClO。(填“大于”或“小于”)(7)工业上常用氯碱工业来制备氯气,其原理为电解饱和食盐水,生成氯气的同时还可得到氢气和烧碱,请写出该反应的离子方程式_______。
已知氯气与强碱溶液反应时,生成的产物受温度的影响。实验室中利用如图1装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。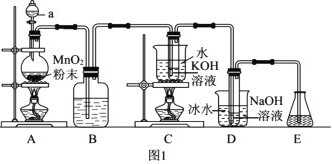
回答下列问题:
(1)仪器a的名称是_______。
(2)装置A产生氯气的化学方程式为_______。
(3)装置B中的试剂为_______,该装置作用为_______。
(4)装置C采用的加热方式是_______,装置D中发生反应的离子方程式为_______。
(5)装置E的作用是_______,可选用试剂_______。(填标号)
a.NaCl溶液b.NaOH溶液c.稀硫酸
(6)探究KClO3和NaClO的氧化能力(图2)
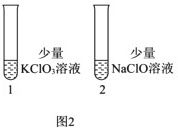
操作:向1号(KClO3)和2号(NaClO)试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3_______NaClO。(填“大于”或“小于”)
(7)工业上常用氯碱工业来制备氯气,其原理为电解饱和食盐水,生成氯气的同时还可得到氢气和烧碱,请写出该反应的离子方程式_______。
参考答案与解析:
-
相关试题
-
在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产
-
[试题]在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)编号 1 2 3 4 加水的质量(g) 10 10 10 10 剩余固体的质量(g) 7.25 4.05 m 3试求:(1)表中m值为_____________ 。(2)所制得氧气的质量。
- 查看答案
-
白色固体粉末氯酸钾(KClO3),在二氧化锰(MnO2)作催化剂并加热的条件下能
-
[试题]白色固体粉末氯酸钾(KClO3),在二氧化锰(MnO2)作催化剂并加热的条件下能较快地分解成氯化钾和氧气,试写出该反应的化学方程式。
- 查看答案
-
炼钢过程中锰氧化反应生成的产物是MnO2。
-
[判断题] 炼钢过程中锰氧化反应生成的产物是MnO2。A . 正确B . 错误
- 查看答案
-
某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。干燥的Cl2 铜粉-|||-A 空试管 水 紫色石AgNO3NaOH-|||-B C 蕊溶液 溶液 溶液-|||-D E F已知:该装置气
-
某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。干燥的Cl2 铜粉-|||-A 空试管 水 紫色石AgNO3NaOH-|||-B C 蕊溶液 溶液
- 查看答案
-
根据下列仪器装置,回答问题。同-|||-A B C D-|||-干燥CO2 氧气-|||-a d-|||-b紫色 c澄清-|||-石蕊 石灰-|||-溶液 水(1)实验室用MnO2和30%的双氧水制
-
根据下列仪器装置,回答问题。同-|||-A B C D-|||-干燥CO2 氧气-|||-a d-|||-b紫色 c澄清-|||-石蕊 石灰-|||-溶液 水
- 查看答案
-
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。1列收集Cl2的正确装置时 。NaOH-|||-溶液
-
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。1列收集Cl2的正确
- 查看答案
-
18.氯气氯气(Cl2)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、-|||-农药、燃料和药品等。-|||-I 氯气的制备-|||-I 氯气的制备-|||-氯气在实验室中可通过MnO2和浓盐酸混
-
18.氯气氯气(Cl2)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、-|||-农药、燃料和药品等。-|||-I 氯气的制备-|||-I 氯气的制备-|||
- 查看答案
-
当水和碱金属反应时,生成哪种以下哪种物质( )。A、盐和氢气B、酸溶液C、碱溶液
-
[单选题]当水和碱金属反应时,生成哪种以下哪种物质( )。A.盐和氢气B.酸溶液C.碱溶液D.不溶性的金属氢氧化物E.碱金属的氧化物
- 查看答案
-
当水和碱金属反应时,生成A、酸溶液B、不溶性的金属氢氧化物C、碱溶液D、盐和氢气
-
[单选题]当水和碱金属反应时,生成A.酸溶液B.不溶性的金属氢氧化物C.碱溶液D.盐和氢气E.碱金属的氧化物
- 查看答案
-
已知,从标准电极电势看,MnO2不能氧化Cl-,但用MnO2加浓盐酸,可以生成C
-
[单选题]已知,从标准电极电势看,MnO2不能氧化Cl-,但用MnO2加浓盐酸,可以生成Cl2,这是因为()。A . 两个相差不大B . 酸性增强,也增加C . Cl-浓度增加,减少D . 以上三个因素都有
- 查看答案