-8原子和离子半径变化有如下一些规律:① 对同种元素的原子半径,共价半径总是小于金属原子半径。② 对同种元素的离子半径来说,阳离子的半径总是小于该元素的原子半径,且正价愈高,半径愈小;阴离子的半径总是大于该元素的原子半径,且负价愈高,半径愈大。③ 同一族元素,离子半径从上向下逐渐增大;④ 同一周期元素,阳离子半径从左向右逐渐减小;⑤ 周期表左上方到右下方对角线方向,阳离子半径近于相等。减小-|||-大 相-|||-、1-11)等同点:晶体结构中物质环境和几何环境完全相同的点,称“等同点”。2)空间格子:联结分布在三维空间内的结点3)单位平行六面体:在空间格子中,所选取的平行六面体的对称性符合整个空间点阵的对称性;棱与棱之间的直角应力求最多;在遵循上两个条件的前提下,所选取的平行六面体的体积应最小。考虑到对称性不能为直角时,选结点间距最小的行列做平行六面体的棱,棱间交角接近直角。按照上述选择原则选取的平行六面体称为单位平行六面体。4)点群 (对称型):结晶多面体中全部对称要素的组合,称为该结晶多面体的对称型。由于在结晶多面体中,全部对称要素相交于一点(晶体几何中心),在进行对称操作时该点不移动,所以对称型也称为点群。5)平移群:晶体结构中所有平移轴的结合。6)空间群:微观对称要素不可能交于一点,因此晶体构造中对称要素的组合叫空间群。7)晶胞:是指晶体结构中的平行六面体单位,其形状大小与对应的空间格子中的平行六面体一致。1-2一切晶体所共有的性质即晶体的基本性质: 1、自限性;2、均一性;3、异向性;4、对称性;5、最小内能;6、稳定性是由晶体的格子构造所决定,1-3晶体对称定律:在晶体中不可能存在五次及大于六次的对称轴。因为不符合空间格子构造规律,其对应的网孔不能毫无间隙地布满整个平面。减小-|||-大 相-|||-、1-9 以NaCl晶胞为例,试说明面心立方紧密堆积中的八面体和四面体空隙的位置和数量。答:以NaCl晶胞中(001)面心的一个球(Cl-离子)为例,它的正下方有1个八面体空隙(体心位置),与其对称,正上方也有1个八面体空隙;前后左右各有1个八面体空隙(棱心位置)。所以共有6个八面体空隙与其直接相邻,由于每个八面体空隙由6个球构成,所以属于这个球的八面体空隙数为6×1/6=1。 在这个晶胞中,这个球还与另外2个面心、1个顶角上的球构成4个四面体空隙(即1/8小立方体的体心位置);由于对称性,在上面的晶胞中,也有4个四面体空隙由这个参与构成。所以共有8个四面体空隙与其直接相邻,由于每个四面体空隙由4个球构成,所以属于这个球的四面体空隙数为8×1/4=2。1-10 临界半径比的定义是:紧密堆积的阴离子恰好互相接触,并与中心的阳离子也恰好接触的条件下,阳离子半径与阴离子半径之比。即每种配位体的阳、阴离子半径比的下限。计算下列配位的临界半径比:(a)立方体配位;(b)八面体配位;(c)四面体配位;(d)三角形配位。
-8原子和离子半径变化有如下一些规律:
① 对同种元素的原子半径,共价半径总是小于金属原子半径。
② 对同种元素的离子半径来说,阳离子的半径总是小于该元素的原子半径,且正价愈高,半径愈小;阴离子的半径总是大于该元素的原子半径,且负价愈高,半径愈大。
③ 同一族元素,离子半径从上向下逐渐增大;
④ 同一周期元素,阳离子半径从左向右逐渐减小;
⑤ 周期表左上方到右下方对角线方向,阳离子半径近于相等。
1-1
1)等同点:晶体结构中物质环境和几何环境完全相同的点,称“等同点”。
2)空间格子:联结分布在三维空间内的结点
3)单位平行六面体:在空间格子中,所选取的平行六面体的对称性符合整个空间点阵的对称性;棱与棱之间的直角应力求最多;在遵循上两个条件的前提下,所选取的平行六面体的体积应最小。考虑到对称性不能为直角时,选结点间距最小的行列做平行六面体的棱,棱间交角接近直角。按照上述选择原则选取的平行六面体称为单位平行六面体。
4)点群 (对称型):结晶多面体中全部对称要素的组合,称为该结晶多面体的对称型。由于在结晶多面体中,全部对称要素相交于一点(晶体几何中心),在进行对称操作时该点不移动,所以对称型也称为点群。
5)平移群:晶体结构中所有平移轴的结合。
6)空间群:微观对称要素不可能交于一点,因此晶体构造中对称要素的组合叫空间群。
7)晶胞:是指晶体结构中的平行六面体单位,其形状大小与对应的空间格子中的平行六面体一致。
1-2
一切晶体所共有的性质即晶体的基本性质: 1、自限性;2、均一性;3、异向性;4、对称性;5、最小内能;6、稳定性是由晶体的格子构造所决定,
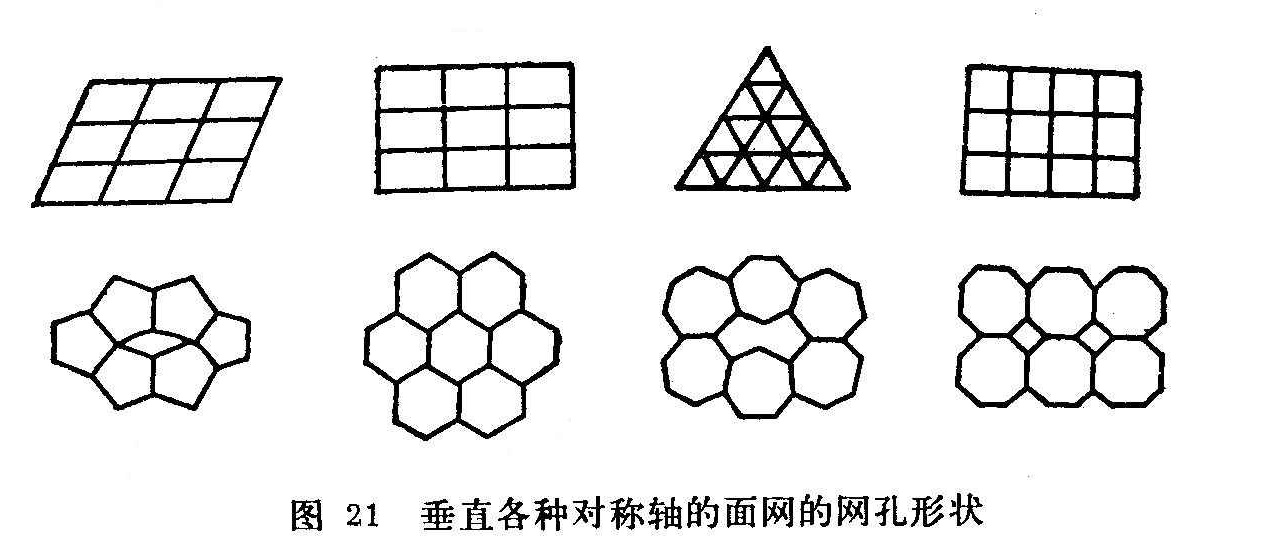
1-3晶体对称定律:在晶体中不可能存在五次及大于六次的对称轴。因为不符合空间格子构造规律,其对应的网孔不能毫无间隙地布满整个平面。
1-9 以NaCl晶胞为例,试说明面心立方紧密堆积中的八面体和四面体空隙的位置和数量。
答:以NaCl晶胞中(001)面心的一个球(Cl-离子)为例,它的正下方有1个八面体空隙(体心位置),与其对称,正上方也有1个八面体空隙;前后左右各有1个八面体空隙(棱心位置)。所以共有6个八面体空隙与其直接相邻,由于每个八面体空隙由6个球构成,所以属于这个球的八面体空隙数为6×1/6=1。 在这个晶胞中,这个球还与另外2个面心、1个顶角上的球构成4个四面体空隙(即1/8小立方体的体心位置);由于对称性,在上面的晶胞中,也有4个四面体空隙由这个参与构成。所以共有8个四面体空隙与其直接相邻,由于每个四面体空隙由4个球构成,所以属于这个球的四面体空隙数为8×1/4=2。
1-10 临界半径比的定义是:紧密堆积的阴离子恰好互相接触,并与中心的阳离子也恰好接触的条件下,阳离子半径与阴离子半径之比。即每种配位体的阳、阴离子半径比的下限。计算下列配位的临界半径比:(a)立方体配位;(b)八面体配位;(c)四面体配位;(d)三角形配位。
参考答案与解析:
-
相关试题
-
原子、离子半径对元素溶解能力的影响主要是通过
-
[问答题] 原子、离子半径对元素溶解能力的影响主要是通过
- 查看答案
-
如何定义离子半径?实际(有效)离子半径受到哪些因素的影响?
-
[问答题] 如何定义离子半径?实际(有效)离子半径受到哪些因素的影响?
- 查看答案
-
()与组成材料各元素的原子量、原子(离子)半径和该材料的结构有关。
-
[单选题]()与组成材料各元素的原子量、原子(离子)半径和该材料的结构有关。A . 相对密度B . 密度C . 质量D . 重量
- 查看答案
-
同价离子,离子半径愈大,交换能力()
-
[单选题]同价离子,离子半径愈大,交换能力()A . 愈弱B . 愈强C . 离子半径与其交换能力无关
- 查看答案
-
下列各组原子和离子半径变化的顺序中,不正确的一组是()。
-
[单选题]下列各组原子和离子半径变化的顺序中,不正确的一组是()。A.B.C.D.
- 查看答案
-
离子半径越大,正负离子间的引力()。
-
[单选题]离子半径越大,正负离子间的引力()。A .越大B .越小C .不变D .无关
- 查看答案
-
(南开91)①!"离子半径!"Å,!"离子半径!"=1.33Å,按离子晶体的结晶化学规律,!"晶体中!"离子的配位数应为( 6 ),!&qu
-
(南开91)①!"离子半径!"Å,!"离子半径!"=1.33Å,按离子晶体的结晶化学规律,!"晶体中!"离子的配位数应为( 6 ),!"离子占据的!"负离子的多
- 查看答案
-
下列元素中,原子半径最大的是( )
-
下列元素中,原子半径最大的是( )A. OB. CC. FD. N
- 查看答案
-
下列元素的原子半径递变规律正确的是()。
-
[单选题]下列元素的原子半径递变规律正确的是()。A.K>Ca>Mg>AlB.Ca>K>Al>MgC.Al>Mg>Ca>KD.Mg>Al>K>Ca
- 查看答案