已知:(rho )^theta ((Cu)^+/(Cu)_(1))=0.521W ,(rho )^theta ((Cu)^+/(Cu)_(1))=0.521W(1)当c(Cu2+) =0.01mol·L-1, c(Cu+) =0.1mol·L-1时,求反应Cu2+(aq) + Cu(s) === 2 Cu+(aq)的电池电动势E。(2)求上反应在298K的K。
已知: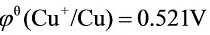 ,
,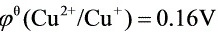
(1)当c(Cu2+) =0.01mol·L-1, c(Cu+) =0.1mol·L-1时,求反应
Cu2+(aq) + Cu(s) === 2 Cu+(aq)的电池电动势E。
(2)求上反应在298K的K。
参考答案与解析:
-
相关试题
-
已知电池 Cu|Cu2+(a2)||Cu2+(a1)|Cu 和 Pt|Cu2+(a2),Cu+(a′)||Cu2+(a1),Cu+(a′)|Pt 的电动势分别为 E1 和 E2,则( )A.E1
-
已知电池 Cu|Cu2+(a2)||Cu2+(a1)|Cu 和 Pt|Cu2+(a2),Cu+(a′)||Cu2+(a1),Cu+(a′)|Pt 的电动势分别为
- 查看答案
-
已知φy( Cu2+/Cu ) = 0.342 V,Cu(OH)2的Ksp= 2.2×10-20,那么φy( Cu(OH)2/Cu )为
-
已知φy( Cu2+/Cu ) = 0.342 V,Cu(OH)2的Ksp= 2.2×10-20,那么φy( Cu(OH)2/Cu )为A. -0.238 VB
- 查看答案
-
根据 varphi^theta(Cu^2+ / Cu)= 0.34 V, varphi^theta(Fe^3+ / Fe^2+ )= 0.77 V,判断标准状态下能将Cu氧化为Cu^2+,但
-
根据 varphi^theta(Cu^2+ / Cu)= 0.34 V, varphi^theta(Fe^3+ / Fe^2+ )= 0.77 V,判
- 查看答案
-
在298.15时,两电对Fe3+/ Fe2+和Cu2+/Cu组成原电池,其中 c(Fe3+)=c(Fe2+)=c(Cu2+)=0.10 mol·L-1已知 :
-
在298.15时,两电对Fe3+/ Fe2+和Cu2+/Cu组成原电池,其中 c(Fe3+)=c(Fe2+)=c(Cu
- 查看答案
-
17.电池(1) |(Cu)^+||(Cu)^+,(Cu)^2+|Pt 和电池(2) /(Cu)^2+||(Cu)^+,(Cu)^2+|Pt 的电池反应均可简写为-|||-+(Cu)^2+=!=!=
-
17.电池(1) |(Cu)^+||(Cu)^+,(Cu)^2+|Pt 和电池(2) /(Cu)^2+||(Cu)^+,(Cu)^2+|Pt 的电池反应均可简写
- 查看答案
-
7-22 已知 ((Cu)^2+/(Cu)^+)=0.1607W, ((Cu)^2+/CuI)=0.866V,-|||-Ksp(CuI)为 () 。-|||-
-
7-22 已知 ((Cu)^2+/(Cu)^+)=0.1607W, ((Cu)^2+/CuI)=0.866V,-|||-Ksp(CuI)为 () 。-|||-
- 查看答案
-
6.已知 (varphi )^theta ((Mn)^2+Mn)=-1.029V ; (varphi )^theta ((Cu)^2+/Cu)=0.342V ; varphi (Ag'+Ag)
-
6.已知 (varphi )^theta ((Mn)^2+Mn)=-1.029V ; (varphi )^theta ((Cu)^2+/Cu)=0.342V ;
- 查看答案
-
25℃时,在Cu2+的氨水溶液中,平衡时c(NH3)=6.710-4mol·L-1,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2+形式存在.则[Cu(NH3)4]2+的
-
25℃时,在Cu2+的氨水溶液中,平衡时c(NH3)=6.710-4mol·L-1,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2
- 查看答案
-
计算KI浓度为1mol·L-1时,Cu2+/Cu+电对的条件电位(忽略离子强度的影响),并说明何以能发生下列反应:2Cu2++5I-=2Cu↓+I-3。
-
计算KI浓度为1mol·L-1时,Cu2+/Cu+电对的条件电位(忽略离子强度的影响),并说明何以能发生下列反应:2Cu2++5I-=2Cu↓+I-3。计算KI
- 查看答案