氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及1,4-二(氯甲基)苯等可通过氯化反应制备。(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:SO2(g)+Cl2(g)⇌SO2Cl2(g) ΔH=-67.59kJ•mol-1①若正反应的活化能为E正kJ•mol-1,则逆反应的活化能E逆= ____ kJ•mol-1(用含E正的代数式表示)。②恒容密闭容器中按不同进料比充入SO2(g)和Cl2(g),测定T1、T2、T3温度下体系达平衡时的Δp(Δp=p0-p,p0为体系初始压强,p0=240kPa,p为体系平衡压强),结果如图甲。75A-|||-75 70-|||-70-|||-65 M(2,60) 65|-|||-60 60-|||-三50 55-|||-55|-|||-45-|||-40 T1 50-|||-35| 45-|||-30| T2 40-|||-25 D-|||-20 T 35|-|||-1 1.5 2 2.5 3 3.5 4-|||-n(SO2):n(Cl2)-|||-甲-|||-75A-|||-70-|||-65|-|||-60-|||-55-|||-50-|||-45-|||-40-|||-D-|||-35|-|||-0.0 0.5 1.5 2.0 2.0 2.5 3 3.5 4.0-|||-n(SO 2):n(Cl2)图甲中温度由高到低的顺序为 ____ ,判断依据为 ____ 。M点Cl2的转化率为 ____ 。T1温度下用分压表示的平衡常数Kp= ____ kPa-1。③图乙曲线中能准确表示T1温度下Δp随进料比变化的是 ____ (填序号)。(2)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅度氯化时反应过程为75A-|||-75 70-|||-70-|||-65 M(2,60) 65|-|||-60 60-|||-三50 55-|||-55|-|||-45-|||-40 T1 50-|||-35| 45-|||-30| T2 40-|||-25 D-|||-20 T 35|-|||-1 1.5 2 2.5 3 3.5 4-|||-n(SO2):n(Cl2)-|||-甲-|||-75A-|||-70-|||-65|-|||-60-|||-55-|||-50-|||-45-|||-40-|||-D-|||-35|-|||-0.0 0.5 1.5 2.0 2.0 2.5 3 3.5 4.0-|||-n(SO 2):n(Cl2)→_(①)^Cl_(2)75A-|||-75 70-|||-70-|||-65 M(2,60) 65|-|||-60 60-|||-三50 55-|||-55|-|||-45-|||-40 T1 50-|||-35| 45-|||-30| T2 40-|||-25 D-|||-20 T 35|-|||-1 1.5 2 2.5 3 3.5 4-|||-n(SO2):n(Cl2)-|||-甲-|||-75A-|||-70-|||-65|-|||-60-|||-55-|||-50-|||-45-|||-40-|||-D-|||-35|-|||-0.0 0.5 1.5 2.0 2.0 2.5 3 3.5 4.0-|||-n(SO 2):n(Cl2)以上各反应的速率方程均可表示为v=kc(A)c(B),其中c(A)、c(B)分别为各反应中对应反应物的浓度,k为速率常数(k1~k5分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气浓度恒定(反应体系体积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下,k1:k2:k3:k4:k5=100:21:7:4:23。①30min时,c(X)=6.80mol•L-1,且30~60min内v(X)=0.042mol•L-1•min-1,反应进行到60min时,c(X)= ____ mol•L-1。②60min时,c(D)=0.099mol•L-1,若0~60min产物T的含量可忽略不计,则此时c(G)= ____ mol•L-1;60min后,随T的含量增加,(c(D))/(c(G)) ____ (填“增大”“减小”或“不变”)。
氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及1,4-二(氯甲基)苯等可通过氯化反应制备。(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
SO2(g)+Cl2(g)⇌SO2Cl2(g) ΔH=-67.59kJ•mol-1
①若正反应的活化能为E正kJ•mol-1,则逆反应的活化能E逆= ____ kJ•mol-1(用含E正的代数式表示)。
②恒容密闭容器中按不同进料比充入SO2(g)和Cl2(g),测定T1、T2、T3温度下体系达平衡时的Δp(Δp=p0-p,p0为体系初始压强,p0=240kPa,p为体系平衡压强),结果如图甲。
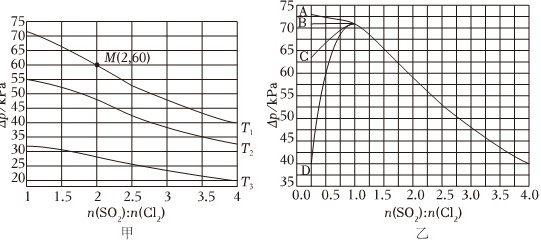
图甲中温度由高到低的顺序为 ____ ,判断依据为 ____ 。M点Cl2的转化率为 ____ 。T1温度下用分压表示的平衡常数Kp= ____ kPa-1。
③图乙曲线中能准确表示T1温度下Δp随进料比变化的是 ____ (填序号)。
(2)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅度氯化时反应过程为
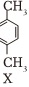 $→_{①}^{Cl_{2}}$
$→_{①}^{Cl_{2}}$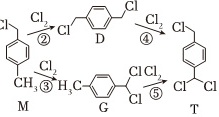
以上各反应的速率方程均可表示为v=kc(A)c(B),其中c(A)、c(B)分别为各反应中对应反应物的浓度,k为速率常数(k1~k5分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气浓度恒定(反应体系体积变化忽略不计),测定不同时刻相关物质的浓度。
已知该温度下,k1:k2:k3:k4:k5=100:21:7:4:23。
①30min时,c(X)=6.80mol•L-1,且30~60min内v(X)=0.042mol•L-1•min-1,反应进行到60min时,c(X)= ____ mol•L-1。
②60min时,c(D)=0.099mol•L-1,若0~60min产物T的含量可忽略不计,则此时c(G)= ____ mol•L-1;60min后,随T的含量增加,$\frac{c(D)}{c(G)}$ ____ (填“增大”“减小”或“不变”)。
参考答案与解析:
-
相关试题
-
氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及1,4-二(氯甲基)苯等可通过氯化反应制备。(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:SO2(g)+Cl2(g)⇌SO
-
氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及1,4-二(氯甲基)苯等可通过氯化反应制备。(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原
- 查看答案
-
B-|||-b-|||-A C 浓盐酸-|||-602 a-|||-活性炭一 KClO3-|||-甲 乙 丙 丁硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,也可用于制造医药、染料、农药等。有关物质的部
-
B-|||-b-|||-A C 浓盐酸-|||-602 a-|||-活性炭一 KClO3-|||-甲 乙 丙 丁硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,也可
- 查看答案
-
18.氯气氯气(Cl2)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、-|||-农药、燃料和药品等。-|||-I 氯气的制备-|||-I 氯气的制备-|||-氯气在实验室中可通过MnO2和浓盐酸混
-
18.氯气氯气(Cl2)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、-|||-农药、燃料和药品等。-|||-I 氯气的制备-|||-I 氯气的制备-|||
- 查看答案
-
化学名为2,3-二氯-4-(2-亚甲基丁酰)苯氧乙酸的是()
-
[单选题,A2型题,A1/A2型题] 化学名为2,3-二氯-4-(2-亚甲基丁酰)苯氧乙酸的是()A . 依他尼酸B . 米力农C . 盐酸维拉帕米D . 呋塞米E . 硝酸甘油
- 查看答案
-
化学名为(2,3-二氯-4-(2-亚甲基丁酰基)苯氧基)乙酸()
-
[单选题,B型题] 化学名为(2,3-二氯-4-(2-亚甲基丁酰基)苯氧基)乙酸()A . 依他尼酸B . 呋噻米C . 盐酸维拉帕米D . 米力农E . 硝酸甘油
- 查看答案
-
有效氯是指A、含氯化合物中,氯的价数>£1者B、含氯化合物中,氯的价数>0者C
-
[单选题]有效氯是指A.含氯化合物中,氯的价数>-1者B.含氯化合物中,氯的价数>0者C.含氯化合物中,氯的价数≥-1者D.含氯化合物中,氯的价数=-1者E.含氯化合物中,氯的价数=0者
- 查看答案
-
原料中的氯化氢和脱氯剂中的有效金属组分进行反应,生成金属氯化物是()
-
[单选题]原料中的氯化氢和脱氯剂中的有效金属组分进行反应,生成金属氯化物是()A . 易挥发的物质B . 不稳定的物质C . 易发生热分解的物质D . 稳定的物质
- 查看答案
-
(),特别是五氯酚钠C6Cl5onA广泛应用于工业冷却水处理。常用氯酚和铜盐混合
-
[单选题](),特别是五氯酚钠C6Cl5onA广泛应用于工业冷却水处理。常用氯酚和铜盐混合控制藻类,间歇投药,可以得到满意的效果。A . 表面活性剂B . 化学药剂处理法C . 氯酚杀菌剂D . 硫酸铜
- 查看答案
-
2.11 写出 2,2,4- 三甲基戊烷进行氯化反应可能得到的一氯代产物的结构式。
-
2.11 写出 2,2,4- 三甲基戊烷进行氯化反应可能得到的一氯代产物的结构式。
- 查看答案
-
氯化聚乙烯防水卷材的主体原料--氯化聚乙烯树脂的含氯量为( )。
-
[单选题]氯化聚乙烯防水卷材的主体原料--氯化聚乙烯树脂的含氯量为( )。A.20%~30%B.20%~40%C.30%~40%D.30%~50%
- 查看答案