从砷化镓废料(主要成分为GaAs、含Fe2O3、SiO2和CaCO3等杂质)中回收镓和砷的工艺流程如图所示:NaOH、H2O2 H2SO4 NaOH滤渣Ⅲ 尾液-|||-申化镓 ↓ ↑-|||-废料 一 浆化 → 碱浸1 → 浸出液 调pH 滤渣Ⅱ 碱浸2 → 电解 Ga-|||-↓-|||-滤渣I 滤液→ 操作 →Na3AsO4·12H2O已知:①Ga与Al同族,Ga(OH)3是两性氢氧化物。②25℃时,Ksp[Ga(OH)3]=7.0×10-36,电离常数Ka[Ga(OH)3]=1.0×10-7。回答下列问题:(1)写出Ga(OH)3在水中的电离方程式: ____ 。(2)“浆化”过程将砷化镓废料转变为悬浊液,目的是 ____ 。(3)“碱浸1”过程,砷化镓转化为NaGaO2和Na3AsO4,该反应的离子方程式为 ____ 。(4)为提高镓的回收率,加硫酸调pH的最大值是 ____ (溶液中含镓元素的微粒的浓度不大于1.0×10-6时,认为该微粒沉淀完全,lg7≈0.85)。(5)“电解”是指用传统的方法将Ga(OH)3溶解到NaOH溶液中,电解得到金属镍。电解时,GaO2-在阴极放电的电极反应式: ____ 。(6)向“调pH”后得到的滤液中加入足量NaOH溶液,使pH大于12,经 ____ 、降温结晶、过滤、洗涤、 ____ 后得到Na3AsO4⋅12H2O。(7)某同学为了探究可逆反应AsO33-(aq)+I2(aq)+2OH-(aq)⇌AsO43-(aq)+2I-(aq)+H2O(l)。设计如图1所示装置。实验操作及现象:按图1装置加入试剂并连接装置,电流由C2流向C1。当不产生电流时,向图1装置左边烧杯中加入一定量2mol⋅L-1盐酸,发现又产生电流,实验中电流与时间的关系如图2所示:NaOH、H2O2 H2SO4 NaOH滤渣Ⅲ 尾液-|||-申化镓 ↓ ↑-|||-废料 一 浆化 → 碱浸1 → 浸出液 调pH 滤渣Ⅱ 碱浸2 → 电解 Ga-|||-↓-|||-滤渣I 滤液→ 操作 →Na3AsO4·12H2O下列说法正确的是 ____ 。a.实验开始时,电子由C1经盐桥流向C2b.图2中,b点时反应达到化学平衡状态c.向左边烧杯中加入盐酸后,平衡逆向移动d.若将所加的盐酸换成氢氧化钠溶液,平衡逆向移动,电流增大
从砷化镓废料(主要成分为GaAs、含Fe2O3、SiO2和CaCO3等杂质)中回收镓和砷的工艺流程如图所示: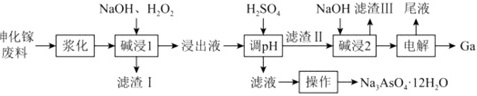
已知:①Ga与Al同族,Ga(OH)3是两性氢氧化物。
②25℃时,Ksp[Ga(OH)3]=7.0×10-36,电离常数Ka[Ga(OH)3]=1.0×10-7。
回答下列问题:
(1)写出Ga(OH)3在水中的电离方程式: ____ 。
(2)“浆化”过程将砷化镓废料转变为悬浊液,目的是 ____ 。
(3)“碱浸1”过程,砷化镓转化为NaGaO2和Na3AsO4,该反应的离子方程式为 ____ 。
(4)为提高镓的回收率,加硫酸调pH的最大值是 ____ (溶液中含镓元素的微粒的浓度不大于1.0×10-6时,认为该微粒沉淀完全,lg7≈0.85)。
(5)“电解”是指用传统的方法将Ga(OH)3溶解到NaOH溶液中,电解得到金属镍。电解时,GaO2-在阴极放电的电极反应式: ____ 。
(6)向“调pH”后得到的滤液中加入足量NaOH溶液,使pH大于12,经 ____ 、降温结晶、过滤、洗涤、 ____ 后得到Na3AsO4⋅12H2O。
(7)某同学为了探究可逆反应AsO33-(aq)+I2(aq)+2OH-(aq)⇌AsO43-(aq)+2I-(aq)+H2O(l)。设计如图1所示装置。实验操作及现象:按图1装置加入试剂并连接装置,电流由C2流向C1。当不产生电流时,向图1装置左边烧杯中加入一定量2mol⋅L-1盐酸,发现又产生电流,实验中电流与时间的关系如图2所示:
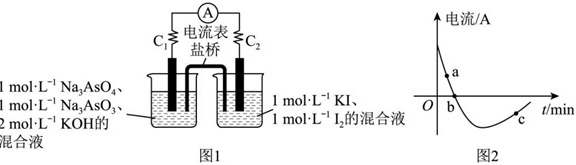
下列说法正确的是 ____ 。
a.实验开始时,电子由C1经盐桥流向C2
b.图2中,b点时反应达到化学平衡状态
c.向左边烧杯中加入盐酸后,平衡逆向移动
d.若将所加的盐酸换成氢氧化钠溶液,平衡逆向移动,电流增大
参考答案与解析:
-
相关试题
-
泥化夹层的主要化学成分为SiO2:、Al2O3、Fe2O3,其次为CaO、MgO
-
[单选题]泥化夹层的主要化学成分为SiO2:、Al2O3、Fe2O3,其次为CaO、MgO、K2O、Na2O等。由于碱金属离子的溶失和游离氧化物的凝聚,与母岩相比泥化夹层的化学成分含量发生了一定的变化,下列说法错误的是()。A . 泥化后CaO的含量比母岩低B . 泥化后Al2O3、Fe2O3的含量比母岩高C . 泥化后Al2O3、Fe2O3的含量比母岩低D . 泥化后Fe2O3的含量比母岩低
- 查看答案
-
废旧锂离子电池的正极材料主要成分是LiCoO_(2),还含有少量金属Al、Fe以及其他不溶性物质,采用如图1工艺流程回收其中的钴制备Co单质:NaOH溶液H2SO4 H2O2 氨水 氨水 HCl-||
-
废旧锂离子电池的正极材料主要成分是LiCoO_(2),还含有少量金属Al、Fe以及其他不溶性物质,采用如图1工艺流程回收其中的钴制备Co单质:NaOH溶液H2S
- 查看答案
-
镓砷磷是砷化镓和磷化镓的固溶体,是一种()材料。
-
[填空题] 镓砷磷是砷化镓和磷化镓的固溶体,是一种()材料。
- 查看答案
-
辉铜矿的主要成分为Cu2S(含少量Fe2O3、SiO2等杂质)。用辉铜矿冶炼铜的主要工艺流程如图所示:空气 X气体 富氧空气 精铜-|||-磨细-|||-高温脱硫 空气 焦炭-|||-粗铜 吹炼-||
-
辉铜矿的主要成分为Cu2S(含少量Fe2O3、SiO2等杂质)。用辉铜矿冶炼铜的主要工艺流程如图所示:空气 X气体 富氧空气 精铜-|||-磨细-|||-高温脱
- 查看答案
-
以废锌催化剂(主要成分为ZnO及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的流程如图1:,O2 适量 有机试 硫酸-|||-过量 (H)_(3)-(N{H)_(4)}_(4)Cl 溶液 溶
-
以废锌催化剂(主要成分为ZnO及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的流程如图1:,O2 适量 有机试 硫酸-|||-过量 (H)_(3)-(
- 查看答案
-
2NaOH+()NH3↑+Na2SO4+2H2O。
-
[单选题]2NaOH+()NH3↑+Na2SO4+2H2O。A . NH3SO4B . NH4HSO4C . NH3HSO3D . NH4SO3
- 查看答案
-
以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6颜料。工艺流程如图:H2SO4-|||-足量 (NH4)2SO4-|||-H2SO4 黄铁矿 H2O NaCl
-
以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6颜料。工艺流程如图:H2SO4-|||-足量 (NH4)2SO4-||
- 查看答案
-
亚氯酸钠(NaClO2)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如图。H2SO4 SO2 H2O2、NaOH-|||-↓-|||-NaClO3 →
-
亚氯酸钠(NaClO2)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如图。H2SO4 SO2 H2O2、NaOH
- 查看答案
-
11.辉铜矿的主要成分为Cu2S(含少量Fe2O3、SiO2等杂质)。用辉铜矿冶炼铜的主要工艺流程如图所示:-|||-空气 X气体 富氧空气-|||-辉 磨细 高温脱硫 空气 焦炭 粗铜 吹炼-|||
-
11.辉铜矿的主要成分为Cu2S(含少量Fe2O3、SiO2等杂质)。用辉铜矿冶炼铜的主要工艺流程如图所示:-|||-空气 X气体 富氧空气-|||-辉 磨细
- 查看答案
-
在H2、H2O、H2SO4、Fe、Fe3O4五种物质中,属于单质的是()。
-
[填空题] 在H2、H2O、H2SO4、Fe、Fe3O4五种物质中,属于单质的是()。
- 查看答案