某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。_(2)S(O)_(4)+(H)_(2)(O)_(2) NaCl(O)_(3)+(Na)_(2)C(O)_(3) 试剂X (NH4)2C2O4-|||-旧电池 还原酸浸 除铁、铝 除铜 沉钴 煅烧 Co2O3-|||-材料-|||-滤液a-|||-试剂b 沉锂 锂盐已知:CoC2O4⋅2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O2−4离子生成Co(C2O4)2(n−1)−n而溶解。(l)“还原酸浸”过程中,LiCoO2发生反应的离子方程式为:___,该过程温度通常控制在40℃以下的原因是:___。(2)“除铝铁”过程的两种试剂的作用分别是___,___。(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式:___。并计算室温下该反应的平衡常数K=___,已知:25℃时Kap(CuS)=8.5×10−45,已知H2S在水中的的电离常数:K1=1.3×10−7,K2=7.l×10−15(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如下图所示:①随n(C2O2−4):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因___。②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是___。_(2)S(O)_(4)+(H)_(2)(O)_(2) NaCl(O)_(3)+(Na)_(2)C(O)_(3) 试剂X (NH4)2C2O4-|||-旧电池 还原酸浸 除铁、铝 除铜 沉钴 煅烧 Co2O3-|||-材料-|||-滤液a-|||-试剂b 沉锂 锂盐(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10−1mol⋅L−1,部分锂盐的溶解度数据如下表所示。 温度 Li2SO4 Li2CO30℃ 36.1g 1.33g100℃ 24.0g 0.72g结合数据分析,沉锂过程所用的试剂b是___(写化学式),相应的操作方法:向滤液a中加入略过量的试剂b,搅拌,___,___,洗涤干燥。检验沉淀洗净的方法是___。
某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。
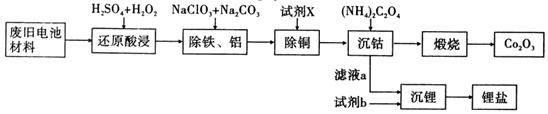
已知:CoC2O4⋅2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O2−4离子生成Co(C2O4)2(n−1)−n而溶解。
(l)“还原酸浸”过程中,LiCoO2发生反应的离子方程式为:___,该过程温度通常控制在40℃以下的原因是:___。
(2)“除铝铁”过程的两种试剂的作用分别是___,___。
(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式:___。并计算室温下该反应的平衡常数K=___,已知:25℃时Kap(CuS)=8.5×10−45,已知H2S在水中的的电离常数:K1=1.3×10−7,K2=7.l×10−15
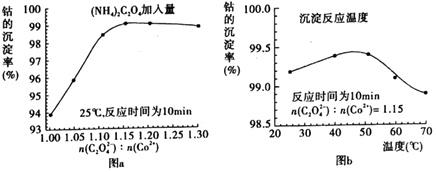
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如下图所示:
①随n(C2O2−4):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因___。
②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是___。
(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10−1mol⋅L−1,部分锂盐的溶解度数据如下表所示。
| 温度 | Li2SO4 | Li2CO3 |
| 0℃ | 36.1g | 1.33g |
| 100℃ | 24.0g | 0.72g |
参考答案与解析:
-
相关试题
-
废旧锂离子电池的正极材料主要成分是LiCoO_(2),还含有少量金属Al、Fe以及其他不溶性物质,采用如图1工艺流程回收其中的钴制备Co单质:NaOH溶液H2SO4 H2O2 氨水 氨水 HCl-||
-
废旧锂离子电池的正极材料主要成分是LiCoO_(2),还含有少量金属Al、Fe以及其他不溶性物质,采用如图1工艺流程回收其中的钴制备Co单质:NaOH溶液H2S
- 查看答案
-
在锂离子电池正极材料中,钴酸锂(LiCoO2)常用于手机电池材料。下列哪项不是钴酸锂的优点?
-
在锂离子电池正极材料中,钴酸锂(LiCoO2)常用于手机电池材料。下列哪项不是钴酸锂的优点?A. 高能量密度B. 良好的循环稳定性C. 低成本
- 查看答案
-
6.4 已知Na2 CO3(s )和H2O(1)可以生成三种水合盐:Na 2CO3·H2O(s),N a2CO3·7H2O(s )和-|||-Na2CO3·10H2O(s ),试求:-|||-(1)在
-
6.4 已知Na2 CO3(s )和H2O(1)可以生成三种水合盐:Na 2CO3·H2O(s),N a2CO3·7H2O(s )和-|||-Na2CO3·10
- 查看答案
-
CO2+2NaOH→Na2CO3+H2O H2S+2NaOH→Na2S+2H2O
-
[单选题]CO2+2NaOH→Na2CO3+H2O H2S+2NaOH→Na2S+2H2O为()的方程式。A . 碱洗反应B . 废碱氧化反应C . 黄油生成D . 干燥器甲烷再生
- 查看答案
-
碳酸钠与水可形成几种化合物:Na 2 CO 3 ·H 2 O(s)、Na 2 CO 3 ·7H 2 O(s)、Na 2 CO 3 ·10H 2 O(s)。试分析在101.325kPa下,与碳酸钠水溶液
-
碳酸钠与水可形成几种化合物:Na 2 CO 3 ·H 2 O(s)、Na 2 CO 3 ·7H 2 O(s)、Na 2 CO 3 ·10H 2 O(s)。试分析
- 查看答案
-
4.9某化合物A的水合晶体A·3H2 O脱水反应过程为-|||-cdot 3(H)_(2)O(s)=!=!= Acdot 2(H)_(2)O(s)+(H)_(2)O(g) K-|||-cdot 2(H
-
4.9某化合物A的水合晶体A·3H2 O脱水反应过程为-|||-cdot 3(H)_(2)O(s)=!=!= Acdot 2(H)_(2)O(s)+(H)_(2
- 查看答案
-
16.重铬酸钠(Na2Cr3O)广泛应用于医药和印染行业,用含铬矿渣(主要成分是Cr2O3,还含有少量-|||-Fe2O3和Al2O3)制备Na2Cr2O7的流程如下:-|||-O 2 H2O H2S
-
16.重铬酸钠(Na2Cr3O)广泛应用于医药和印染行业,用含铬矿渣(主要成分是Cr2O3,还含有少量-|||-Fe2O3和Al2O3)制备Na2Cr2O7的流
- 查看答案
-
常见的Na2CO3(s)水化物有Na2CO3·H2O(s)、Na2CO3·7H2O(s)、Na2CO3·10H2O(s)三种水合物,问在 101325 Pa 的压力下,能与Na2CO3水溶液及冰平衡共
-
常见的Na2CO3(s)水化物有Na2CO3·H2O(s)、Na2CO3·7H2O(s)、Na2CO3·10H2O(s)三种水合物,问在 101325 Pa 的
- 查看答案
-
从砷化镓废料(主要成分为GaAs、含Fe2O3、SiO2和CaCO3等杂质)中回收镓和砷的工艺流程如图所示:NaOH、H2O2 H2SO4 NaOH滤渣Ⅲ 尾液-|||-申化镓 ↓ ↑-|||-废料
-
从砷化镓废料(主要成分为GaAs、含Fe2O3、SiO2和CaCO3等杂质)中回收镓和砷的工艺流程如图所示:NaOH、H2O2 H2SO4 NaOH滤渣Ⅲ 尾液
- 查看答案
-
硫酸与水可组成三种化合物:H2SO4·H2O(s)、H2SO4·2H2O(s)、H2SO4·4H2O(s),在一定压力下,能与硫酸水溶液共存的化合物最多有几种( )
-
硫酸与水可组成三种化合物:H2SO4·H2O(s)、H2SO4·2H2O(s)、H2SO4·4H2O(s),在一定压力下,能与硫酸水溶液共存的化合物最多有几种(
- 查看答案