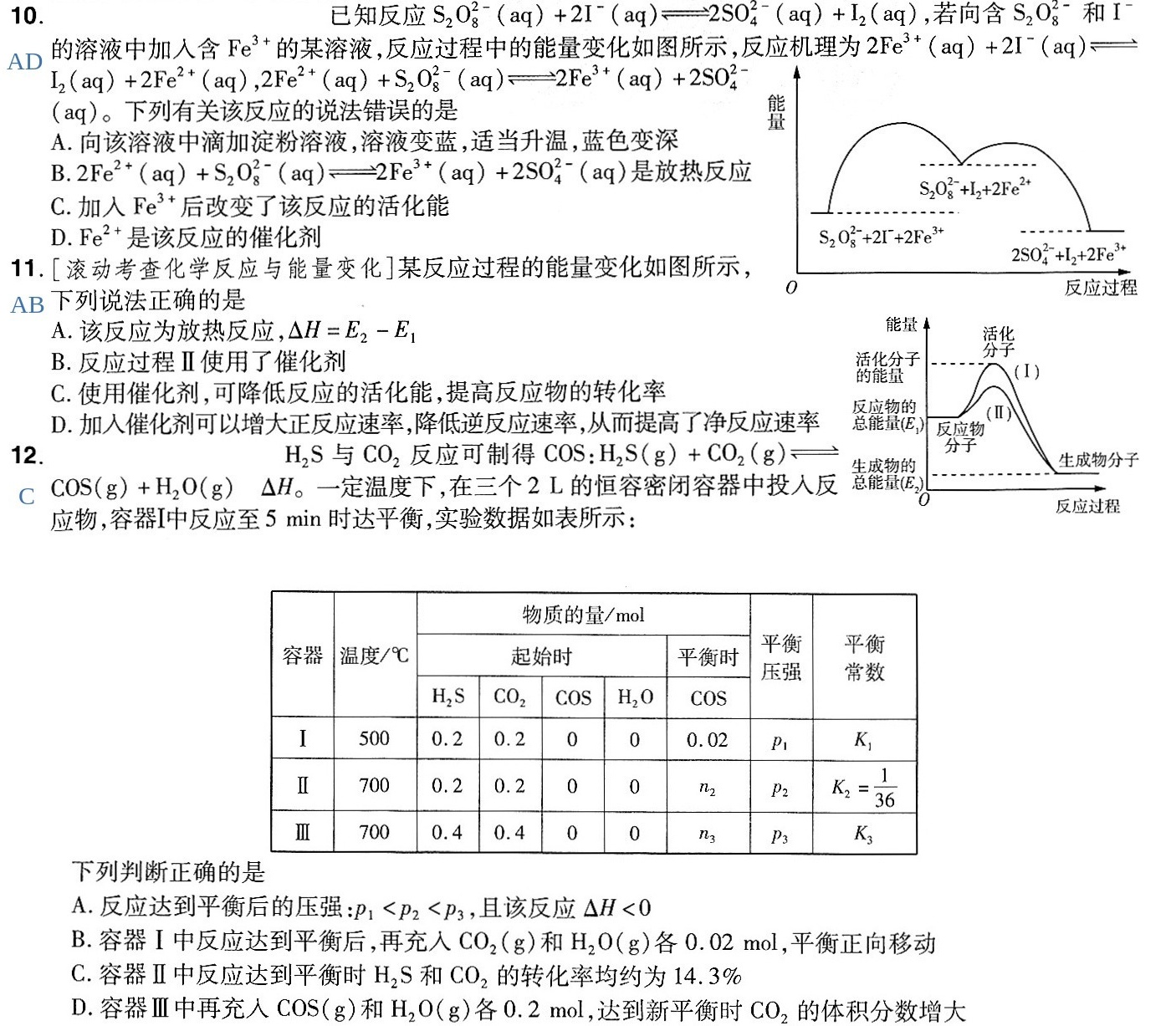
已知反应-|||-S2O2^(2-)(aq)+21^- (aq)=2SO2^(2-)(aq)+l2(an)-|||-AD的溶液中加入含 (e)^3+ 的某溶液,反应 过程中的能量变化如图 所示,反应机理为 (Fe)^3+(aq)+(21)^-(aq)leftharpoons -|||-(aq)=2SO2^(2-)(aq)+l2(an)-|||-_(2)(aq)+2(Fe)^2+(aq), (Fe)^2+(aq)+({S)_(2)(O)_(8)}^2-(aq)leftharpoons 2F(e)^3+(aq)+2(S{O)_(4)}^2--|||-_(2)(aq)+2(Fe)^2+(aq), (Fe)^2+(aq)+({S)_(2)(O)_(8)}^2-(aq)leftharpoons 2F(e)^3+(aq)+2(S{O)_(4)}^2--|||-(aq)。下列有关该反应的说法错误的是-|||-A.向该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色变深-|||-B. (Fe)^2+(aq)+(S)_(2)(O)_(8)^2-(aq)leftharpoons 2(Fe)^3+(aq)+2S(O)_(4)^2-(aq) 是放热反应-|||-C.加入 ^3+ 后改变了该反应的活化能-|||-D. ^2+ 是该反应的催化剂-|||-量-|||-2Fe^2+-|||-_(2)({O)_(8)}^2-+(21)^-+2(Fe)^3+-|||-2SO4^(2-)+I2+2Fe^(3+)-|||-0 反应过程-|||-11.[滚动考查化学反应与能量变化]某反应过程的能量变化如图所示,-|||-AB下列说法正确的是 0-|||-A.该反应为放热反应, Delta H=(E)_(2)-(E)_(1)-|||-B.反应过程Ⅱ使用了催化剂-|||-C.使用催化剂,可降低反应的活化能,提高反应物的转化率-|||-D.加入催化剂可以增大正反应速率,降低逆反应速率,从而提高了净反应速率-|||-能量↑-|||-活化分子 活化-|||-的能量 (I)-|||-反应物的 Ⅱ)-|||-总能量(E1) 反应物-|||-分子-|||-成物的 生成物分子-|||-总能量(E2)-|||-0 反应过程-|||-12. H2S与CO2反应可制得 cos ((H)_(2)S(g)+C(O)_(2)(g)leftharpoons 成物的 分子-|||-C cos (g)+(H)_(2)O(g) Delta (H)_(0) 一定温度下,在三个2L的恒容密闭容器中投入反 总能量(E2)-|||-应物,容器I中反应至5min时达平衡,实验数据如表所示: 0-|||-物质的量 /mol-|||-容器 温度/℃ 起始时 平衡时 平衡 平衡-|||-压强 常数-|||-H2S CO2 COS H2O COS-|||-I 500 0.2 0.2 0 0 0.02 p1 K-|||-Ⅱ 700 0.2 0.2 0 0 2 p2 _(2)=dfrac (1)(36)-|||-Ⅲ 700 0.4 0.4 0 0 3 P3 K3-|||-下列判断正确的是-|||-A.反应达到平衡后的压强: _(1)lt (P)_(2)lt (P)_(3), 且该反应 Delta Hlt 0-|||-B.容器I中反应达到平衡后,再充入CO2(g)和H2O(g )各0.02mol,平衡正向移动-|||-C.容器Ⅱ中反应达到平衡时H2S和CO2的转化率均约为14.3%-|||-D.容器Ⅲ中再充入COS(g)和H2O(g)各0.2 mol,达到新平衡时CO2的体积分数增大
参考答案与解析:
-
相关试题
-
11.已知某原电池反应:-|||-:(aq)+2(Cl)^2+(aq)+:(H)_(2)O(l)arrow 3HCl(aq)(aq)+(Cr{O)_(4)}^-(aq)+8(H)^+(aq)-|||-
-
11.已知某原电池反应:-|||-:(aq)+2(Cl)^2+(aq)+:(H)_(2)O(l)arrow 3HCl(aq)(aq)+(Cr{O)_(4)}^-
- 查看答案
-
2、25℃时,反应 ^2+(aq)+(Ag)^+(aq)=!=!= (Fe)^3+(aq)+Ag(s) 的标准平衡常数 ^theta =3.-|||-2。在含有 https:/img.zuoyeban
-
2、25℃时,反应 ^2+(aq)+(Ag)^+(aq)=!=!= (Fe)^3+(aq)+Ag(s) 的标准平衡常数 ^theta =3.-|||-2。在含有
- 查看答案
-
反应式:Ba(OH)2(aq)+HC2O4(aq)→H2O(l)+BaC2O4(
-
[单选题]反应式:Ba(OH)2(aq)+HC2O4(aq)→H2O(l)+BaC2O4(s)表示发生了下列何种反应()A . 氧化还原B . 络合C . 中和D . 歧化
- 查看答案
-
15.写出下列电池的电极反应及电池反应:-|||-(1) |AgCl(g)|KCl(aq)|(H)_(2)(Cl)_(2)(s)|Hg-|||-(2)Ag|AgBr|Br (aq)|| (e)^3+,
-
15.写出下列电池的电极反应及电池反应:-|||-(1) |AgCl(g)|KCl(aq)|(H)_(2)(Cl)_(2)(s)|Hg-|||-(2)Ag|Ag
- 查看答案
-
根据反应2 S_2 O_3^ (2-)+l_2=S_4 O_6^ (2-)+2 l^ (-)构成原电池,查表得phi ^ theta (l_2/l^ (-) )=0.535 V, phi
-
根据反应2 S_2 O_3^ (2-)+l_2=S_4 O_6^ (2-)+2 l^ (-)构成原电池,查表得phi ^ theta (l_2/l^ (
- 查看答案
-
【题目】将下列反应组成原电池(温度为298.15K)2I^-(a)+2Fe^(3+)+(aq)=I_2(s)+2Fe^(2+)(aq)(1)计算原电池的标准电动势;(2)计算反应的标准摩尔吉布斯函数变
-
【题目】将下列反应组成原电池(温度为298.15K)2I^-(a)+2Fe^(3+)+(aq)=I_2(s)+2Fe^(2+)(aq)(1)计算原电池的标准电动
- 查看答案
-
工业上常用NaHSO3处理含Cr2O7^2-的废液,反应的离子方程式为:5H+ +Cr2O7^2- +3HSO3^- →2Cr^3+ +3SO4^2- +4H2O下列判断错误的是( )
-
工业上常用NaHSO3处理含Cr2O7^2-的废液,反应的离子方程式为:5H+ +Cr2O7^2- +3HSO3^- →2Cr^3+ +3SO4^2- +4H2
- 查看答案
-
4.16 一溶液中 (S{O)_(4)}^2- 及 (C{O)_(3)}^2- 的浓度均为 .10molcdot (dm)^-3 ,向其中逐滴加入 ^2+ 溶液。-|||-试通过计算说明:-|||-(
-
4.16 一溶液中 (S{O)_(4)}^2- 及 (C{O)_(3)}^2- 的浓度均为 .10molcdot (dm)^-3 ,向其中逐滴加入 ^2+ 溶液
- 查看答案
-
H2O2的分解反应为: H2O2(aq) → H2O(l) + 1/2O2(g),下列表示的瞬时速度中,正确的是………………………………………………………………………………( )
-
H2O2的分解反应为: H2O2(aq) → H2O(l) + 1/2O2(g),下列表示的瞬时速度中,正确的是………………………………………………………………
- 查看答案
-
薈课程名称:普通化学(A)卷螈一、填空题(每空2分,共30分)袅1.反应2MnO4-(aq)+10Cl-(aq)+16H+(aq)=2Mn2+(aq)+5Cl2+8H2O(l)的标准蒂平衡常数表达式为
-
薈课程名称:普通化学(A)卷螈一、填空题(每空2分,共30分)袅1.反应2MnO4-(aq)+10Cl-(aq)+16H+(aq)=2Mn2+(aq)+5Cl2
- 查看答案