测得某电池在298K时的E=1.228V,在该温度下可逆放电2F时电池吸热49.12kJ,若电池反应的Delta;rHm不随温度而变,求 (1)电池在298K时的((dfrac {OE)(OT))}_(p)的值是多少? (2)若((dfrac {OE)(OT))}_(p)是不随T而变的量,计算318K时的E及放电2F的Delta;H; (3)证明((dfrac {OE)(OT))}_(p)确实是不随T而变化的。
测得某电池在298K时的E=1.228V,在该温度下可逆放电2F时电池吸热49.12kJ,若电池反应的Delta;rHm不随温度而变,求 (1)电池在298K时的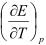 的值是多少? (2)若
的值是多少? (2)若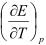 是不随T而变的量,计算318K时的E及放电2F的Delta;H; (3)证明
是不随T而变的量,计算318K时的E及放电2F的Delta;H; (3)证明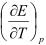 确实是不随T而变化的。
确实是不随T而变化的。
参考答案与解析:
-
相关试题
-
7996 V , Ag Br 在 298K 时的 活度积 K sp = 4.79 × 10 -13 , (1) 写出电极反应和电池反应; (2) 当电池可逆地输出 2mol 电子的电荷量时,求 298
-
7996 V , Ag Br 在 298K 时的 活度积 K sp = 4.79 × 10 -13 , (1) 写出电极反应和电池反应; (2) 当电池可逆地输
- 查看答案
-
电池Cu(s)|CuAC2(0.1mol+kg-1)|AgAc(s),Ag(s)在298K时,电动势E=0.372V,当温度升至308K时,E=0.374V已知298K时φ(Ag+Ag)=0.800V
-
电池Cu(s)|CuAC2(0.1mol+kg-1)|AgAc(s),Ag(s)在298K时,电动势E=0.372V,当温度升至308K时,E=0.374V已知
- 查看答案
-
电池Zn(S)ZnCl2(0.05mol-kg-1)AgCl(s)Ag(s)的电动势与温度的关系为E/V=1.015-4.92×10-(T/K-298)(1)写出电池反应(2)计算298K时上述电池可
-
电池Zn(S)ZnCl2(0.05mol-kg-1)AgCl(s)Ag(s)的电动势与温度的关系为E/V=1.015-4.92×10-(T/K-298)(1)写
- 查看答案
-
298K 时,要使电池 Na(Hg)(a 1 )|Na + (aq )| Na(Hg)(a 2 )成为自发电池,则 a 1 > a 2 。
-
298K 时,要使电池 Na(Hg)(a 1 )|Na + (aq )| Na(Hg)(a 2 )成为自发电池,则 a 1 > a 2 。A. 正确B. 错误
- 查看答案
-
9.36 在298K时,某电池的电池反应为-|||-.(s)+Cu(Br)_(2)(aq)=!=!= Pb(Br)_(2)(s)+Cu(s)-|||-其中CuBr2的质量摩尔浓度为 (2)求电池的标准
-
9.36 在298K时,某电池的电池反应为-|||-.(s)+Cu(Br)_(2)(aq)=!=!= Pb(Br)_(2)(s)+Cu(s)-|||-其中CuB
- 查看答案
-
9.36 在298K时,某电池的电池反应为-|||-.(s)+Cu(Br)_(2)(aq)=!=!= Pb(Br)_(2)(s)+Cu(s)-|||-其中CuBr2的质量摩尔浓度为 (2)求电池的标准
-
9.36 在298K时,某电池的电池反应为-|||-.(s)+Cu(Br)_(2)(aq)=!=!= Pb(Br)_(2)(s)+Cu(s)-|||-其中CuB
- 查看答案
-
计算温度高于298K的半电池反应的标准电极电位的方法有()。
-
[多选题] 计算温度高于298K的半电池反应的标准电极电位的方法有()。A . 用电子的热力学性质计算B . 根据海尔根孙公式进行计算C . 与标准氢电极加在一起计算D . 根据氢气的燃烧热进行计算
- 查看答案
-
有电池 (s)|ZnS(O)_(4)(0.01mol)KKg(H)^-1)|(A)_(2)S(O)_(4)(s)|Ag(s), 在298K时,电池-|||-电动势 =1.559V-|||-已知此温度下
-
有电池 (s)|ZnS(O)_(4)(0.01mol)KKg(H)^-1)|(A)_(2)S(O)_(4)(s)|Ag(s), 在298K时,电池-|||-电动
- 查看答案
-
电池Zn(S)|ZnCl2(0.05mol·kg-1)|AgCl(s)|Ag(s)的电动势与温度的关系为E/V=1.015-4.92×10-(T/K-298)(1)写出电池反应(2)计算298K时上述
-
电池Zn(S)|ZnCl2(0.05mol·kg-1)|AgCl(s)|Ag(s)的电动势与温度的关系为E/V=1.015-4.92×10-(T/K-298)(
- 查看答案
-
下列电池:Pt,H2(p?)|H2SO4(aq)|O2(p?),Pt298K时E=1.228V,已知液体水的生成热ΔfHm? (298K,H2O,l) = -2.851×105J·mol-1。(1)
-
下列电池:Pt,H2(p?)|H2SO4(aq)|O2(p?),Pt298K时E=1.228V,已知液体水的生成热ΔfHm? (298K,H2O,l) = -2
- 查看答案