N2O5. 电池:_. 已知反应_(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g)的一种可能的机理如下:① _(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g) _(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g)② _(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g) _(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g)③ _(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g) _(2)(O)_(5)(g)arrow 2N(O)_(2)(g)+dfrac (1)(2)(O)_(2)(g)若反应①生成的N2O2绝大部分是通过反应②变为反应物,只有少部分通过反应③变为产物(1) 导出反应的速率方程式;(2) 求反应的表观活化能E表.
解释:(1)蔗糖转化实验中旋光仪为什么用钠光灯做光源;(2)明矾净水的原理;
三(12分). N2O5(g)的分解反应为: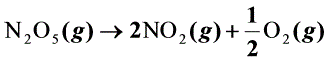 ,在600K时,该反应的速率常数k = 4.8×10-4s-1;
,在600K时,该反应的速率常数k = 4.8×10-4s-1;
(1) 求反应的半衰期;
(2) 若初始压力为50kPa, 问10min钟后总压力为多少?
(3) 若温度升高10K, 速率常数变为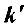 = 1.44×10-3s-1;求反应的活化能;
= 1.44×10-3s-1;求反应的活化能;
四(22分). 电池: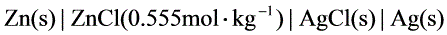 ;在298K时的电动势E = 1.105V, 已知
;在298K时的电动势E = 1.105V, 已知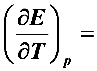
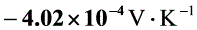 ,
,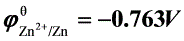 ,
,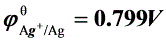 ,
,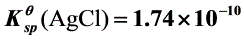 。
。
(1) 写出电池的电极反应及电池的总反应(设电荷转移数为2);
(2) 求电池反应在298K时的标准平衡常数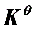 ;
;
(3) 上述电池中ZnCl溶液的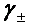 ;
;
(4) 上述电池可逆放电2F下, 电池反应热是多少?
(5) 若电池反应在恒压反应釜中进行,反应热多少?
五(10分). 已知反应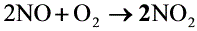 的一种可能的机理如下:
的一种可能的机理如下:
① 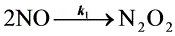
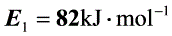
② 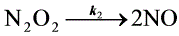
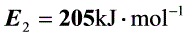
③ 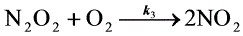
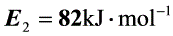
若反应①生成的N2O2绝大部分是通过反应②变为反应物,只有少部分通过反应③变为产物
(1) 导出反应的速率方程式;
(2) 求反应的表观活化能E表.
参考答案与解析:
-
相关试题
-
(O)_(2)(g)+(O)_(2)(g)=2(N)_(2)(O)_(5)(g)-|||-D.固态碘升华
-
(O)_(2)(g)+(O)_(2)(g)=2(N)_(2)(O)_(5)(g)-|||-D.固态碘升华
- 查看答案
-
3-2 某温度下,N2O5按下式分解:-|||-.(N)_(2)(O)_(5)(g)=!=!= 4N(O)_(2)(g)+(O)_(2)(g)-|||-由实验测得在67℃时N2O5浓度随时间的变化如下
-
3-2 某温度下,N2O5按下式分解:-|||-.(N)_(2)(O)_(5)(g)=!=!= 4N(O)_(2)(g)+(O)_(2)(g)-|||-由实验测
- 查看答案
-
N2O5分解反应的机理如下:-|||-① _(2)(O)_(5)xrightarrow [K]({K)_(1)}N(O)_(2)+N(O)_(3)-|||-② (O)_(2)+N(O)_(3)xrig
-
N2O5分解反应的机理如下:-|||-① _(2)(O)_(5)xrightarrow [K]({K)_(1)}N(O)_(2)+N(O)_(3)-|||-②
- 查看答案
-
N2O5分解反应的机理如下:-|||-① _(2)(O)_(5)xlongequal [高温]({K)_(i)}=(N{O)_(2)}+N(O)_(3)-|||-② (N{O)_(2)}+N(O)_(
-
N2O5分解反应的机理如下:-|||-① _(2)(O)_(5)xlongequal [高温]({K)_(i)}=(N{O)_(2)}+N(O)_(3)-|||
- 查看答案
-
298 K 时,N2O5(g)=N2O4(g)+12O2(g),该分解反应的半衰期 t12=5.7 h,此值与 N2O5(g) 的起始浓度无关。试求:该反应的速率常数。N2O5(g) 转化掉 90%
-
298 K 时,N2O5(g)=N2O4(g)+12O2(g),该分解反应的半衰期 t12=5.7 h,此值与 N2O5(g) 的起始浓度无关。试求:该反应的速
- 查看答案
-
已知:( bigcirc (1)C(H)_(5)OH(g)+dfrac (1)(2)(O)_(2)(g)=C(O)_(2)(g)+2(H)_(2)(g) Delta H=-192.9kJ/mol-|
-
已知:( bigcirc (1)C(H)_(5)OH(g)+dfrac (1)(2)(O)_(2)(g)=C(O)_(2)(g)+2(H)_(2)(g) De
- 查看答案
-
1.N2O5的分解反应 _(2)(O)_(5)arrow 2N(O)_(2)+(1/2)(O)_(2) 是一级反应,已知在某温度下的速率系数为-|||-.8times (10)^-4(s)^-1-||
-
1.N2O5的分解反应 _(2)(O)_(5)arrow 2N(O)_(2)+(1/2)(O)_(2) 是一级反应,已知在某温度下的速率系数为-|||-.8ti
- 查看答案
-
2.13 已知下列反应在298K时的标准摩尔焓变:-|||-(1) (C)_(2)(H)_(2)(g)+5(O)_(2)(g)=4C(O)_(2)(g)+2(H)_(2)O(g) (Delta )_(
-
2.13 已知下列反应在298K时的标准摩尔焓变:-|||-(1) (C)_(2)(H)_(2)(g)+5(O)_(2)(g)=4C(O)_(2)(g)+2(H
- 查看答案
-
反应2N2(g)+O2(g)→2N2O(g),在298K时,ΔrHmθ为164.
-
[填空题] 反应2N2(g)+O2(g)→2N2O(g),在298K时,ΔrHmθ为164.0kJ.mol-1,则反应ΔU=()。
- 查看答案
-
例8 N2O5分解反应的历程如下:-|||-(i) _(2)(O)_(5)xlongequal [高温]({K)_(1)}N(O)_(2)+(N{O)_(3)}-|||-(ii) (N{O)_(2)}
-
例8 N2O5分解反应的历程如下:-|||-(i) _(2)(O)_(5)xlongequal [高温]({K)_(1)}N(O)_(2)+(N{O)_(3)}
- 查看答案