试用计算说明向CuSO4溶液中加入KI是否会产生白色沉淀?并计算下列反应的平衡常数:2Cu2+ +4I- = 2CuI +I2(已知:φy(Cu2+/Cu+) = 0.158 V; φy(I2/I-) = 0.537V;Ksp (CuI) =1.2710-12)
试用计算说明向CuSO4溶液中加入KI是否会产生白色沉淀?并计算下列反应的平衡常数:2Cu2+ +4I- = 2CuI +I2(已知: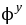 (Cu2+/Cu+) = 0.158 V;
(Cu2+/Cu+) = 0.158 V; 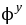 (I2/I-) = 0.537V;Ksp (CuI) =1.2710-12)
(I2/I-) = 0.537V;Ksp (CuI) =1.2710-12)
参考答案与解析:
-
相关试题
-
、17V,φ0I2/I-=0. 、535V ,因此 Cu2+ 离子不能氧 化 I- 离子。 2(×)10、标定 I2 溶液时,既可以用 Na2S2O3 滴定 I2 溶液,也可以用 I2 滴定Na2S2
-
、17V,φ0I2/I-=0. 、535V ,因此 Cu2+ 离子不能氧 化 I- 离子。 2(×)10、标定 I2 溶液时,既可以用 Na2S2O3 滴定 I
- 查看答案
-
计算KI浓度为1mol·L-1时,Cu2+/Cu+电对的条件电位(忽略离子强度的影响),并说明何以能发生下列反应:2Cu2++5I-=2Cu↓+I-3。
-
计算KI浓度为1mol·L-1时,Cu2+/Cu+电对的条件电位(忽略离子强度的影响),并说明何以能发生下列反应:2Cu2++5I-=2Cu↓+I-3。计算KI
- 查看答案
-
已知φy( Cu2+/Cu ) = 0.342 V,Cu(OH)2的Ksp= 2.2×10-20,那么φy( Cu(OH)2/Cu )为
-
已知φy( Cu2+/Cu ) = 0.342 V,Cu(OH)2的Ksp= 2.2×10-20,那么φy( Cu(OH)2/Cu )为A. -0.238 VB
- 查看答案
-
已知电极反应为Cu2+ + 2e = Cu 的标准电极电势为0.342V,则电极反应2Cu2+ - 4e =2Cu2+的标准电极电势应为( ) 。
-
已知电极反应为Cu2+ + 2e = Cu 的标准电极电势为0.342V,则电极反应2Cu2+ - 4e =2Cu2+的标准电极电势应为( ) 。A. 0.34
- 查看答案
-
【题目】已知电对 Cu^(2+)/Cu^+ 的 E^Θ=0.15V ,电对 I_2/I 的 E^Θ=0.54V ,CuI的K_pΘ=1.3*10^(-12) (1)试求氧化还原反应Cu^(2+)+2I
-
【题目】已知电对 Cu^(2+)/Cu^+ 的 E^Θ=0.15V ,电对 I_2/I 的 E^Θ=0.54V ,CuI的K_pΘ=1.3*10^(-12) (
- 查看答案
-
已知电池 Cu|Cu2+(a2)||Cu2+(a1)|Cu 和 Pt|Cu2+(a2),Cu+(a′)||Cu2+(a1),Cu+(a′)|Pt 的电动势分别为 E1 和 E2,则( )A.E1
-
已知电池 Cu|Cu2+(a2)||Cu2+(a1)|Cu 和 Pt|Cu2+(a2),Cu+(a′)||Cu2+(a1),Cu+(a′)|Pt 的电动势分别为
- 查看答案
-
5.单选题-|||-对于反应 (Cu)^2++4(I)^-leftharpoons 2CuI+(I)_(2) ,已知 ^2+ 的初始浓度为 .100molcdot (L)^-1 ^--|||-.500
-
5.单选题-|||-对于反应 (Cu)^2++4(I)^-leftharpoons 2CuI+(I)_(2) ,已知 ^2+ 的初始浓度为 .100molcdo
- 查看答案
-
计算题:计算下列反应的平衡常数,并判断反应方向:[HgCl4]2-+4I-=[H
-
[问答题] 计算题:计算下列反应的平衡常数,并判断反应方向:[HgCl4]2-+4I-=[HgI4]2-+4Cl-
- 查看答案
-
已知φθ(Fe3+/Fe2+)=0.77V,φθ(I2/I-)=0.54V,则标
-
[单选题]已知φθ(Fe3+/Fe2+)=0.77V,φθ(I2/I-)=0.54V,则标态下能发生的反应为()A .2Fe3++I2=2Fe2++2I-B .2Fe3++2I-=2Fe2++I2C .2Fe2++2I-=2Fe3++I2D .2Fe2++I2=2Fe3++2I-
- 查看答案
-
已知电极反应Cu2++2e-=Cu的为0.347V,则反应2Cu-4e-=2Cu
-
[单选题]已知电极反应Cu2++2e-=Cu的为0.347V,则反应2Cu-4e-=2Cu2+的值为()。A . -0.694VB . +0.694VC . -0.347VD . +0.347V
- 查看答案