, l4 t0 t2对碳硫及其化合物的研究有重要的意义. I.利用水煤气合成二甲醚(CH3OCH3)的三步反应如下: ①2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ.mol-1②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ.mol-1③CO(g)+H2O(g)═CO2+H2(g)△H=-41.3kJ.mol-1写出利用水煤气合成二甲醚(CH3OCH3) 的热化学方程式: ______ . Ⅱ.工业制硫酸的过程中利用反应2SO2(g)+O2(g), l4 t0 t2SO3(g)△H=-196.6kJ•mol-1,将SO2转化为SO3,尾气SO3可用NaOH溶液进行吸收.请回答下列问题: (1)写出该反应的化学平衡常数表达式: ______ . (2)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应,下列说法中正确的是 ______ (填字母). A.若反应速率v正(O2)=2v逆(SO3),则可以说明该可逆反应已达到平衡状态 B.保持温度和容器体积不变,再充入2mol SO2和1mol O2,n(SO3)/n(SO2)增大 C.平衡后移动活塞压缩气体,达到平衡时SO2、O2的百分含量减小,SO3的百分含量增大 D.平衡后升高温度,平衡常数K增大 (3)将一定量的SO2(g)和O2(g)分别通入到容积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据: 实验编号 温度/℃ 起始量/mol 平衡量/mol 达到平衡所需时间/min SO2 O2 SO2 O2 1 T1 4 2 X 0.8 6 2 T2 4 2 0.4 Y t 实验1从开始到反应达到化学平衡时,v(SO2)表示的反应速率为 ______ ;T1______ T2(选填“>”“<”或“=”),理由是 ______ (4)某SO2(g)和O2(g)反应体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图所示.若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是 ______ ;图中表示平衡混合物中SO2的转化率最高的一段时间是 ______ .
 对碳硫及其化合物的研究有重要的意义.
对碳硫及其化合物的研究有重要的意义.
I.利用水煤气合成二甲醚(CH3OCH3)的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ.mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ.mol-1
③CO(g)+H2O(g)═CO2+H2(g)△H=-41.3kJ.mol-1
写出利用水煤气合成二甲醚(CH3OCH3) 的热化学方程式: ______ .
Ⅱ.工业制硫酸的过程中利用反应2SO2(g)+O2(g)
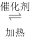 SO3(g)△H=-196.6kJ•mol-1,将SO2转化为SO3,尾气SO3可用NaOH溶液进行吸收.请回答下列问题:
SO3(g)△H=-196.6kJ•mol-1,将SO2转化为SO3,尾气SO3可用NaOH溶液进行吸收.请回答下列问题:
(1)写出该反应的化学平衡常数表达式: ______ .
(2)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应,下列说法中正确的是 ______ (填字母).
A.若反应速率v正(O2)=2v逆(SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,再充入2mol SO2和1mol O2,n(SO3)/n(SO2)增大
C.平衡后移动活塞压缩气体,达到平衡时SO2、O2的百分含量减小,SO3的百分含量增大
D.平衡后升高温度,平衡常数K增大
(3)将一定量的SO2(g)和O2(g)分别通入到容积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | X | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | Y | t |
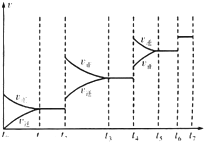
(4)某SO2(g)和O2(g)反应体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图所示.若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是 ______ ;图中表示平衡混合物中SO2的转化率最高的一段时间是 ______ .
参考答案与解析:
-
相关试题
-
在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)△H已知:①CO(g)+2H2(g)⇌CH3OH(g)△H1=-90.7kJ•
-
在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)△H已知:①CO(g)+2H2(g)⇌
- 查看答案
-
计算298 K下,CO(g)和CH3OH(g)的标准生成焓,并计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变。已知如下燃烧焓数据:ΔcH(298 K)(CH3OH(g))=-763.9
-
计算298 K下,CO(g)和CH3OH(g)的标准生成焓,并计算反应CO(g)+2H2(g)=CH3OH(g)的标准焓变。已知如下燃烧焓数据:ΔcH(298
- 查看答案
-
“碳中和”引起各国的高度重视,正成为科学家研究的主要课题。利用CO2合成二甲醚有两种工艺。工艺1:先在设备一加氢合成甲醇,涉及以下主要反应:Ⅰ.甲醇的合成:CO2(g)+3H2(g)⇌CH3OH(g)
-
“碳中和”引起各国的高度重视,正成为科学家研究的主要课题。利用CO2合成二甲醚有两种工艺。工艺1:先在设备一加氢合成甲醇,涉及以下主要反应:Ⅰ.甲醇的合成:CO
- 查看答案
-
氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用。涉及反应如下:反应Ⅰ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH1=-206.2kJ⋅mol-1反应Ⅱ:CO(g)+H2O(g)⇌CO
-
氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用。涉及反应如下:反应Ⅰ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH1=-206.2kJ⋅mol-
- 查看答案
-
已知:CH3CH2CH2CH3(g)+O2(g)4CO2(g)+5H2O(l)&
-
[单选题]已知:CH3CH2CH2CH3(g)+O2(g)4CO2(g)+5H2O(l)ΔH=-2878kJ/mol;(CH3)2CHCH3(g)+O2(g)4CO2(g)+5H2O(l)△H=-2869kJ/mol;下列说法正确的是()。A . 正丁烷分子储存的能量大于异丁烷分子B . 正丁烷的稳定性大于异丁烷C . 异丁烷转化为正丁烷的过程是一个放热过程D . 异丁烷分子中的碳氢键比正丁烷的多
- 查看答案
-
5.(醛和酮)-|||-下面反应的主产物是什么?-|||-CH3OH H3CO OCH3 OCH3 CH Q-|||-H2SO4-|||-1 2 3 4
-
5.(醛和酮)-|||-下面反应的主产物是什么?-|||-CH3OH H3CO OCH3 OCH3 CH Q-|||-H2SO4-|||-1 2 3 4
- 查看答案
-
试判断下列分子哪些是极性的。(1)HBr(2)I2(3)CCl4(4)CH2Cl2(5)CH3OH(6)CH3OCH3
-
试判断下列分子哪些是极性的。(1)HBr(2)I2(3)CCl4(4)CH2Cl2(5)CH3OH(6)CH3OCH3试判断下列分子哪些是极性的。(1)HBr(
- 查看答案
-
[题目]试判断下列分子哪些是极性的。-|||-(1)HBr(2)I2(3)CCl4-|||-(4)CH2Cl2(5)CH3OH(6)CH3OCH3
-
[题目]试判断下列分子哪些是极性的。-|||-(1)HBr(2)I2(3)CCl4-|||-(4)CH2Cl2(5)CH3OH(6)CH3OCH3
- 查看答案
-
合成气(CO和H2)是重要的工业原料气。(1)合成气制备甲醇:CO(g)+2H2(g)=CH3OH(g)。CO的结构式为C≡O,估算该反应的ΔH需要 ____ (填数字)种化学键的键能数据。(2)合成
-
合成气(CO和H2)是重要的工业原料气。(1)合成气制备甲醇:CO(g)+2H2(g)=CH3OH(g)。CO的结构式为C≡O,估算该反应的ΔH需要 ____
- 查看答案
-
在标准压力和 298 K 时,计算如下反应的 ΔrG⊖m(298 K),从所得的数值判断反应的可能性。(1)CH4(g)+12O2(g)→CH3OH(l);(2)C(石墨)+2H2(g)+12O2(g
-
在标准压力和 298 K 时,计算如下反应的 ΔrG⊖m(298 K),从所得的数值判断反应的可能性。(1)CH4(g)+12O2(g)→CH3OH(l);(2
- 查看答案