煤炭地下气化可将煤高效转化为富含氢气的煤气,H2主要通过水蒸气的还原析氢得到。反应如下(温度为T0):反应ⅰC(s)+H2O(g)⇌H2(g)+CO(g) Δ(H)_(1)=+131.5kJ•mo(l)^-1 K1反应ⅱCO(g)+H2O(g)⇌H2(g)+CO2(g) Δ(H)_(2)=-41.0kJ•mo(l)^-1 K2回答下列问题:(1)写出反应ⅰ平衡常数的表达式:K1= ____ 。(2)反应C(s)+2H2O(g)⇌2H2(g)+CO2(g)的ΔH= ____ kJ•mol-1,平衡常数K= ____ (用含K1、K2的代数式表示)。(3)氧交换机理常用于描述反应ⅰ的历程,包含如图所示两个过程,过程1为活性炭位C吸附H2O(g)形成碳氧复合物C(O),补充该过程的化学方程式:H2O+C= ____ +C(O)。过程1 过程2-|||-90 bigcirc -|||-bigcirc ○□ooo =00 bigcirc -|||-bigcirc ○○一。 bigcirc -|||-bigcirc C OH(4)温度为T0时,在恒容密闭容器中模拟水蒸气的还原析氢过程,下列说法正确的是 ____ 。A.适当减小压强能提高水蒸气的平衡转化率B.增加煤炭可以提高H2的平衡产率C.向容器内充入He可提高反应速率D.选择合适催化剂可以提高H2在单位时间内的产量(5)还原析氢过程中,煤层地下水含量过高会降低反应区温度,影响平衡时煤气(主要包含H2、CO与CO2)组成。煤气组成与煤层地下水含量的关系如图,曲线a是H2,曲线b是 ____ 。煤层地下水含量>0.3%时,H2占有量随煤层地下水含量增大逐渐 ____ (填“增大”、“减小”或“不变”),原因是 ____ 。过程1 过程2-|||-90 bigcirc -|||-bigcirc ○□ooo =00 bigcirc -|||-bigcirc ○○一。 bigcirc -|||-bigcirc C OH
煤炭地下气化可将煤高效转化为富含氢气的煤气,H2主要通过水蒸气的还原析氢得到。反应如下(温度为T0):反应ⅰC(s)+H2O(g)⇌H2(g)+CO(g) $Δ{H}_{1}=+131.5kJ•mo{l}^{-1}$ K1
反应ⅱCO(g)+H2O(g)⇌H2(g)+CO2(g) $Δ{H}_{2}=-41.0kJ•mo{l}^{-1}$ K2
回答下列问题:
(1)写出反应ⅰ平衡常数的表达式:K1= ____ 。
(2)反应C(s)+2H2O(g)⇌2H2(g)+CO2(g)的ΔH= ____ kJ•mol-1,平衡常数K= ____ (用含K1、K2的代数式表示)。
(3)氧交换机理常用于描述反应ⅰ的历程,包含如图所示两个过程,过程1为活性炭位C吸附H2O(g)形成碳氧复合物C(O),补充该过程的化学方程式:H2O+C= ____ +C(O)。
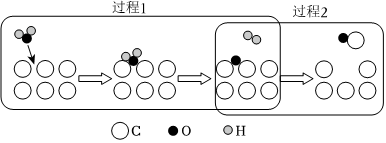
(4)温度为T0时,在恒容密闭容器中模拟水蒸气的还原析氢过程,下列说法正确的是 ____ 。
A.适当减小压强能提高水蒸气的平衡转化率
B.增加煤炭可以提高H2的平衡产率
C.向容器内充入He可提高反应速率
D.选择合适催化剂可以提高H2在单位时间内的产量
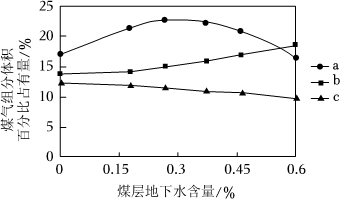
(5)还原析氢过程中,煤层地下水含量过高会降低反应区温度,影响平衡时煤气(主要包含H2、CO与CO2)组成。煤气组成与煤层地下水含量的关系如图,曲线a是H2,曲线b是 ____ 。煤层地下水含量>0.3%时,H2占有量随煤层地下水含量增大逐渐 ____ (填“增大”、“减小”或“不变”),原因是 ____ 。
参考答案与解析:
-
相关试题
-
器 0.50-|||-0.15-|||-0.05 c-|||-T0 T1 →增大-|||-温度T水煤气是H2的主要来源。研究CaO对C—H2O体系制H2的影响,涉及主要反应如下:C(s)+H2O(g)
-
器 0.50-|||-0.15-|||-0.05 c-|||-T0 T1 →增大-|||-温度T水煤气是H2的主要来源。研究CaO对C—H2O体系制H2的影响,
- 查看答案
-
水煤气反应:C(s)+H2O(g)=CO(g)+H2(g) 问:(1)此反应在298.15K时,H2O(g),CO(g)及H2(g) 的分压均为100kPa下能否向正方向进行?(2)(3)若升高温度能
-
水煤气反应:C(s)+H2O(g)=CO(g)+H2(g) 问:(1)此反应在298.15K时,H2O(g),CO(g)及H2(g) 的分压均为100kPa下能
- 查看答案
-
在823K,标准态下下列反应的θY:(1)CO2(g)+H2(g)=CO(g)+H2O(g) θY(2)CoO(s)+H2(g)=Co(s)+H2O(g) θY试求823K,标准态下反应(3)
-
在823K,标准态下下列反应的θY:(1)CO2(g)+H2(g)=CO(g)+H2O(g) θY(2)CoO(s)+H2(g)=Co(s)+H2O(g)
- 查看答案
-
18.已知:-|||-①H2O(g)=H2(g)+2O2(g) H=+241.88kJ/mol-|||-②C(s)+2O2(g )=CO(g) △H=-110.50.5kJ/mol-|||-③C(s)
-
18.已知:-|||-①H2O(g)=H2(g)+2O2(g) H=+241.88kJ/mol-|||-②C(s)+2O2(g )=CO(g) △H=-110.
- 查看答案
-
水煤气发生炉中共有C(s),H2O(g),CO(g), CO2(g)及H2(g)五种物质,它们之能发生下述反应:CO2(g)+ C(s) = 2CO(g) CO2(g) + H2(g) = CO(
-
水煤气发生炉中共有C(s),H2O(g),CO(g), CO2(g)及H2(g)五种物质,它们之能发生下述反应:CO2(g)+ C(s) = 2CO(g)
- 查看答案
-
为了提高CO在CO(g)+H2O(g) CO2(g)+H2(g)反应中的平衡转化率,可以…………………( )
-
为了提高CO在CO(g)+H2O(g) CO2(g)+H2(g)反应中的平衡转化率,可以…………………( )A. 增加CO的浓度(或分压)B. 增
- 查看答案
-
氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用。涉及反应如下:反应Ⅰ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH1=-206.2kJ⋅mol-1反应Ⅱ:CO(g)+H2O(g)⇌CO
-
氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用。涉及反应如下:反应Ⅰ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH1=-206.2kJ⋅mol-
- 查看答案
-
在298K时,H2(g)+1/2O2(g)=H2O(L),△H=-285.8kJ
-
[单选题]在298K时,H2(g)+1/2O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()A . 正反应速率增大,逆反应速率减小B . 正反应速率增大,逆反应速率增大C . 正反应速率减小,逆反应速率增大D . 正反应速率减小,逆反应速率减小
- 查看答案
-
已知下列反应的平衡常数:H2(g)+S(s)=H2S(g)①K1;S(s)+O2(g)=SO2(g)②K2。则反应H2(g)+SO2(g)=O2(g)+H2S(g)的平衡常数为
-
已知下列反应的平衡常数:H2(g)+S(s)=H2S(g)①K1;S(s)+O2(g)=SO2(g)②K2。则反应H2(g)+SO2(g)=O2(g)+H2S(
- 查看答案
-
在 723 K 时,将 0.10 mol H2(g) 和 0.20 mol CO2(g) 通入抽空的瓶中,发生如下反应:(1) H2(g)+CO2(g)⇌H2O(g)+CO(g),平衡后瓶中的总压为
-
在 723 K 时,将 0.10 mol H2(g) 和 0.20 mol CO2(g) 通入抽空的瓶中,发生如下反应:(1) H2(g)+CO2(g)⇌H2O
- 查看答案