10 分 298K时,在Ag+/Ag电极中加入过量I,设达到平衡时[I] = 0.10 mol·dm-3,而另一个电极为Cu2+/Cu,[Cu2+] = 0.010 mol·dm-3,现将两电极组成原电池,写出原电池的符号、电池反应式、并计算电池反应的平衡常数。 (Ag+/Ag) = 0.80 V, (Cu2+/Cu) = 0.34 V,Ksp(AgI) = 1.0 10-18
10 分 298K时,在Ag+/Ag电极中加入过量I,设达到平衡时[I] = 0.10 mol·dm-3,而另一个电极为Cu2+/Cu,[Cu2+] = 0.010 mol·dm-3,现将两电极组成原电池,写出原电池的符号、电池反应式、并计算电池反应的平衡常数。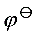 (Ag+/Ag) = 0.80 V,
(Ag+/Ag) = 0.80 V,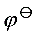 (Cu2+/Cu) = 0.34 V,Ksp(AgI) = 1.0 10-18
(Cu2+/Cu) = 0.34 V,Ksp(AgI) = 1.0 10-18
参考答案与解析:
-
相关试题
-
原电池:Cu│Cu2+(1.0mol·dm-3)‖[AuCl4]-(0.10 mol·dm-3), Cl-(0.10mol·dm-3)│Au已知:Eө(Au3+/Au) = 1.50 V,Eө([Au
-
原电池:Cu│Cu2+(1.0mol·dm-3)‖[AuCl4]-(0.10 mol·dm-3), Cl-(0.10mol·dm-3)│Au已知:Eө(Au3+
- 查看答案
-
在298.15时,两电对Fe3+/ Fe2+和Cu2+/Cu组成原电池,其中 c(Fe3+)=c(Fe2+)=c(Cu2+)=0.10 mol·L-1已知 :
-
在298.15时,两电对Fe3+/ Fe2+和Cu2+/Cu组成原电池,其中 c(Fe3+)=c(Fe2+)=c(Cu
- 查看答案
-
已知电极反应为Cu2+ + 2e = Cu 的标准电极电势为0.342V,则电极反应2Cu2+ - 4e =2Cu2+的标准电极电势应为( ) 。
-
已知电极反应为Cu2+ + 2e = Cu 的标准电极电势为0.342V,则电极反应2Cu2+ - 4e =2Cu2+的标准电极电势应为( ) 。A. 0.34
- 查看答案
-
25℃时,在Cu2+的氨水溶液中,平衡时c(NH3)=6.710-4mol·L-1,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2+形式存在.则[Cu(NH3)4]2+的
-
25℃时,在Cu2+的氨水溶液中,平衡时c(NH3)=6.710-4mol·L-1,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2
- 查看答案
-
Al3+、Fe3+、Ag+、Cu2+等金属离子中,与过量氨水反应,生成沉淀的是( )
-
Al3+、Fe3+、Ag+、Cu2+等金属离子中,与过量氨水反应,生成沉淀的是( )A. l3+、Fe3+、Cu2+B. Al3+、Fe3+C. Al3+、Fe
- 查看答案
-
查表得,298K时0.01mol•dm-3的KCl溶液的k=0.1413s•m-1,用同一个电导池测得0.01mol•dm-3的KCl溶液的电阻为1064Ω,0.01mol•dm-3的HAc溶液的电阻
-
查表得,298K时0.01mol•dm-3的KCl溶液的k=0.1413s•m-1,用同一个电导池测得0.01mol•dm-3的KCl溶液的电阻为1064Ω,0
- 查看答案
-
将铜丝插入浓度为1mol/LCuSO4溶液,银丝插入浓度为1mol/L的AgNO3溶液,组成原电池(E ag+/ag=0.779V E cu2+/cu=0.34V Kf(Cu(NH3)4)2+)=4.
-
将铜丝插入浓度为1mol/LCuSO4溶液,银丝插入浓度为1mol/L的AgNO3溶液,组成原电池(E ag+/ag=0.779V E cu2+/cu=0.34
- 查看答案
-
要配制450cm3pH=9.30的缓冲溶液,需用0.10mol·dm-3氨水和0.10 mol·dm-3盐酸各多少?若在此溶液中含有0.020mol·dm-3 MgCl2,能否产生Mg(OH)2沉淀?
-
要配制450cm3pH=9.30的缓冲溶液,需用0.10mol·dm-3氨水和0.10 mol·dm-3盐酸各多少?若在此溶液中含有0.020mol·dm-3
- 查看答案
-
计算KI浓度为1mol·L-1时,Cu2+/Cu+电对的条件电位(忽略离子强度的影响),并说明何以能发生下列反应:2Cu2++5I-=2Cu↓+I-3。
-
计算KI浓度为1mol·L-1时,Cu2+/Cu+电对的条件电位(忽略离子强度的影响),并说明何以能发生下列反应:2Cu2++5I-=2Cu↓+I-3。计算KI
- 查看答案
-
已知电池 Cu|Cu2+(a2)||Cu2+(a1)|Cu 和 Pt|Cu2+(a2),Cu+(a′)||Cu2+(a1),Cu+(a′)|Pt 的电动势分别为 E1 和 E2,则( )A.E1
-
已知电池 Cu|Cu2+(a2)||Cu2+(a1)|Cu 和 Pt|Cu2+(a2),Cu+(a′)||Cu2+(a1),Cu+(a′)|Pt 的电动势分别为
- 查看答案