某化学兴趣小组做了如图所示实验,当向乙烧杯中依次加入MnO2和H2O2溶液时,发现有大量气泡产生,并产生大量白雾,蜡烛燃烧更旺,但过一会儿逐渐熄灭。而甲烧杯中蜡烛一直持续燃烧。MnO2-|||-A-|||-200mL-|||-H2O2溶液-|||-甲 乙 乙【知识回忆】写出过氧化氢分解产生氧气的化学方程式: ____ 。【问题1】导致乙烧杯中蜡烛熄灭的原因是什么?【作出猜想】猜想一:燃烧产生的CO2使蜡烛熄灭;猜想二:白雾是水雾导致蜡烛熄灭;小组同学经过讨论,排除了猜想一,其理由是 ____ 。【实验1】向一只装有燃者蜡烛的烧杯中加入100℃水,另一只依次加入MnO2和H2O2溶液,若观察到 ____ 的现象,则猜想二正确。【查阅资料】水雾产生与H2O2溶液的溶质质量分数大小有关,并且H2O2溶液的溶质质量分数越大,产生的水雾越多。【问题2】为什么H2O2溶液的溶质质量分数越大水雾越多呢?【实验2】分别向三只烧杯依次加入MnO2和溶质质量分数的不同H2O2溶液测定温度变化。 H2O溶液 5% 10% 30% 温度变化曲线 MnO2-|||-A-|||-200mL-|||-H2O2溶液-|||-甲 乙 乙 MnO2-|||-A-|||-200mL-|||-H2O2溶液-|||-甲 乙 乙 MnO2-|||-A-|||-200mL-|||-H2O2溶液-|||-甲 乙 乙 【解释与结论】(1)该对比实验过程中不需要控制的条件是 ____ 。A.H2O2溶液的初始温度相同 B.反应开始的时间相同 C.二氧化锰的质量相同(2)根据实验2,可得出的一个结论是 ____ 。
某化学兴趣小组做了如图所示实验,当向乙烧杯中依次加入MnO2和H2O2溶液时,发现有大量气泡产生,并产生大量白雾,蜡烛燃烧更旺,但过一会儿逐渐熄灭。而甲烧杯中蜡烛一直持续燃烧。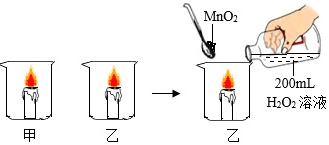
【知识回忆】写出过氧化氢分解产生氧气的化学方程式: ____ 。
【问题1】导致乙烧杯中蜡烛熄灭的原因是什么?
【作出猜想】猜想一:燃烧产生的CO2使蜡烛熄灭;
猜想二:白雾是水雾导致蜡烛熄灭;
小组同学经过讨论,排除了猜想一,其理由是 ____ 。
【实验1】向一只装有燃者蜡烛的烧杯中加入100℃水,另一只依次加入MnO2和H2O2溶液,若观察到 ____ 的现象,则猜想二正确。
【查阅资料】水雾产生与H2O2溶液的溶质质量分数大小有关,并且H2O2溶液的溶质质量分数越大,产生的水雾越多。
【问题2】为什么H2O2溶液的溶质质量分数越大水雾越多呢?
【实验2】分别向三只烧杯依次加入MnO2和溶质质量分数的不同H2O2溶液测定温度变化。
| H2O溶液 | 5% | 10% | 30% |
| 温度变化曲线 | 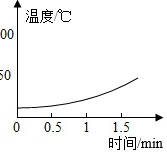 |
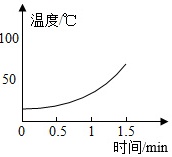 |
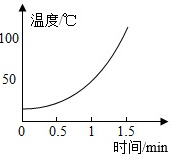 |
(1)该对比实验过程中不需要控制的条件是 ____ 。
A.H2O2溶液的初始温度相同 B.反应开始的时间相同 C.二氧化锰的质量相同
(2)根据实验2,可得出的一个结论是 ____ 。
参考答案与解析:
-
相关试题
-
3.[2022·河北]下列实验设计不能达到相-|||-应实验目的的是 ()-|||-选项 实验目的 实验设计-|||-A 加入MnO2-|||-鉴别H2O2溶液-|||-和H2O-|||-鉴别NaCl
-
3.[2022·河北]下列实验设计不能达到相-|||-应实验目的的是 ()-|||-选项 实验目的 实验设计-|||-A 加入MnO2-|||-鉴别H2O2溶液
- 查看答案
-
某小组探究H2O2氧化性、还原性的变化规律。资料:Na2O2+2H2O═2NaOH+H2O2、H2O2═2H2O+O2↑(1)制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。向A中加入过
-
某小组探究H2O2氧化性、还原性的变化规律。资料:Na2O2+2H2O═2NaOH+H2O2、H2O2═2H2O+O2↑(1)制备H2O2:将Na2O2溶于冰水
- 查看答案
-
^2+ 有 __ 性,能与H2O2反应产生MnO2-|||-猜想3.-|||-(3)探究猜想2的合理性,并分析I中没有产生棕褐色固体的原因,设计实验如下:-|||-序号 实验 试剂 现象-|||-i
-
^2+ 有 __ 性,能与H2O2反应产生MnO2-|||-猜想3.-|||-(3)探究猜想2的合理性,并分析I中没有产生棕褐色固体的原因,设计实验如下:-||
- 查看答案
-
夏天,小丽将冰水和热水分别注入常温下的两只透明烧杯中,如图2所示,一会儿发现两只
-
[单选题]夏天,小丽将冰水和热水分别注入常温下的两只透明烧杯中,如图2所示,一会儿发现两只烧杯的杯壁上都有一部分出现小水珠,变得模糊了。针对这一现象,下列说法正确的是()A . 甲、乙两杯都在内壁出现了水珠B . 甲、乙两杯都在外壁出现了水珠C . 甲杯的内壁出现了水珠,乙杯的外壁出现了水珠D . 甲杯的外壁出现了水珠,乙杯的内壁出现了水珠
- 查看答案
-
某兴趣小组的同学向一定体积的 rm Ba((OH))_(2) 溶液中逐渐加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如右图所示。A-|||-C-|||-B.-|||-o a-|||-时间(1)
-
某兴趣小组的同学向一定体积的 rm Ba((OH))_(2) 溶液中逐渐加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如右图所示。A-|||-C-|||-
- 查看答案
-
二氧化锰因应用广泛而备受关注。某研究小组采用如图装置通过焙烧MnCO3制取MnO2,发生反应的化学方程式为:2MnCO3+O2(underline(;△;))/(;)2CO2+2MnO2。↑剩余固体的
-
二氧化锰因应用广泛而备受关注。某研究小组采用如图装置通过焙烧MnCO3制取MnO2,发生反应的化学方程式为:2MnCO3+O2(underline(;△;))/
- 查看答案
-
已知,从标准电极电势看,MnO2不能氧化Cl-,但用MnO2加浓盐酸,可以生成C
-
[单选题]已知,从标准电极电势看,MnO2不能氧化Cl-,但用MnO2加浓盐酸,可以生成Cl2,这是因为()。A . 两个相差不大B . 酸性增强,也增加C . Cl-浓度增加,减少D . 以上三个因素都有
- 查看答案
-
MnO2可被金属粉还原。
-
[判断题] MnO2可被金属粉还原。A . 正确B . 错误
- 查看答案
-
根据碱性溶液中锰元素的电势图:MnO 4 - MnO 4 2- MnO 2 可知电对MnO 4 - / MnO 2 的E 值为()。
-
根据碱性溶液中锰元素的电势图:MnO 4 - MnO 4 2- MnO 2 可知电对MnO 4 - / MnO 2 的E 值为()。A. 0.56VB. 0.5
- 查看答案
-
称取软锰矿0.1000g,试样经过烧碱熔后,得到MnO42-,煮沸溶液以除去过氧化物,酸化后,此时MnO42-歧化为MnO4-和MnO2,然后滤去MnO2,用0.1012mol/LFe2+标准溶液滴定
-
称取软锰矿0.1000g,试样经过烧碱熔后,得到MnO42-,煮沸溶液以除去过氧化物,酸化后,此时MnO42-歧化为MnO4-和MnO2,然后滤去MnO2,用0
- 查看答案