(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1是高铁电池的模拟实验装置:①该电池放电时正极的电极反应式为_____________________;若维持电流强度为1 A,电池工作十分钟,理论消耗Zn________g(已知F=96 500 C·mol-1)。②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向________(填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向________(填“左”或“右”)移动。③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_____________________________________________________________________________________________。(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,电池正极的电极反应式为____________________________,A是________。(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如下图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发生的电极反应式为_____________________________________________________________________________________。解析:(1)①放电时高铁酸钾为正极,正极发生还原反应,电极反应式为FeO+4H2O+3e-===Fe(OH)3↓+5OH-;若维持电流强度为1 A,电池工作十分钟,转移电子的物质的量为1×10×60÷96 500=0.006 217 6 mol。理论消耗Zn的质量0.006 217 6 mol÷2×65≈0.2 g(已知F=96 500 C·mol-1)。②电池工作时,阴离子移向负极,阳离子移向正极,所以盐桥中氯离子向右移动;若用阳离子交换膜代替盐桥,则钾离子向左移动。③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有使用时间长、工作电压稳定。(2)该电池的本质反应是合成氨反应,电池中氢气失去电子,在负极发生氧化反应,氮气得电子在正极发生还原反应,则正极反应式为N2+8H++6e-===2NH,氨气与HCl反应生成氯化铵,则电解质溶液为氯化铵溶液。(3)工作时电极b作正极,O2-由电极b移向电极a;该装置是原电池,通入一氧化碳的电极a是负极,负极上一氧化碳失去电子发生氧化反应,电极反应式为CO+O2--2e-===CO2。
(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1是高铁电池的模拟实验装置:①该电池放电时正极的电极反应式为_____________________;若维持电流强度为1 A,电池工作十分钟,理论消耗Zn________g(已知F=96 500 C·mol-1)。②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向________(填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向________(填“左”或“右”)移动。③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_____________________________________________________________________________________________。(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,电池正极的电极反应式为____________________________,A是________。(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如下图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发生的电极反应式为_____________________________________________________________________________________。解析:(1)①放电时高铁酸钾为正极,正极发生还原反应,电极反应式为FeO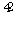 +4H2O+3e-===Fe(OH)3↓+5OH-;若维持电流强度为1 A,电池工作十分钟,转移电子的物质的量为1×10×60÷96 500=0.006 217 6 mol。理论消耗Zn的质量0.006 217 6 mol÷2×65≈0.2 g(已知F=96 500 C·mol-1)。②电池工作时,阴离子移向负极,阳离子移向正极,所以盐桥中氯离子向右移动;若用阳离子交换膜代替盐桥,则钾离子向左移动。③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有使用时间长、工作电压稳定。(2)该电池的本质反应是合成氨反应,电池中氢气失去电子,在负极发生氧化反应,氮气得电子在正极发生还原反应,则正极反应式为N2+8H++6e-===2NH
+4H2O+3e-===Fe(OH)3↓+5OH-;若维持电流强度为1 A,电池工作十分钟,转移电子的物质的量为1×10×60÷96 500=0.006 217 6 mol。理论消耗Zn的质量0.006 217 6 mol÷2×65≈0.2 g(已知F=96 500 C·mol-1)。②电池工作时,阴离子移向负极,阳离子移向正极,所以盐桥中氯离子向右移动;若用阳离子交换膜代替盐桥,则钾离子向左移动。③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有使用时间长、工作电压稳定。(2)该电池的本质反应是合成氨反应,电池中氢气失去电子,在负极发生氧化反应,氮气得电子在正极发生还原反应,则正极反应式为N2+8H++6e-===2NH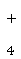 ,氨气与HCl反应生成氯化铵,则电解质溶液为氯化铵溶液。(3)工作时电极b作正极,O2-由电极b移向电极a;该装置是原电池,通入一氧化碳的电极a是负极,负极上一氧化碳失去电子发生氧化反应,电极反应式为CO+O2--2e-===CO2。
,氨气与HCl反应生成氯化铵,则电解质溶液为氯化铵溶液。(3)工作时电极b作正极,O2-由电极b移向电极a;该装置是原电池,通入一氧化碳的电极a是负极,负极上一氧化碳失去电子发生氧化反应,电极反应式为CO+O2--2e-===CO2。
参考答案与解析:
-
相关试题
-
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。高铁酸钾(K 2FeO 4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。湿法、干法制备高铁酸盐的原理如下所
-
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。高铁酸钾(K 2FeO 4)是一种新型、高效、多功能水处理剂,且不会造成二次
- 查看答案
-
8.写出下列原电池的电极反应式和电池反应式,并计算原电池的电动势(298K):-|||-|(Fe)^2+(1.0molcdot (L)^-1) jí ^-(1.0molcdot (L)^-1)/(Cl
-
8.写出下列原电池的电极反应式和电池反应式,并计算原电池的电动势(298K):-|||-|(Fe)^2+(1.0molcdot (L)^-1) jí ^-(1.
- 查看答案
-
回答下列问题:(1)利用(Fe)、(Cu)作电极设计成原电池,可以确定它们活动性的相对强弱.试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出正极反应式.正极反应式:___.(
-
回答下列问题:(1)利用(Fe)、(Cu)作电极设计成原电池,可以确定它们活动性的相对强弱.试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,
- 查看答案
-
用磷酸铁锂作为正极材料的锂离子电池,电池负极是石墨,电池单体标称电压为()。
-
用磷酸铁锂作为正极材料的锂离子电池,电池负极是石墨,电池单体标称电压为()。A. 2.1VB. 3.6VC. 3.2VD. 1.2V
- 查看答案
-
铁酸钙是一种()高()好的粘结相。
-
[填空题] 铁酸钙是一种()高()好的粘结相。
- 查看答案
-
97、 用磷酸铁锂作为正极材料的锂离子电池,电池负极是石墨,电池单体标称电压为( )。
-
97、 用磷酸铁锂作为正极材料的锂离子电池,电池负极是石墨,电池单体标称电压为( )。A. 3.2VB. 1.2VC. 3.6VD. 2.1V
- 查看答案
-
10.298K时,已知如下三个电极的反应及标准还原电极电势,-|||-如将电极(1)与(3)和(2)与(3)分别组成自发电池(设活度均为1),-|||-写出电池的书面表达式、电池反应式并计算电池的标准
-
10.298K时,已知如下三个电极的反应及标准还原电极电势,-|||-如将电极(1)与(3)和(2)与(3)分别组成自发电池(设活度均为1),-|||-写出电池
- 查看答案
-
有一原电池Ag | AgCl(s) | Cl-(a=1)||Cu2+(a=0、01)| Cu。(1)写出上述原电池的反应式;(2)计算该原电池在25℃时的电动势E;(3)25℃时,原电池反应的 吉布斯
-
有一原电池Ag | AgCl(s) | Cl-(a=1)||Cu2+(a=0、01)| Cu。(1)写出上述原电池的反应式;(2)计算该原电池在25℃时的电动势
- 查看答案
-
在碳钢原电池中,铁相当于电池的()
-
[单选题]在碳钢原电池中,铁相当于电池的()A . 正B . 负C . 什么都不表示
- 查看答案
-
当蓄电池的放电率高10H放电率时,电池容量较小。
-
[判断题]当蓄电池的放电率高10H放电率时,电池容量较小。A.对B.错
- 查看答案